
【题目】氧化钪![]() 广泛应用在合金电光源,催化剂,激活剂等领域,下列流程图是用钪精矿生产氧化钪的方法之一:
广泛应用在合金电光源,催化剂,激活剂等领域,下列流程图是用钪精矿生产氧化钪的方法之一:![]() 钪精矿主要成分是钪的氧化物,硅铁等氧化物
钪精矿主要成分是钪的氧化物,硅铁等氧化物![]()
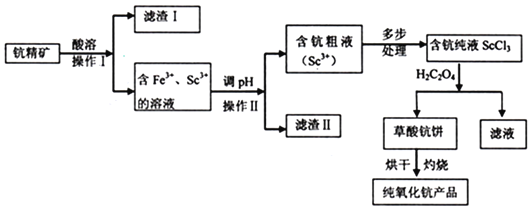
回答下列问题:
![]() 滤渣I是______
滤渣I是______![]() 填化学式
填化学式![]() 。在实验室里,操作Ⅰ必要的玻璃仪器有烧杯、______。
。在实验室里,操作Ⅰ必要的玻璃仪器有烧杯、______。
![]() 调pH的目的是______,如何检验含钪粗液中不含
调pH的目的是______,如何检验含钪粗液中不含![]() 离子______。
离子______。
![]() 写出制取草酸钪饼的化学方程式______。
写出制取草酸钪饼的化学方程式______。
![]() 写出草酸钪饼在空气中灼烧的化学方程式______,每生成
写出草酸钪饼在空气中灼烧的化学方程式______,每生成![]() ,转移的电子数为______。
,转移的电子数为______。
![]() 某工厂用
某工厂用![]() 的钪精矿制备纯氧化钪,得到纯产品
的钪精矿制备纯氧化钪,得到纯产品![]() ,则钪精矿中钪的质量分数是______
,则钪精矿中钪的质量分数是______![]() 假设Sc的利用率为
假设Sc的利用率为![]() 。
。
【答案】![]() 漏斗、玻璃棒 除去
漏斗、玻璃棒 除去![]() 沉淀
沉淀![]() 取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含
取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含![]() 离子
离子 ![]()
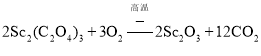
![]()
![]()
【解析】
利用钪精矿为原料![]() 主要成分为
主要成分为![]() ,还含有
,还含有![]() 、MnO等杂质
、MnO等杂质![]() 生产氧化钪,钪精矿加入盐酸酸溶,过滤分离出滤渣I为
生产氧化钪,钪精矿加入盐酸酸溶,过滤分离出滤渣I为![]() ,滤液中含
,滤液中含![]() 、
、![]() ,为使钪浸出,加入氨水调节溶液pH,过滤分离出滤渣II主要成分是
,为使钪浸出,加入氨水调节溶液pH,过滤分离出滤渣II主要成分是![]() ,含
,含![]() 的溶液多步处理得到
的溶液多步处理得到![]() ,加草酸发生
,加草酸发生![]() ,草酸钪“灼烧”氧化发生
,草酸钪“灼烧”氧化发生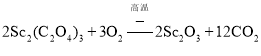 ,以此来解答。
,以此来解答。
![]() 由上述分析可知,滤渣I为
由上述分析可知,滤渣I为![]() ,操作I为过滤,需要的仪器为漏斗、玻璃棒、玻璃棒,故答案为:
,操作I为过滤,需要的仪器为漏斗、玻璃棒、玻璃棒,故答案为:![]() ;漏斗、玻璃棒;
;漏斗、玻璃棒;
![]() 调pH的目的是除去
调pH的目的是除去![]() 沉淀
沉淀![]() ,检验含钪粗液中不含
,检验含钪粗液中不含![]() 离子的方法为取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含
离子的方法为取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含![]() 离子,故答案为:除去
离子,故答案为:除去![]() 沉淀
沉淀![]() ;取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含
;取最后一次洗涤液,向其中滴加KSCN溶液,若未出现血红色,则证明不含![]() 离子;
离子;
![]() 制取草酸钪饼的化学方程式为
制取草酸钪饼的化学方程式为![]() ;
;
![]() 草酸钪饼在空气中灼烧的化学方程式为
草酸钪饼在空气中灼烧的化学方程式为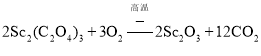 ;由反应可知生成
;由反应可知生成![]() 时转移12mol电子,每生成
时转移12mol电子,每生成![]() ,转移的电子数为
,转移的电子数为![]() ,故答案为:
,故答案为: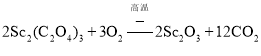 ;
;![]() ;
;
![]() 用
用![]() 的钪精矿制备纯氧化钪,得到纯产品
的钪精矿制备纯氧化钪,得到纯产品![]() ,则钪精矿中钪的质量分数是
,则钪精矿中钪的质量分数是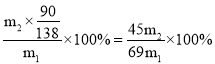 ,故答案为:
,故答案为:![]() 。
。


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是

A.ZY、ZW、W2X的水溶液都显酸性
B.原子半径大小:W>R>X,简单离子半径大小:R>W>X
C.W的氢化物与R的氢化物水溶液的酸性比较,前者强于后者,可证明非金属性:R>W
D.Z与X、Z与R两种元素形成的化合物中均可能存在共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型解热镇痛抗炎药扑炎痛的结构如图所示,下列关于扑炎痛的叙述正确的是
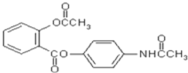
A.该物质的分子式为![]()
B.该物质的核磁共振氢谱上共有9个峰
C.该物质与浓溴水反应生成白色沉淀
D.该物质在酸性条件下水解最终可以得到4种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酯类物质M是一种药物的主要合成中间体,其合成路线如下:

已知以下信息:
①芳香烃A的相对分子质量在100~110之间,1molA完全燃烧可消耗10molO2。
②H的核磁共振氢谱显示其有3种氢。
③RCH=CH2![]() RCHClCH3
RCHClCH3
④RX+Mg![]() RMgX(X代表卤素)
RMgX(X代表卤素)
⑤
![]()


回答下列问题:
(1)A的结构简式为______,H中官能团的名称为______。
(2)由E和H生成M的化学方程式为______。
(3)属于氧化反应的是______(填序号)。
(4)同时符合下列条件的E的同分异构体有______种(不考虑立体异构),其中苯环上一氯代物只有两种的结构简式为______。(任写一种)
①能与碳酸钠溶液发生反应;②苯环上的取代基数目有2个
(5)请结合所给信息,由苯合成苯乙烯,合成路线如图所示,请回答下列问题。

试剂②为______,最后一步反应的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以A、B为原料制备线型高分子化合物M和抗凝血药N的一种路线如下(部分反应条件和试剂略去):

已知:I. 烃A的密度是相同条件下H2密度的14倍;
I.![]()
II. ![]()
请回答下列问题:
(1)B的化学名称为____。F的结构简式为______。
(2)N中含氧官能团的名称为 _______。
(3)D→E的反应类型为_____。
(4)I的核磁共振氢谱中有_______组吸收峰。G分子中最多有____个原子共平面。
(5)B+C→M的化学方程式为_______。
(6)同时满足下列条件的J的同分异构体有_____种(不考虑立体异构)。
①苯环上连有2个取代基
②1mol该物质与足量的NaHCO3反应,生成2molCO2
(7)参照上述信息和合成路线,以HO![]() CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备
CH3和(CH3CO)2O为起始原料(其他无机试剂任选),设计制备![]() 的合成路线 _______。
的合成路线 _______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72LH2(已折算成标准状况),甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25g/L。请回答下列问题:
(1)甲的化学式是__________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________。
(3)气体丙与金属镁反应的产物是__________(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式__________。有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之__________(已知Cu2O+2H+=Cu+Cu2++H2O)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Na2CO3和NaHCO3的混合溶液中c(![]() )、c(
)、c(![]() )与pH的关系如图所示[假设c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1]。下列说法正确的是( )
)与pH的关系如图所示[假设c(Na2CO3)+c(NaHCO3)=0.100 mol·L-1]。下列说法正确的是( )

A.图中E点溶液表示浓度均为0.05 mol·L-1的Na2CO3和NaHCO3溶液混合后所得到的溶液
B.pH=10的溶液中:c(H+)+c(Na+)+c(H2CO3)=c(OH-)+c(![]() )
)
C.pH=11的溶液中:c(![]() )<c(
)<c(![]() )
)
D.向E点溶液中加入等体积0.100 mol·L-1的NaOH溶液,c(![]() )与c(
)与c(![]() )之和保持不变
)之和保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯和乙炔为原料合成化工原料E的路线如下:

回答下列问题:
(1)以下有关苯和乙炔的认识正确的是 ______
![]() 苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
苯和乙炔都能使溴水褪色,前者为化学变化,后者为物理变化
![]() 苯和乙炔在空气中燃烧都有浓烟产生
苯和乙炔在空气中燃烧都有浓烟产生
![]() 苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
苯与浓硝酸混合,水浴加热55~60℃,生成硝基苯
![]() 聚乙炔是一种有导电特性的高分子化合物
聚乙炔是一种有导电特性的高分子化合物
(2)A的名称 ______。
(3)生成B的化学方程式为 ______,反应类型是 ______。
(4)C的结构简式为 ______ ,C的分子中一定共面的碳原子最多有 ______ 个。
(5)与D同类别且有二个六元环结构(环与环之间用单键连接)的同分异构体有______种,请任写两种同分异构体的结构简式:______。
(6)参照上述合成路线,设计一条以乙炔和必要试剂合成环丙烷的路线: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO),无色气体,易溶于水,有特殊的刺微气味,对人眼、鼻等有刺激作用。40%甲醛溶液沸点为96℃,易挥发。甲醛在碱性溶液中具有极强的还原性。为探究过量甲醛和新制Cu(OH)2反应的产物成分,进行如下研究:
(1)在下图装置中进行实验,向a中加入0.5mol·L-1CuSO4溶液50mL和5 mol·L-1 NaOH溶液100mL,振荡,再加入40%的甲醛溶液40mL,缓慢加热a,在65℃时回流20分钟后冷却至室温。反应过程中观察到有棕色固体生成,最后变成红色,并有气体产生。

①仪器b的名称是____________。
②仪器c的作用为____________。
③能说明甲醛具有还原性的实验现象是____________。
(2)查阅资料发现气体产物是副反应产生的。为确认气体产物中含H2不含CO,将装置A和如下图所示的装置连接后进行实验。

①依次连接的合理顺序为:A→B→_____→_____→_____→_____→G,________
②装置B的作用是_______________。
③确认气体产物中含H2而不含CO的现象是_________________________。
(3)已知:![]() 。证明a中甲醛的碳元素未被氧化成+4价的实验方案为:取少量a中反应后的清液,____________________,则说明甲醛的碳元素未被氧化成+4价。
。证明a中甲醛的碳元素未被氧化成+4价的实验方案为:取少量a中反应后的清液,____________________,则说明甲醛的碳元素未被氧化成+4价。
(4)为研究红色固体产物的组成,进行如下实验(以下每步均充分反应);

已知:ⅰ.Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色) ![]() [Cu(NH3)4]2+(蓝色)
[Cu(NH3)4]2+(蓝色)
ⅱ.2Cu+8NH3·H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O
通过上述实验,可以得出红色固体产物主要是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com