
【题目】下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水:C1-+2H2O![]() H2↑+Cl2↑+OH-
H2↑+Cl2↑+OH-
B.铅蓄电池充电时阳极反应式为:PbSO4–2e-+2H2O=PbO2+4H++SO42―
C.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH-
D.钢铁发生电化学腐蚀的正极反应式:Fe–2e-=Fe2+
【答案】B
【解析】
A. 该离子方程式的原子不守恒,正确的是2Cl-+2H2O ![]() H2↑+Cl2↑+2OH-,故A错误;
H2↑+Cl2↑+2OH-,故A错误;
B. 电池充电时电池的正极接电源的正极,电池的负极接电源的负极,铅蓄电池正极为PbO2,其电极反应式为PbO2+2e-+SO42-+4H+=PbSO4+2H2O,根据电解原理,阳极反应式为PbSO4-2e-+2H2O=PbO2++SO42-+4H+,故B正确;
C. 根据原电池的工作原理,负极上失去电子,电极反应式为H2-2e-+2OH-=2H2O,正极反应式为O2+2H2O+4e-=4OH-,故C错误;
D. 正极上得到电子,发生还原反应,钢铁腐蚀中负极反应式为Fe-2e-=Fe2+,故D错误;
答案:B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业含铬(Ⅵ)污水能污染水源,被人体吸收后易积累而导致器官癌变,必须经无害化处理后才能排放。青岛某污水处理厂的工艺流程如图:
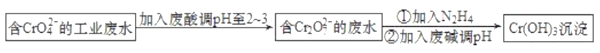
回答下列问题:
(1)CrO42-氧化性较弱,酸性条件下转化为具有较强氧化性的Cr2O72-的离子方程式为__。
(2)已知N2H4与Cr2O72-反应生成无毒气体。若要处理Cr2O72-浓度为0.01mol·L-1的废水1m3,至少需要加入N2H4__kg。
(3)含有SO32-的废水可以代替N2H4处理酸性含铬(Ⅵ)废水,用离子方程式表示其反应原理__。
(4)Cr(OH)3的化学性质与Al(OH)3相似。上述流程中“②加入废碱调pH”时要控制溶液的pH不能过高,原因是__。
(5)含铬(Ⅵ)污水也可用电解法处理。用铁和石墨作电极电解污水,Cr2O72-在阳极区转化为Cr3+,随着电解的进行,溶液pH逐渐增大,Cr3+转化为Cr(OH)3沉淀除去。
①该电解装置中用___作阳极,阳极区除生成Cr(OH)3外还有_沉淀(写化学式)。
②阴极电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯胺![]() 是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
已知:①![]() 和NH3相似,与盐酸反应生成易溶于水的盐
和NH3相似,与盐酸反应生成易溶于水的盐![]()
②用硝基苯制取苯胺的反应原理: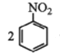 +3Sn+12HCl
+3Sn+12HCl![]()
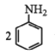 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
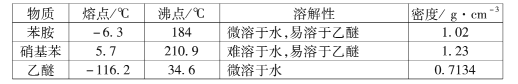
I.比较苯胺与氨气的性质
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为____;用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是____。
Ⅱ.制备苯胺
往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50% NaOH溶液,至溶液呈碱性。

(2)冷凝管的进水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为____。
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气,烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液。

ii.往所得水溶液中加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺2.79g。
(4)装置B无需用到温度计,理由是____。
(5)操作i中,为了分离混合物,取出烧瓶C前,应先打开止水夹d,再停止加热,理由是____。
(6)该实验中苯胺的产率为____。
(7)欲在不加热条件下除去苯胺中的少量硝基苯杂质,简述实验方案:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列说法错误的是
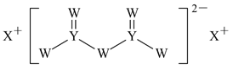
A.气态氢化物的稳定性:Z>Y
B.W和Y形成的晶体为共价晶体
C.Y单质的熔点低于X单质
D.化合物M中W、Y都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,该材料中Ni为主要活泼元素,通常可以简写为LiAO2。充电时总反应为LiAO2+nC=Li1-xAO2+LixCn(0<x<1),工作原理如图所示,下列说法正确的是
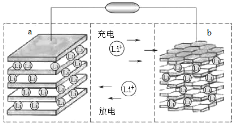
A.放电时Ni元素最先失去电子
B.放电时电子从a电极由导线移向b电极
C.充电时的阳极反应式为LiAO2 xe-= Li1-xAO2 + xLi+
D.充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述不正确的是( )
A. 表示反应4CO(g)+2NO2(g)N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a
表示反应4CO(g)+2NO2(g)N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a
B. b表示25℃时,分别加水稀释体积均为100 mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数小于CH3COOH的电离平衡常数
b表示25℃时,分别加水稀释体积均为100 mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数小于CH3COOH的电离平衡常数
C. c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1 > p2
c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1 > p2
D. d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的贵重金属,其化合物在催化剂研究和光电材料等方面应用广泛。回答下列问题:
(1)在铜的配合物中,H2O、NH3、CO等常用作配体。
①基态Cu2+的价电子轨道表示式为_________。
②H、C、N、O元素中,元素的第一电离能最高的为_____,元素电负性由大到小的顺序为________。
③水溶液中有H3O+、H5O2+、H9O4+等微粒的形式。H3O+中O的杂化轨道类型为_____,其H-O-H键角_______(填“>”或“<”)H2O中H-O-H的键角。H5O2+内部存在氢键,H5O2+的结构式可表示为__________。
④Cu2Cl2·2CO·2H2O是一种配合物,其结构如图所示:![]() ,其中每个Cu原子能与其他原子形成_________个配位键。
,其中每个Cu原子能与其他原子形成_________个配位键。
(2)CuCl结构属于立方晶系,其晶胞如图所示:

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。则A原子分数坐标为_________。
②晶胞中距离每个Cu+最近的Cl-的个数为_______,若晶胞的棱长为a pm,晶体的密度为ρ g·cm-3,计算阿伏加德罗常数NA=________(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出COS的电子式__________________,C与O形成共价键时,共用电子对会偏向__________原子,判断依据是___________。
(2)已知COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1=-34kJ/mol
H2S(g)+CO2(g) △H1=-34kJ/mol
CO(g)+H2O(g)![]() H2(g)+CO2(g) △H2=-41kJ/mol
H2(g)+CO2(g) △H2=-41kJ/mol
写出H2S与CO反应生成COS的热化学方程式__________________________________。
100℃时将CO与H2S按物质的量比为1∶1充入反应器中,达平衡后CO的转化率α=33.3%,此时反应的平衡常数k=________________________。
(3)在充有催化剂的恒压密闭容器中进行反应。设起始充入的n(CO)∶n(H2S)=m,相同时间内测得H2S转化率与m和温度(T)的关系如图所示。
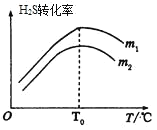
①m1________m2(填>、<或=)
②温度高于T0时,H2S转化率减小的可能原因为_________
a.反应停止了 b.反应的△H变大
c.反应达到平衡 d.催化剂活性降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰是一.种重要的化工原料,在农业、电化学和建筑等领域均有广泛应用。以含锰废料(含有MnO2 、CuO、Fe和少量CaO)为原料制备MnSO4的一种流程如下:
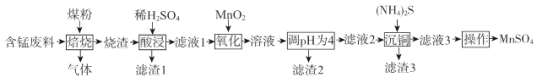 已知:
已知:
I .烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:
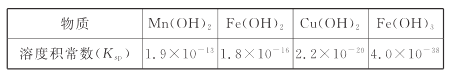
回答下列问题:
(1)“焙烧”过程加入煤粉的主要作用为___________________________。
(2)“酸浸”时所加稀H2SO4不宜过量太多的原因为______________________________.滤渣1的主要成分为_____________________(填化学式)。
(3)“氧化”过程中主要反应的离子方程式为__________________。
(4)“调pH为4”的目的为______________________;若“溶液”中c(Cu2+ )=0.022 mol/L,“滤液2”的体积是“溶液”体积的2倍,则“调pH为4”时Cu2+是否开始沉淀____________(通过计算说明)。
(5)(NH4)2S的电子式为___________________。
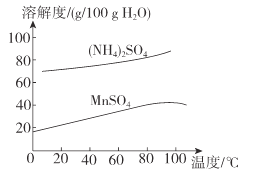
(6)已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩_______、过滤 、洗涤、干燥;其中用乙醇代替水洗涤的原因为__________,需控制温度为____( 填选项字母)得到产品最多。
A.10°C B.40 °C C.60 °C D.100°C
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com