
【题目】(1)写出COS的电子式__________________,C与O形成共价键时,共用电子对会偏向__________原子,判断依据是___________。
(2)已知COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1=-34kJ/mol
H2S(g)+CO2(g) △H1=-34kJ/mol
CO(g)+H2O(g)![]() H2(g)+CO2(g) △H2=-41kJ/mol
H2(g)+CO2(g) △H2=-41kJ/mol
写出H2S与CO反应生成COS的热化学方程式__________________________________。
100℃时将CO与H2S按物质的量比为1∶1充入反应器中,达平衡后CO的转化率α=33.3%,此时反应的平衡常数k=________________________。
(3)在充有催化剂的恒压密闭容器中进行反应。设起始充入的n(CO)∶n(H2S)=m,相同时间内测得H2S转化率与m和温度(T)的关系如图所示。
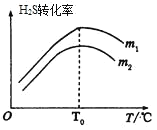
①m1________m2(填>、<或=)
②温度高于T0时,H2S转化率减小的可能原因为_________
a.反应停止了 b.反应的△H变大
c.反应达到平衡 d.催化剂活性降低
【答案】![]() O(氧) C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C CO(g)+H2S(g)
O(氧) C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C CO(g)+H2S(g)![]() COS(g)+H2(g)△H2=-7kJ/mol 0.25 > d
COS(g)+H2(g)△H2=-7kJ/mol 0.25 > d
【解析】
(1)根据共价键的相关知识解答;
(2) COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1=-34kJ/mol①,
H2S(g)+CO2(g) △H1=-34kJ/mol①,
CO(g)+H2O(g)![]() H2(g)+CO2(g) △H2=-41kJ/mol②,
H2(g)+CO2(g) △H2=-41kJ/mol②,
运用盖斯定律CO(g)+H2S(g)![]() COS(g)+H2(g) △H,由②-①所得,计算可得;平衡常数,可用三段式进行计算;
COS(g)+H2(g) △H,由②-①所得,计算可得;平衡常数,可用三段式进行计算;
(3)①在充有催化剂的恒压密闭容器中只进行反应,设起始充入的n(CO)∶n(H2S)=m,m越大说明CO量越多,两种反应物增加一种会提高另一种的转化率;
②温度高于T0,H2S转化率减小是因为温度升高,催化剂活性减弱,反应减慢,平衡逆向进行,H2S转化率减小。
(1) COS的电子式![]() ;C与O形成共价键时,由于C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C,共用电子对会偏向氧原子,故答案为:
;C与O形成共价键时,由于C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C,共用电子对会偏向氧原子,故答案为:![]() ;O(氧);C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C;
;O(氧);C与O同周期,核电荷数O>C,原子半径O<C,非金属性O>C;
(2) COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H1=-34kJ/mol①,
H2S(g)+CO2(g) △H1=-34kJ/mol①,
CO(g)+H2O(g)![]() H2(g)+CO2(g) △H2=-41kJ/mol②,
H2(g)+CO2(g) △H2=-41kJ/mol②,
运用盖斯定律CO(g)+H2S(g)![]() COS(g)+H2(g) △H,由②-①所得△H=-41kJ/mol-(-34kJ/mol)= -7kJ/mol,故H2S与CO反应生成COS的热化学方程式为CO(g)+H2S(g)
COS(g)+H2(g) △H,由②-①所得△H=-41kJ/mol-(-34kJ/mol)= -7kJ/mol,故H2S与CO反应生成COS的热化学方程式为CO(g)+H2S(g)![]() COS(g)+H2(g) △H=-7kJ/mol;CO与H2S按物质的量比为1∶1充入反应器中,设CO与H2S的起始量各为3mol,达平衡后CO的转化率α=33.3%,可用三段式进行计算;
COS(g)+H2(g) △H=-7kJ/mol;CO与H2S按物质的量比为1∶1充入反应器中,设CO与H2S的起始量各为3mol,达平衡后CO的转化率α=33.3%,可用三段式进行计算;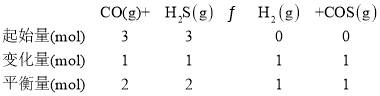 ,体积相同,则K=
,体积相同,则K=![]() ,故答案为:CO(g)+H2S(g)
,故答案为:CO(g)+H2S(g)![]() COS(g)+H2(g) △H=-7kJ/mol;0.25;
COS(g)+H2(g) △H=-7kJ/mol;0.25;
(3)①在充有催化剂的恒压密闭容器中只进行反应,设起始充入的n(CO)∶n(H2S)=m,m越大说明CO量越多,两种反应物增加一种会提高另一种的转化率,则m1>m2,故答案为:>;
②温度高于T0,H2S转化率减小是因为温度升高,催化剂活性减弱,反应减慢,平衡逆向进行,H2S转化率减小,可逆反应处于动态平衡,△H只与反应物和生成物的总能量有关,故答案为:d。


科目:高中化学 来源: 题型:
【题目】CH4 是一种清洁、高效、具有优良的环保性能的燃料,其燃烧热为890.3kJ·mol-1。它可以作为燃料电池的燃料。
(1)写出甲烷燃烧的热化学方程式:____________________________________________;
(2)以甲烷、空气、氢氧化钾溶液为原料,惰性电极为电极可以构成燃料电池。该电池的负极反应式为____
(3)用(2)中的燃料电池为电源,以石墨为电极电解500mL滴有酚酞的NaCl溶液,装置如图所示:
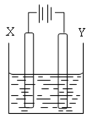
①请写出电解过程中阴极附近观察到的现象:____________________。
②当燃料电池消耗2.8L O2(标准状况下)时,计算此时NaCl溶液的pH=__________ (假设溶液的体积不变,气体全部从溶液中逸出)。在Y极通过的电子的物质的量为:_______________________。
③电解之后,要使溶液恢复原状,应该向溶液中加入物质 _________(填名称)。溶液中Cl―流向 ____________极(填“X”或“Y”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列用来表示物质变化的化学用语中,正确的是( )
A.电解饱和食盐水:C1-+2H2O![]() H2↑+Cl2↑+OH-
H2↑+Cl2↑+OH-
B.铅蓄电池充电时阳极反应式为:PbSO4–2e-+2H2O=PbO2+4H++SO42―
C.氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH-
D.钢铁发生电化学腐蚀的正极反应式:Fe–2e-=Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是
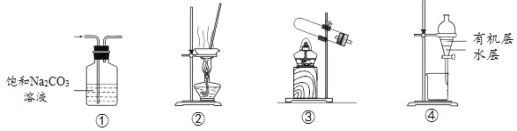
A.用①装置除去CO2中含有的少量SO2
B.用②装置蒸干饱和AlCl3溶液制备AlCl3晶体
C.用③装置加热NH4Cl固体制取NH3
D.用④装置分离乙酸乙酯与水的混合液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用氯酸钠(NaClO3)为原料制取,(常温下ClO2为气态),下列说法错误的是
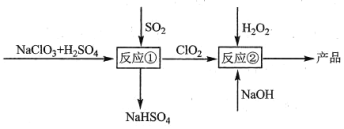
A.反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B.反应①后生成的气体要净化后进入反应②装置
C.升高温度,有利于反应②提高产率
D.反应②中有气体生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧(DO)的多少是衡量水体水质的重要指标。某化学小组测定某河流中氧的含量,经查阅有关资料了解到溶解氧测定可用“碘量法”,
Ⅰ.用已准确称量的硫代硫酸钠(Na2S2O3)固体配制一定体积的cmol/L标准溶液;
Ⅱ.用水样瓶取河流中水样v1mL并立即依次序注入1.0mLMnCl2溶液和1.0mL碱性KI溶液,塞紧瓶塞(瓶内不准有气泡),反复震荡后静置约1小时;
Ⅲ.向水样瓶中加入1.0mL硫酸溶液,塞紧瓶塞,振荡水样瓶至沉淀全部溶解,此时溶液变为黄色; Ⅳ.将水样瓶内溶液全量倒入锥形瓶中,用硫代硫酸钠标准溶液滴定;
V.待试液呈淡黄色后,加1mL淀粉溶液,继续滴定到终点并记录消耗的硫代硫酸钠溶液体积为v2。
已知:I2 +2Na2S2O3 =2NaI+Na2S4O6
(1)在滴定环节中使用的仪器有滴定管夹、铁架台、烧杯、锥形瓶和________________________。
(2)在步骤Ⅱ中,水样中出现了MnMnO3沉淀,离子方程式为4Mn2++O2+8OH-![]() 2MnMnO3↓+4H2O。
2MnMnO3↓+4H2O。
(3)步骤Ⅲ中发生反应的离子方程式为 _______________________________________________________________。
(4)滴定时,溶液由__________色到______________色,且半分钟内颜色不再变化即达到滴定终点。
(5)河水中的溶解氧为_____________________________mg/L。
(6)当河水中含有较多NO3-时,测定结果会比实际值________(填偏高、偏低或不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下述转化关系,回答问题:

已知:①+CH3Br![]() CH3+HBr;
CH3+HBr;
②C物质苯环上一卤代物只有两种。
(1)写出B物质的名称__________;D物质的结构简式________。
(2)写出反应②的类型________;反应⑤的条件________。
(3)写出反应⑥的化学方程式:________________________________。
(4)写出D+E反应的化学方程式:_______________。
(5)反应②还有可能生成一种C16H18的有机物,其苯环上一卤代物也只有两种,写出它的结构简式:_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如下图所示:下列叙述正确的是
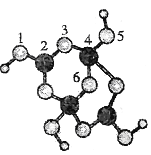
A.Xm-的化学式为B4O8H42-
B.硼原子轨道的杂化类型有sp2、 sp3
C.配位键存在于4、6原子之间
D.硼砂晶体中有离子键、配位键两种化学键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
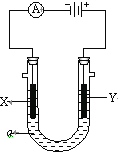
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①Y电极上的电极反应式为___;在X极附近观察到的实验现象是___;
②电解总反应的离子方程式:____。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是___;电极反应式是___。
②Y电极的材料是___;电极反应式是___。
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com