
ЎҫМвДҝЎҝК®ҫЕҙуұЁёжМбіцТӘ¶Ф»·ҫіОКМвҪшРРИ«ГжЎўПөНіөДҝЙіЦРшЦОАнЎЈВМЙ«ДЬФҙКЗКөК©ҝЙіЦРш·ўХ№өДЦШТӘНҫҫ¶Ј¬АыУГЙъОпТТҙјАҙЦЖИЎВМЙ«ДЬФҙЗвЖшөДІҝ·Ц·ҙУҰ№эіМИзПВНјЛщКҫЈә

(1)ТСЦӘЈәCO(g) +H2O(g)CO2(g)+H2(g) H1=-41 kJЎӨmol-1
CH3CH2OH(g)+3H2O(g)2CO2(g)+6H2(g) H2 =+174.1 kJЎӨmol-1
·ҙУҰIөДИИ»ҜС§·ҪіМКҪОӘ______ЎЈ
(2)·ҙУҰIIФЪҪшЖшұИ[n(CO) : n(H2O)]І»Н¬КұЈ¬ІвөГПаУҰөД CO ЖҪәвЧӘ»ҜВКјыПВНј(ёчөг¶ФУҰөД·ҙУҰОВ¶ИҝЙДЬПаН¬Ј¬ТІҝЙДЬІ»Н¬Ј»ёчөг¶ФУҰөДЖдЛы·ҙУҰМхјю¶јПаН¬)ЎЈ

ўЩНјЦРAЎўEәН GИэөг¶ФУҰөД·ҙУҰОВ¶ИTAЎўTEЎўTGөД№ШПөКЗ_____Ј¬ЖдФӯТтКЗ ______ЎЈёГОВ¶ИПВЈ¬ТӘМбёЯCOЖҪәвЧӘ»ҜВКЈ¬іэБЛёДұдҪшЖшұИЦ®НвЈ¬»№ҝЙІЙИЎөДҙлК©КЗ______ЎЈ
ўЪУЙНјЦРҝЙЦӘCOөДЖҪәвЧӘ»ҜВКУлҪшЖшұИЎў·ҙУҰОВ¶ИЦ®јдөД№ШПөКЗ____ЎЈ
ўЫAЎўB БҪөг¶ФУҰөД·ҙУҰЛЩВКҙуРЎЈәvA_____vB(МоЎ°<Ўұ Ў°=Ўұ»тЎ°>Ўұ)ЎЈТСЦӘ·ҙУҰЛЩВК v=vХэvДж= kХэx(CO)x(H2O) kДжx(CO2) x(H2) Ј¬kОӘ·ҙУҰЛЩВКіЈКэЈ¬xОӘОпЦКөДБҝ·ЦКэЈ¬ФЪҙпөҪЖҪәвЧҙМ¬ОӘDөгөД·ҙУҰ№эіМЦРЈ¬өұCOөДЧӘ»ҜВКёХәГҙпөҪ20ЈҘКұЈ¬![]() =_____ЎЈ
=_____ЎЈ
(3)·ҙУҰIIIФЪұҘәНKHCO3өзҪвТәЦРЈ¬өзҪв»о»ҜөДCO2АҙЦЖұёТТҙјЈ¬ЖдФӯАнИзНјЛщКҫЈ¬ФтТхј«өДөзј«·ҙУҰКҪОӘ___________ЎЈ
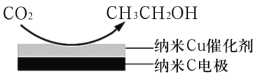
Ўҫҙр°ёЎҝCH3CH2OH(g)+H2O(g)4H2(g)+2CO(g) H= +256.1 kJЎӨmol-1 TA=TE=TG KA=KE=KG=1 ј°КұТЖИҘІъОп ОВ¶ИПаН¬Ј¬ҪшЖшұИФҪҙуЈ¬COөДЖҪәвЧӘ»ҜВКФҪРЎЈ»ҪшЖшұИПаН¬Ј¬·ҙУҰОВ¶ИФҪёЯЈ¬COөДЖҪәвЧӘ»ҜВКФҪРЎ Јј 36.0 14CO2+12e+9H2OЁTCH3CH2OH+12HCO3
ЎҫҪвОцЎҝ
(1)·ҙУҰI»ҜС§·ҪіМКҪОӘCH3CH2OH(g)+H2O(g)ЁT4H2(g)+2CO(g)Ј¬
ўЩCO(g)+H2O(g)CO2(g)+H2(g)ЎчH1=-41kJ/mol
ўЪCH3CH2OH(g)+3H2O(g)2CO2(g)+6H2(g)ЎчH2=+174.1kJ/mol
ёщҫЭёЗЛ№¶ЁВЙўЪ-ўЩЎБ2јЖЛгCH3CH2OH(g)+H2O(g)ЁT4H2(g)+2CO(g)өДЎчHЈ»
(2)ўЩ·ҙУҰIIОӘCO(g)+H2O(g)CO2(g)+H2(g)ЎчH1=-41kJ/molЈ¬Хэ·ҙУҰ·ЕИИЈ¬ҝЙУГAЎўEәНGИэөг¶ФУҰКэЦөҪбәП·ҙУҰИэ¶ОКҪјЖЛгЖҪәвіЈКэЈ¬ёщҫЭЖҪәвіЈКэөДұд»Ҝ·ЦОцЕР¶ПЈ»ёщҫЭ·ҙУҰМШөгЈ¬ҪбәПОВ¶ИЎўЕЁ¶И¶ФЖҪәвТЖ¶ҜөДУ°Пм·ЦОцМбёЯCOЖҪәвЧӘ»ҜВКөДҙлК©Ј»
ўЪУЙНјҝЙЦӘЈ¬өұCOөДЧӘ»ҜВКПаН¬КұЈ¬ОВ¶ИУЙөНөҪёЯ¶ФУҰөДҪшЖшұИОӘ0.5Ўў1Ўў1.5Ј¬УЙҙЛҝЙИ·¶ЁОВ¶ИУлҪшЖшұИөД№ШПөЈ»
ўЫCO(g)+H2O(g)CO2(g)+H2(g)ЎчH1=-41kJ/molЈ¬·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬ЙэОВЖҪәвДжПтҪшРРЈ¬COЧӘ»ҜВКјхРЎЈ»ҙпөҪЖҪәвЧҙМ¬ОӘDөгөД·ҙУҰ№эіМЦРЈ¬ЖҪәвіЈКэK=![]() Ј¬Фт
Ј¬Фт![]() =
=![]() =KЎБ
=KЎБ![]() Ј¬ёщҫЭ·ҙУҰИэ¶ОКҪјЖЛгDөгКұЖҪәвіЈКэKЎўјЖЛгCOЧӘ»ҜВКёХәГҙпөҪ20%КұёчОпЦКөДОпЦКөДБҝ·ЦКэxЈ¬ҙъИл
Ј¬ёщҫЭ·ҙУҰИэ¶ОКҪјЖЛгDөгКұЖҪәвіЈКэKЎўјЖЛгCOЧӘ»ҜВКёХәГҙпөҪ20%КұёчОпЦКөДОпЦКөДБҝ·ЦКэxЈ¬ҙъИл![]() =KЎБ
=KЎБ![]() ЦРјЖЛгұИЦөЈ»
ЦРјЖЛгұИЦөЈ»
(3)Тхј«өГөзЧУ·ўЙъ»№Фӯ·ҙУҰЈ¬ҪбәПөзЧУКШәгЎўөзәЙКШәгКйРҙөзј«·ҙУҰ·ҪіМКҪЎЈ
(1)·ҙУҰI»ҜС§·ҪіМКҪОӘCH3CH2OH(g)+H2O(g)ЁT4H2(g)+2CO(g)Ј¬ўЩCO(g)+H2O(g)CO2(g)+H2(g)ЎчH1=41kJ/mol
ўЪCH3CH2OH(g)+3H2O(g)2CO2(g)+6H2(g)ЎчH2=+174.1kJ/mol
ёщҫЭёЗЛ№¶ЁВЙўЪўЩЎБ2јЖЛгCH3CH2OH(g)+H2O(g)ЁT4H2(g)+2CO(g)өДЎчH=+174.1kJ/mol(41kJ/mol)ЎБ2=+256.1kJ/molЈ¬јҙИИ»ҜС§·ҪіМКҪОӘCH3CH2OH(g)+H2O(g)ЁT4H2(g)+2CO(g)ЎчH=+256.1kJ/molЈ»
(2)ўЩНјЦРAөгКэЦөОӘ(0.5Ј¬66.7)Ј¬јҙ![]() =0.5Ј¬COөДЧӘ»ҜВКОӘ66.7%=
=0.5Ј¬COөДЧӘ»ҜВКОӘ66.7%=![]() Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә
Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә
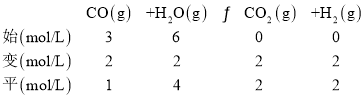
KA=![]() =
=![]() =1Ј»
=1Ј»
НјЦРEөгКэЦөОӘ(1Ј¬50)Ј¬јҙ![]() =1Ј¬COөДЧӘ»ҜВКОӘ50%Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә
=1Ј¬COөДЧӘ»ҜВКОӘ50%Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә

ЖҪәвіЈКэKE=![]() =
=![]() =1Ј»
=1Ј»
НјЦРGөгКэЦөОӘ(1.5Ј¬40)Ј¬јҙ![]() =1.5Ј¬COөДЧӘ»ҜВКОӘ40%Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә
=1.5Ј¬COөДЧӘ»ҜВКОӘ40%Ј¬ёщҫЭ№ШПөБРИэ¶ОКҪЈә
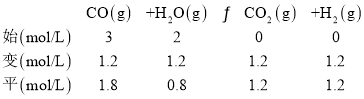
ЖҪәвіЈКэKG =![]() =
=![]() =1Ј»
=1Ј»
ёщҫЭТФЙПјЖЛгҝЙЦӘЈ¬KA=KE=KG=1Ј¬ЖҪәвіЈКэІ»ұдЈ¬ЖҪәвіЈКэКЗОВ¶ИөДәҜКэЈ¬ОВ¶ИІ»ұдЈ¬ФтЖҪәвіЈКэІ»ұдЈ¬ФтҝЙөГTA=TE=TGЈ»
CO(g)+H2O(g)CO2(g)+H2(g)ЎчH=41kJmol1Ј¬јҙХэПтОӘЖшМеМе»эІ»ұдөД·ЕИИ·ҙУҰЈ¬ЛщТФәгОВМхјюПВЈ¬ФцҙуH2O(g)өДЕЁ¶И»тј°Кұ·ЦАліцCO2өИІъОпҫщҝЙМбёЯCOөДЖҪәвЧӘ»ҜВКЈ»
ўЪУЙНјҝЙЦӘЈ¬ОВ¶ИПаН¬Ј¬ҪшЖшұИФҪҙуЈ¬COөДЖҪәвЧӘ»ҜВКФҪРЎЈ»ҪшЖшұИПаН¬Ј¬·ҙУҰОВ¶ИФҪёЯЈ¬COөДЖҪәвЧӘ»ҜВКФҪРЎЈ»
ўЫCO(g)+H2O(g)CO2(g)+H2(g)ЎчH1=41kJ/molЈ¬·ҙУҰОӘ·ЕИИ·ҙУҰЈ¬ЙэОВЖҪәвДжПтҪшРРЈ¬COЧӘ»ҜВКјхРЎЈ¬ФтBөгОВ¶ИёЯЈ¬·ҙУҰЛЩВКҝмЈ¬јҙvAЈјvBЈ»DөгКэЦөОӘ(1Ј¬60)Ј¬·ҙУҰИэ¶ОКҪОӘЈә

DөгОВ¶ИПВөДЖҪәвіЈКэKDЈҪ![]() =
=![]() =2.25Ј¬·ҙУҰҙпөҪЖҪәвКұvХэ=vДжЈ¬јҙkХэxЈЁCOЈ©xЈЁH2OЈ©=kДжxЈЁCO2Ј©xЈЁH2Ј©Ј¬ЛщТФ
=2.25Ј¬·ҙУҰҙпөҪЖҪәвКұvХэ=vДжЈ¬јҙkХэxЈЁCOЈ©xЈЁH2OЈ©=kДжxЈЁCO2Ј©xЈЁH2Ј©Ј¬ЛщТФ![]() =
=![]() =
=![]() =K=2.25Ј¬ФЪҙпөҪЖҪәвЧҙМ¬ОӘDөгөД·ҙУҰ№эіМЦРЈ¬өұCOЧӘ»ҜВКёХәГҙпөҪ20%КұЈ¬·ҙУҰИэ¶ОКҪОӘЈә
=K=2.25Ј¬ФЪҙпөҪЖҪәвЧҙМ¬ОӘDөгөД·ҙУҰ№эіМЦРЈ¬өұCOЧӘ»ҜВКёХәГҙпөҪ20%КұЈ¬·ҙУҰИэ¶ОКҪОӘЈә

XЈЁCOЈ©=xЈЁH2OЈ©=![]() =0.4Ј¬xЈЁCO2Ј©=xЈЁH2Ј©=
=0.4Ј¬xЈЁCO2Ј©=xЈЁH2Ј©=![]() =0.1Ј¬ЛщТФ
=0.1Ј¬ЛщТФ![]() =
=![]() =KЎБ
=KЎБ![]() =2.25ЎБ
=2.25ЎБ![]() =36.0Ј»
=36.0Ј»
(3)Тхј«өГөзЧУ·ўЙъ»№Фӯ·ҙУҰЈ¬№Көзј«·ҙУҰ·ҪіМКҪ14CO2+12e+9H2OЁTCH3CH2OH+12HCO3ЎЈ


 Т»ұҫәГМвҝЪЛгМвҝЁПөБРҙр°ё
Т»ұҫәГМвҝЪЛгМвҝЁПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҙјЛбКчЦ¬КЗТ»ЦЦіЙДӨРФәГөДКчЦ¬Ј¬ИзНјКЗТ»ЦЦҙјЛбКчЦ¬өДәПіЙПЯВ·Јә

ТСЦӘЈә![]()
![]()
![]() ·ҙУҰўЩөД»ҜС§·ҪіМКҪКЗ______Ј®
·ҙУҰўЩөД»ҜС§·ҪіМКҪКЗ______Ј®
![]() РҙіцBөДҪб№№јтКҪКЗ______Ј®
РҙіцBөДҪб№№јтКҪКЗ______Ј®
![]() ·ҙУҰўЩ~ўЫЦРКфУЪИЎҙъ·ҙУҰөДКЗ______
·ҙУҰўЩ~ўЫЦРКфУЪИЎҙъ·ҙУҰөДКЗ______![]() МоРтәЕ
МоРтәЕ![]() Ј®
Ј®
![]() ·ҙУҰўЬөД»ҜС§·ҪіМКҪОӘКЗ______Ј®
·ҙУҰўЬөД»ҜС§·ҪіМКҪОӘКЗ______Ј®
![]() ·ҙУҰўЭөД»ҜС§·ҪіМКҪКЗ______Ј®
·ҙУҰўЭөД»ҜС§·ҪіМКҪКЗ______Ј®
![]() ПВБРЛө·ЁХэИ·өДКЗ______
ПВБРЛө·ЁХэИ·өДКЗ______![]() МоЧЦДё
МоЧЦДё![]() Ј®
Ј®
a BҙжФЪЛі·ҙТм№№
b 1molEУлЧгБҝөДТш°ұИЬТә·ҙУҰДЬЙъіЙ2mol![]()
c FДЬУл![]() ·ҙУҰІъЙъ
·ҙУҰІъЙъ![]()
d¶ЎНйЎў![]() ұыҙјәНDЦР·РөгЧоёЯөДОӘ¶ЎНй
ұыҙјәНDЦР·РөгЧоёЯөДОӘ¶ЎНй
![]() Рҙіц·ыәППВБРМхјюөДУл
Рҙіц·ыәППВБРМхјюөДУл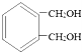 »ҘОӘН¬·ЦТм№№МеөДҪб№№јтКҪ______Ј®
»ҘОӘН¬·ЦТм№№МеөДҪб№№јтКҪ______Ј®
![]() ДЬУлЕЁдеЛ®·ҙУҰЙъіЙ°ЧЙ«іБөн
ДЬУлЕЁдеЛ®·ҙУҰЙъіЙ°ЧЙ«іБөн![]() ұҪ»·ЙПТ»ВИҙъОпУРБҪЦЦ
ұҪ»·ЙПТ»ВИҙъОпУРБҪЦЦ![]() ДЬ·ўЙъПыИҘ·ҙУҰЈ®
ДЬ·ўЙъПыИҘ·ҙУҰЈ®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДі»ҜС§КөСйРЎЧйҪ«Ч°УРНӯУлЕЁБтЛбЙХЖҝјУИИТ»¶ОКұјдәуЈ¬ИЎіцЙХЖҝЦР№ММеЈ¬МҪҫҝЖдіЙ·ЦЎЈІйЧКБПҝЙЦӘЈ¬ЕЁБтЛбУлНӯ·ҙУҰҝЙДЬЙъіЙCuS»тCu2SЈ¬ЛьГЗ¶јДСИЬУЪЛ®Ј¬ДЬИЬУЪПЎПхЛбЎЈКөСйИзПВЈә
ЈЁiЈ©УГХфБуЛ®ПҙөУ№ММеЈ¬өГөҪА¶Й«ИЬТәЈ¬№ММеіКәЪЙ«ЎЈ
ЈЁiiЈ©ИЎЙЩБҝәЪЙ«№ММеУЪКФ№ЬЦРЈ¬јУИлККБҝПЎПхЛбЈ¬әЪЙ«№ММеЦрҪҘИЬҪвЈ¬ИЬТәұдОӘА¶Й«Ј¬ІъЙъОЮЙ«ЖшЕЭЎЈИЎЙЩБҝЙПІгЗеТәУЪКФ№ЬЈ¬өОјУВИ»ҜұөИЬТәЈ¬ІъЙъ°ЧЙ«іБөнЎЈ
ўЩёщҫЭКөСйЈЁiЈ©өГөҪА¶Й«ИЬТәҝЙЦӘЈ¬№ММеЦРә¬____________ЈЁМо»ҜС§КҪЈ©
ўЪёщҫЭКөСйЈЁiiЈ©өДПЦПу_______ЈЁМоЎ°ДЬЎұ»тЎ°І»ДЬЎұЈ©И·¶ЁәЪЙ«№ММеКЗCuS»№КЗCu2SЈ¬АнУЙКЗ__________________________________________________________________________ЎЈ
РҙіцCu2SУлПЎПхЛб·ҙУҰөД»ҜС§·ҪіМКҪ____________________________________________
ўЫОӘБЛҪшТ»ІҪМҪҫҝәЪЙ«№ММеөДіЙ·ЦЈ¬Ҫ«КөСйЈЁiЈ©ЦРәЪЙ«№ММеПҙөУЎўәжёЙЈ¬ФЩіЖИЎ48.0gәЪЙ«№ММеҪшРРИзПВКөСйЈ¬НЁИлЧгБҝO2Ј¬К№УІЦКІЈБ§№ЬЦРәЪЙ«№ММеід·Ц·ҙУҰЈ¬№ЫІмөҪFЖҝЦРЖ·әмИЬТәНКЙ«ЎЈ

КөСйРтәЕ | ·ҙУҰЗ°әЪЙ«№ММеЦКБҝ/g | ід·Ц·ҙУҰәуәЪЙ«№ММеЦКБҝ/g |
I | 48.0 | 48.0 |
ўт | 48.0 | 44.0 |
ўу | 48.0 | 40.0 |
ёщҫЭЙПұнКөСйКэҫЭНЖІвЈәКөСйIЦРәЪЙ«№ММеөД»ҜС§КҪОӘ_____________________________Ј»КөСйўтЦРәЪЙ«№ММеөДіЙ·Цј°ЦКБҝОӘ_______________________________________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ№ӨТөЙПБӘәПЙъІъМјЛбЗвДЖәНВИҙъМюөД№ӨТХБчіМИзНјЛщКҫЈ¬ФЪЙъІъNaHCO3өД№эіМЦРНкіЙТТП©ВИ»ҜЈ¬ПВБРРрКцҙнОуөДКЗ
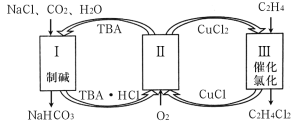
A.№эіМўсЦРөДTBAМжҙъБЛәоөВ°сЦЖјо·ЁЦРөД°ұЖш
B.ФЪ№эіМўтЦРКөПЦБЛTBAЎўCuCl2өДФЩЙъ
C.АнВЫЙПГҝЙъіЙ1mol NaHCO3Ј¬ҝЙөГөҪ1mol C2H4Cl2
D.№эіМўуЦРөД·ҙУҰКЗC2H4+2CuCl2![]() C2H4Cl2+2CuCl
C2H4Cl2+2CuCl
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіС§ЙъТФМъЛҝәНCl2ОӘФӯБПҪшРРПВБРИэёцКөСйЎЈҙУ·ЦАаҪЗ¶И·ЦОцЈ¬ПВБРЛө·ЁХэИ·өДКЗ (ЎЎЎЎ)
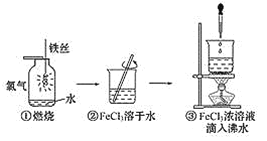
A.КөСйўЩЎўўЪЛщЙжј°өДОпЦКҫщОӘөзҪвЦК
B.КөСйўЩЎўўЫ·ўЙъөДҫщОӘАлЧУ·ҙУҰ
C.КөСйўЪЎўўЫҫщОҙ·ўЙъСх»Ҝ»№Фӯ·ҙУҰ
D.КөСйўЩЎўўЫ·ҙУҰЦЖөГөДОпЦКҫщОӘҙҝҫ»Оп
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОВКТЖшМеCO2ЧКФҙ»ҜАыУГөДТ»ЦЦНҫҫ¶ИзПВЈ¬ЙъіЙОпHәНIҝЙУГЧчп®АлЧУөзіШөДөзҪвЦКЎЈ

»ШҙрПВБРОКМвЈә
(1)УЙAөҪBөД·ҙУҰАаРНОӘ_____Ј»УЙCөҪDөД·ҙУҰЛщРиКФјБОӘ______ЎЈ
(2)EЦР№ЩДЬНЕөДГыіЖКЗ_____Ј¬Чо¶а_______ёцФӯЧУ№ІПЯЎЈ
(3)FәПіЙGөД»ҜС§·ҪіМКҪОӘ_______ЎЈ
(4)УлG»ҘОӘН¬·ЦТм№№МеөДфИЛбАа·јПгЧе»ҜәПОпЦРЈ¬әЛҙЕ№ІХсЗвЖЧОӘЛДЧй·еЈ¬·еГж»эЦ®ұИОӘ6Јә2Јә1Јә1өДҪб№№јтКҪОӘ____ЎЈ
(5)ЙијЖУЙұыИІәНјЧИ©ОӘЖрКјФӯБПЦЖұё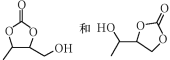 өДәПіЙВ·ПЯ(ОЮ»ъКФјБИОСЎ)______ЎЈ
өДәПіЙВ·ПЯ(ОЮ»ъКФјБИОСЎ)______ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝп®-НӯҝХЖшИјБПөзіШИЭБҝёЯЎўіЙұҫөНЈ¬ҫЯУР№гА«өД·ўХ№З°ҫ°ЎЈёГөзіШНЁ№эТ»ЦЦёҙФУөДНӯёҜКҙЎ°ПЦПуЎұІъЙъөзДЬЈ¬ЖдЦР·Еөз№эіМОӘ2Li+Cu2O+H2O=2Cu+2Li++2OH-Ј¬ПВБРЛө·ЁҙнОуөДКЗ( )
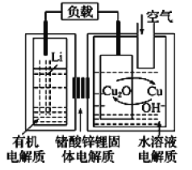
A.ёГөзіШөДёәј«ОӘLi
B.НЁҝХЖшКұЈ¬Нӯұ»ёҜКҙЈ¬ұнГжІъЙъCu2O
C.·ЕөзКұЈ¬Хэј«өДөзј«·ҙУҰКҪОӘO2+2H2O+4e-=4OH-
D.ИфУР1 mol Li+Нё№э№ММеөзҪвЦККұЈ¬ұкЧјЧҙҝцПВІОУл·ҙУҰөДO2Ме»эОӘ5.6 L
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТ»ЦЦәПіЙЗҝР§ҪөСӘЦ¬Т©ОпЈЁGЈ©өДЎ°Ж¬¶ОЎұИзПВЈә
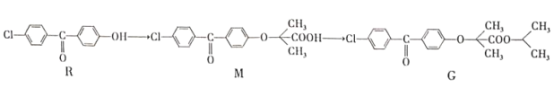
ПВБРЛө·ЁХэИ·өДКЗ
A.RЎўMЎўG¶јДЬ·ўЙъјУіЙЎўИЎҙъ·ҙУҰB.RЎўMЎўG¶јУР3ЦЦә¬Сх№ЩДЬНЕ
C.M·ЦЧУЦРЛщУРМјФӯЧУҝЙДЬ№ІЖҪГжD.G·ЦЧУЦРұҪ»·ЙП¶юдеҙъОпУР6ЦЦ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝәЈЛ®өДЧЫәПАыУГҝЙТФЦЖұёҪрКфГҫЈ¬ЖдБчіМИзНјЛщКҫЈә
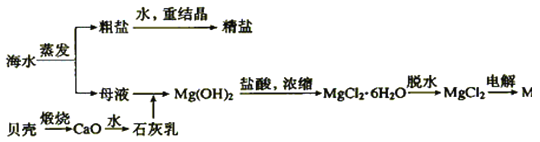
ЈЁ1Ј©РҙіцПВБР·ҙУҰөД»ҜС§·ҪіМКҪЎЈ
ўЩКҜ»ТИйУлДёТә·ҙУҰ___Ј»
ўЪMg(OH)2ЦРјУИлСОЛбөДАлЧУ·ҪіМКҪЈә__Ј»
ўЫMgCl2![]() MgЈә___ЎЈ
MgЈә___ЎЈ
ЈЁ2Ј©ФЪәЈЛ®МбИЎГҫөД№эіМЦРЈ¬Г»УРЙжј°өД»ҜС§·ҙУҰАаРН__
AЈ®·ЦҪв·ҙУҰ BЈ®»ҜәП·ҙУҰ CЈ®ёҙ·ЦҪв·ҙУҰ DЈ®ЦГ»»·ҙУҰ EЈ®Сх»Ҝ»№Фӯ·ҙУҰ
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com