
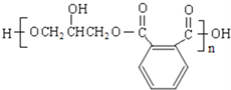
【题目】醇酸树脂是一种成膜性好的树脂,如图是一种醇酸树脂的合成线路:

已知:![]()
![]()
![]() 反应①的化学方程式是______.
反应①的化学方程式是______.
![]() 写出B的结构简式是______.
写出B的结构简式是______.
![]() 反应①~③中属于取代反应的是______
反应①~③中属于取代反应的是______![]() 填序号
填序号![]() .
.
![]() 反应④的化学方程式为是______.
反应④的化学方程式为是______.
![]() 反应⑤的化学方程式是______.
反应⑤的化学方程式是______.
![]() 下列说法正确的是______
下列说法正确的是______![]() 填字母
填字母![]() .
.
a B存在顺反异构
b 1molE与足量的银氨溶液反应能生成2mol![]()
c F能与![]() 反应产生
反应产生![]()
d丁烷、![]() 丙醇和D中沸点最高的为丁烷
丙醇和D中沸点最高的为丁烷
![]() 写出符合下列条件的与
写出符合下列条件的与 互为同分异构体的结构简式______.
互为同分异构体的结构简式______.
![]() 能与浓溴水反应生成白色沉淀
能与浓溴水反应生成白色沉淀![]() 苯环上一氯代物有两种
苯环上一氯代物有两种![]() 能发生消去反应.
能发生消去反应.
【答案】![]()
![]()
![]()
![]()
![]()
![]() +O2
+O2![]()
![]() +2H2O
+2H2O  c
c 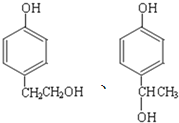
【解析】
由题中各物质的转化关系可知,![]() 在氢氧化钠乙醇溶液中发生消去反应生成A为
在氢氧化钠乙醇溶液中发生消去反应生成A为![]() ,
,![]() 在NBS作用之下生成B为
在NBS作用之下生成B为![]() ,
,![]() 与
与![]() 生成C为
生成C为![]() ,
,![]() 再碱性水解生成D为
再碱性水解生成D为![]() ,根据
,根据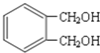
![]()
 ,结合反应条件可知,E为
,结合反应条件可知,E为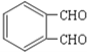 ,F为
,F为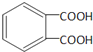 ,据此来解题即可。
,据此来解题即可。
![]() 反应①的化学方程式为
反应①的化学方程式为![]() ;
;
![]() 根据上面的分析可知,B的结构简式是
根据上面的分析可知,B的结构简式是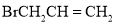 ;
;
![]() 根据上面的分析可知,反应①为消去反应,反应②为加成反应,反应③为取代反应
根据上面的分析可知,反应①为消去反应,反应②为加成反应,反应③为取代反应![]() 或水解反应
或水解反应![]() ,答案为③;
,答案为③;
![]() 反应④的化学方程式为
反应④的化学方程式为 ;
;
![]() 反应⑤的化学方程式是
反应⑤的化学方程式是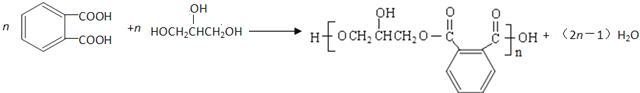 ;
;
![]() 为
为![]() ,在碳碳双键上的一个碳上有两个原子都是氢,所以不存在顺反异构,故a错误;
,在碳碳双键上的一个碳上有两个原子都是氢,所以不存在顺反异构,故a错误;
![]() 为
为 ,1mol E与足量的银氨溶液反应能生成4mol Ag,故b错误;
,1mol E与足量的银氨溶液反应能生成4mol Ag,故b错误;
![]() 中有羧基,能与
中有羧基,能与![]() 反应产生
反应产生![]() ,故c正确;
,故c正确;
![]() 丁烷、
丁烷、![]() 丙醇和
丙醇和![]() 中沸点最高的为
中沸点最高的为![]() ,故d错误;
,故d错误;
答案选c;
![]() 符合下列条件
符合下列条件![]() 能与浓溴水反应生成白色沉淀,说明有酚的结构,
能与浓溴水反应生成白色沉淀,说明有酚的结构,![]() 苯环上一氯代物有两种,
苯环上一氯代物有两种,![]() 能发生消去反应,与
能发生消去反应,与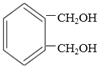 互为同分异构体,这样的结构有
互为同分异构体,这样的结构有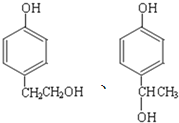 ,共2种。
,共2种。


科目:高中化学 来源: 题型:
【题目】已知![]() 摩尔盐
摩尔盐![]() 在
在![]() 时分解生成
时分解生成![]() 、
、![]() 和
和![]() 等。某小组称取mg样品进行如下实验
等。某小组称取mg样品进行如下实验![]() 尾气处理装置省略
尾气处理装置省略![]() ,验证它的分解产物。
,验证它的分解产物。
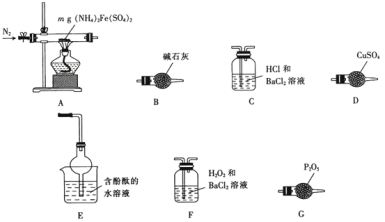
下列说法正确的是![]()
![]()
A.C中盐酸的作用是增强酸性,可以用硝酸替代盐酸
B.装置按![]() 连接可以检验
连接可以检验![]() 、
、![]() 、
、![]()
C.若实验中C、F都产生白色沉淀,则发生的反应不同,沉淀成分相同
D.实验完毕后,称量A中硬质玻璃管总质量,可以确定![]() 中x、y的值
中x、y的值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酯纤维的结构为:![]() ,以下是聚酯纤维的合成流程图:
,以下是聚酯纤维的合成流程图:


(1)写出产物C的结构简式:______________________。
(2)写出①和②的反应条件及试剂:
____________________;____________________。
(3)反应类型为X的反应方程式______________________,反应类型Y是___________。
(4)写出D、E生成聚酯纤维的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:四甲基氢氧化铵[(CH3)4NOH ]是强碱,甲胺 (CH3NH2H2O)为弱碱。常温下,在体积均为20 mL、浓度均为0.1 mol/L的四甲基氢氧化铵溶液和甲胺溶液中,分别滴加浓度为0.1 mol/L的盐酸,溶液的导电率与盐酸体积的关系如图所示。下列说法正确的是

A. pH的相对大小: c>d
B. 在b、c、e三点中,水的电离程度最大的点是e
C. b 点溶液:c(H+)+c(CH3NH3+) = c(OH-)
D. c 点溶液:c(Cl-)>c(CH3NH3+) >c(H+) >c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4molA 气体和 2molB 气体在 2L 的容器中混合,在一定条件下发生如下反应:2A(g) +B(g) 2C(g),若经 2s 后达到平衡,测得 C 的浓度为 0.6mol·L-1,现有下列几种说法:①用物质 A 的浓度变化表示的反应速率为 0.3mol·L -1·s -1,②用物质 B 的浓度变化表示的反应速率为0.6 mol·L-1·s -1,③平衡时物质A 的转化率为70%,④平衡时物质B 的浓度为0.7mol·L-1,其中正确的是( )
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸生产中,500℃时,NH3和O2可能发生如下反应:
① 4NH3 (g) + 5O2 (g) ![]() 4NO (g) + 6H2O (g);△H = -907.2kJ·mol-1 K=1.1×1026
4NO (g) + 6H2O (g);△H = -907.2kJ·mol-1 K=1.1×1026
② 4NH3 (g) + 4O2 (g) ![]() 2N2O (g) + 6H2O (g);△H= -1104.9kJ·mol-1 K=4.4×1028
2N2O (g) + 6H2O (g);△H= -1104.9kJ·mol-1 K=4.4×1028
③ 4NH3 (g) + 3O2 (g) ![]() 2N2 (g) + 6H2O (g);△H= -1269.2kJ·mol-1 K=7.1×1034
2N2 (g) + 6H2O (g);△H= -1269.2kJ·mol-1 K=7.1×1034
下列说法正确的是
A.增大压强,则反应的②K不变,反应①和③的K减小
B.500℃时,2NH3 (g) + 2O2 (g) ![]() N2O (g) + 3H2O (g) K=2.2×1028
N2O (g) + 3H2O (g) K=2.2×1028
C.500℃时,N2 (g) + O2 (g)= 2NO (g) △H = +181 kJ·mol-1
D.500℃时,2 mol NH3 与2.5 mol O2混合发生反应①,可放出热量453.6 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述不正确的是 ( )
A. 2.0 g D2O中含有的质子数、电子数均为NA
B. 室温下,7 g乙烯和丁烯的混合气体中所含的氢原子数目是NA
C. 室温下,2 L 0.05 mol·L-1 NH4NO3溶液中所含的氮原子数目是0.2NA
D. 256 g S8(分子结构如图 )含S—S键数目为7NA
)含S—S键数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+CO2(g)![]() 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
A.升高温度和增大压强B.降低温度和减小压强
C.降低温度和增大压强D.升高温度和减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二钴(Co2O3)常用于制滤光眼镜的添加剂、催化剂和强氧化剂。以含钴废料(主要成分CoO、Co2O3,含有少量MnO2、NiO、Fe3O4)为原料制备Co2O3的流程如下:

(1)研磨的目的是____________。滤渣1的主要成分为______________(填化学式)。
(2)酸浸时双氧水的作用有___________。不能用盐酸代替硫酸的原因是_________________。
(3)在实验室里,萃取操作要用到的玻璃仪器主要有___________。
(4)沉钴时发生反应的离子方程式为_______。煅烧时发生反应的化学方程式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com