
【题目】将 4molA 气体和 2molB 气体在 2L 的容器中混合,在一定条件下发生如下反应:2A(g) +B(g) 2C(g),若经 2s 后达到平衡,测得 C 的浓度为 0.6mol·L-1,现有下列几种说法:①用物质 A 的浓度变化表示的反应速率为 0.3mol·L -1·s -1,②用物质 B 的浓度变化表示的反应速率为0.6 mol·L-1·s -1,③平衡时物质A 的转化率为70%,④平衡时物质B 的浓度为0.7mol·L-1,其中正确的是( )
A.①③B.①④C.②③D.③④
科目:高中化学 来源: 题型:
【题目】I.实验室用如图所示的装置制取乙酸乙酯。
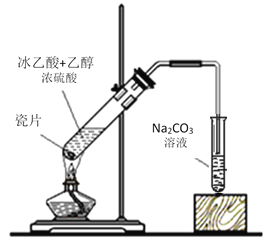
(1)浓硫酸的作用是:① _______________;② ______________。
(2)右边装置中通蒸气的导管要插在液面上而不能插入溶液中,目的是防止溶液的倒吸。造成倒吸的原因是____________。
(3)分离得到乙酸乙酯的方法是________________,分离需要的玻璃仪器是___________。
(4)若加的是C2H518OH写出制乙酸乙酯的方程式___________。
II.某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现红色和黑色交替的现象,请写出乙醇催化氧化的化学方程式____________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_______反应。
(2)甲和乙两个水浴作用不相同。甲的作用是_________;乙的作用是___________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是__________。集气瓶中收集到的气体的主要成分是____________。
(4)图中丙处导管应倾斜的原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是

A. BOH属于弱碱
B. BOH的电离常数K=1×10-4.8
C. P点所示的溶液中:c(Cl-)>c(B+)
D. N点所示的溶液中:c(H+)=c(Cl-)+c(OH-)-c(BOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中不符合此条件的是 ( )
A.CH4 C2H4B.CH4 C3H4C.C2H4 C3H4D.C2H2 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
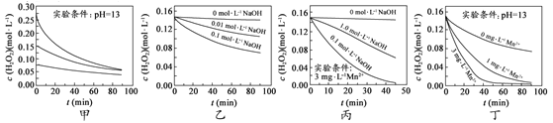
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇酸树脂是一种成膜性好的树脂,如图是一种醇酸树脂的合成线路:

已知:![]()
![]()
![]() 反应①的化学方程式是______.
反应①的化学方程式是______.
![]() 写出B的结构简式是______.
写出B的结构简式是______.
![]() 反应①~③中属于取代反应的是______
反应①~③中属于取代反应的是______![]() 填序号
填序号![]() .
.
![]() 反应④的化学方程式为是______.
反应④的化学方程式为是______.
![]() 反应⑤的化学方程式是______.
反应⑤的化学方程式是______.
![]() 下列说法正确的是______
下列说法正确的是______![]() 填字母
填字母![]() .
.
a B存在顺反异构
b 1molE与足量的银氨溶液反应能生成2mol![]()
c F能与![]() 反应产生
反应产生![]()
d丁烷、![]() 丙醇和D中沸点最高的为丁烷
丙醇和D中沸点最高的为丁烷
![]() 写出符合下列条件的与
写出符合下列条件的与 互为同分异构体的结构简式______.
互为同分异构体的结构简式______.
![]() 能与浓溴水反应生成白色沉淀
能与浓溴水反应生成白色沉淀![]() 苯环上一氯代物有两种
苯环上一氯代物有两种![]() 能发生消去反应.
能发生消去反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是
A. 2L 0.5mol/L亚硫酸溶液中含有的H+离子数为2NA
B. 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C. 电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32g
D. 某密闭容器中盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目小于0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.78g Na2O2溶于水后所得溶液中含有O22-数目为2NA
B.将2.24 LCl2(标况)通入到足量的NaOH溶液中,转移的电子数目为0.1NA
C.0.1 mol/LNH4Cl溶液中含有的NH4+数目小于0.1NA
D.用铅蓄电池电解氯化钠溶液,得到1 molH2时,理论上铅蓄电池中消耗氢离子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.图1是实验室用乙醇和浓硫酸制乙烯的发生装置,图2是乙烯性质实验装置,请回答:
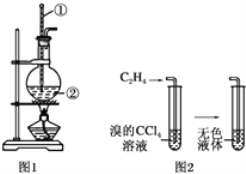
(1)图1中仪器①、②的名称分别为________、________。
(2)请写出实验室制乙烯的化学方程式:________。
(3)向溴的四氯化碳溶液中通入乙烯,溶液的颜色很快褪去,该反应属于________(填反应类型)。
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。请回答:

(1)图中①、②、③、④装置盛放的试剂是下列中的(请将下列有关试剂的序号填入对应装置内,可重复选用):①_____②_____③______④________
A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明二氧化硫气体存在的现象是_______。
(3)使用装置②的目的是________。
(4)使用装置③的目的是________。
(5)验证含有乙烯的现象是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com