
����Ŀ��ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ��Ϊ�ⶨ�����Ũ�ȣ���ʵ�����н�������ʵ�飬�����������գ�
��1�� ����100mL 0.10mol/L NaOH����Һ��
��2��ȡ20.00mL����ϡ������Һ������ƿ�У����μ�2~3�η�̪��ָʾ�������Լ����Ƶı�NaOH��Һ���еζ����ظ������ζ�����2~3�Σ���¼�������¡�
ʵ���� | NaOH��Һ��Ũ�� ��mol/L�� | �ζ����ʱ��NaOH��Һ����������mL�� | ����������Һ����� ��mL�� |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
�ٵζ��ﵽ�յ��������_______________________________________����ʱ��ƿ����Һ��pHΪ________��
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ____________________��������λ��Ч���֣�
��������ʵ���У����в���������������ȷ������ɲⶨ���ƫ�ߵ���_______��
A���ζ��յ����ʱ���Ӷ���
B����ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ô���������Һ��ϴ
C����ƿˮϴ��δ����
D������ǰNaOH�����л���Na2CO3����
E����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ
���𰸡� �����һ��NaOH��Һ����ʱ����Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ 8.2 0.11 molL��1 D E
��������������Ҫ�����к͵ζ�ʵ�顣
��1�� ����100mL 0.10mol/L NaOH����Һ��
��2���ٵζ��ﵽ�յ�������ǵ����һ��NaOH��Һ����ʱ����Һ����ɫ��Ϊ��ɫ���Ұ�����ڲ���ɫ����ʱ��ƿ����Һ��pHΪ8.2��
��ƽ����������������Һ22.71mL���ɼ�����������Ũ��ԼΪ![]() =0.11 molL��1��
=0.11 molL��1��
��A���ն�����С������������Һ�����ֵ��С���ⶨ���ƫ�ͣ�B�����ᱻϡ�ͣ���������������Һ������٣��ⶨ���ƫ�ͣ�C����Ӱ��ⶨ�����D������������Һ�к�������С����������������Һ������࣬�ⶨ���ƫ�ߣ�E������������Һ�����ֵ���ⶨ���ƫ�ߡ���ѡDE��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʣ�����Ȳ �ڱ�����Һ ����ȩ �ܵ�����Һ �ݰ����ᣮ��ش�
��1������ˮ����ɫ����������ţ���ͬ����
��2���ܷ������ķ�Ӧ���� ��
��3���ܸ��巢���ӳɷ�Ӧ���� ��
��4���ܸ�������Һ����������Ӧ���� ��
��5���ܸ�������ˮ��Ӧ���ɰ�ɫ�������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����Ȼ�ѧ����ʽ�У���ѧ��Ӧ�Ħ�Hǰ��С�ں��ߵ���
��C(s)+ ![]() O2(g) ===CO(g)����H1 C(s)+O2(g) ===CO2(g)����H2
O2(g) ===CO(g)����H1 C(s)+O2(g) ===CO2(g)����H2
��S(g)+O2(g) ===SO2(g)����H3 S(s)+O2(g) ===SO2(g)����H4
��CaO(s)+H2O(l) ===Ca(OH)2(s)����H5 CaCO3(s) ===CaO(s)+CO2(g)����H6
A���� B���٢� C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����ͼ��ʾ��ת����ϵ����X��Y�����ǣ� ��
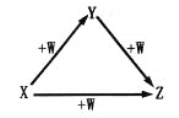
��C��CO ��AlCl3�� Al��OH��3 ��N2��NO ��S��SO2
A. �٢� B. �ڢ� C. �ۢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����к�NaCl��Na2SO4��NaNO3�Ļ���ѡ���ʵ����Լ���ȥ��Һ�е�NaCl��Na2SO4 �� �Ӷ��õ�������NaNO3��Һ����Ӧ��ʵ����̿�����ͼ��ʾ��
��1��д���������ʵĻ�ѧʽX��A��B
��2������ʵ�������м��������Na2CO3��Ŀ���� ��
��3������ʵ�鷽���õ�����Һ3�п϶��������ѧʽ�����ʣ�Ϊ�˽��������⣬��������Һ3�м�����������ѧʽ����֮����Ҫ��ù���NaNO3����е�ʵ�����������������ƣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ������������й�˵����ȷ���ǣ� ��
A.�ڳ��³�ѹ�£�11.2LN2���еķ�����Ϊ0.5NA
B.�ڳ��³�ѹ�£�1mol�������е�ԭ����Ϊ2NA
C.71gCl2����ԭ����Ϊ2NA
D.23g���ڻ�ѧ��Ӧ��ʧȥ������ĿΪ10NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں���Cu(NO3)2��Zn(NO3)2��Fe(NO3)3��AgNO3��0.01 mol�����Ի����Һ�м���0.01 mol���ۣ�����������ı仯Ӧ�� �� ��
A. ���ܽ⣬����0.01 mol Ag��0.005 mol Cu
B. ���ܽ⣬����0.01 mol Ag���ų�H2
C. ���ܽ⣬����0.01 mol Ag����Һ�в�����Fe3��
D. ���ܽ⣬����0.01 mol Ag����Һ�в�����Cu2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ƽ�ȩ(NaHSO2HCHO2H2O)�׳Ƶ��飬���ȶ���120��ʱ��ֽ⡣��ӡȾ��ҽҩ�Լ�ԭ���ܹ�ҵ���й㷺Ӧ�á���Na2SO3��SO2��HCHO��п��Ϊԭ���Ʊ����������Ƽ�ȩ��ʵ�鲽�����£�
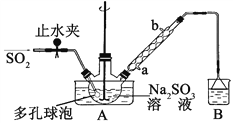
����1����������ƿ�м���һ����Na2SO3��ˮ�������ܽ⣬����ͨ��SO2������ҺpH ԼΪ4���Ƶ�NaHSO3��Һ��
����2����װ��A �е����ܻ�����Ƥ��������ƿ�м����Թ�����п�ۺ�һ������ȩ��Һ����80��90���£���ӦԼ3h����ȴ�����£����ˣ�
����3������Һ�������Ũ������ȴ�ᾧ��
��1��װ��B ���ձ���Ӧ�������Һ��____________������������ȴˮ��_____(����a������b��)�ڽ�ˮ��
��2��A�ж�����ݵ�������__________________________________________��
��3���������л�������Ҫ���ʳ�H2O ���________ (�ѧʽ)��
��4��д������2�з�����Ӧ�Ļ�ѧ����ʽ________________________________��
��5������3�����������������Ũ����ԭ����____________________________��
��6��Ϊ�˲ⶨ��Ʒ�Ĵ��ȣ�ȷ��ȡ2.0g��Ʒ����ȫ����ˮ���100mL��Һ��ȡ20.00mL������Һ�������������ȫ��Ӧ��(��֪I2����������ȩ�����ʲ���Ӧ)������BaCl2��Һ��������ȫ�����ˡ�ϴ�ӡ����������صõ���ɫ����0.466g�������ƵõIJ�Ʒ�Ĵ���Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ������仯����˵������ȷ���ǣ� ��
A.�����������ͻ����B.С�մ�����ʳƷ���ɼ�
C.���������к�θ�����D.������������Ϳ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com