
����Ŀ������ȼ��ʱ�������仯��ͼ���й�˵����ȷ���ǣ� ��

A.ͼ1�з�ӦΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=+890.3kJ/mol
B.ͼ2�з�ӦΪ��CH4(g)+![]() O2(g)=CO(g)+2H2O(g) H=��607.3kJ/mol
O2(g)=CO(g)+2H2O(g) H=��607.3kJ/mol
C.��ͼ�����Ƶã�CO(g)+![]() O2(g)=CO2(g) H=��283kJ/mol
O2(g)=CO2(g) H=��283kJ/mol
D.��ͼ������֪�������ʵ�����CO2��CO��CO2���е�������
���𰸡�C
��������
A������ͼ���������Ӧ�����������������������������ͼ1�з�ӦΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol��A����
B������ͼ�������������ˮ��״̬��Һ̬����ͼ2�з�ӦΪ��CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol��B����
O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol��B����
C��CO(g)+![]() O2(g)=CO2(g) ���ʱ�ɸ���CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol�ͷ�ӦH=��283kJ/mol��CH4(g)+
O2(g)=CO2(g) ���ʱ�ɸ���CH4(g)+2O2(g)=CO2(g)+2H2O(l) H=-890.3kJ/mol�ͷ�ӦH=��283kJ/mol��CH4(g)+![]() O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol����ʱ�H=��283kJ/mol��C��ȷ��
O2(g)=CO(g)+2H2O(l) H=��607.3kJ/mol����ʱ�H=��283kJ/mol��C��ȷ��
D��CO(g)+![]() O2(g)=CO2(g) H=��283kJ/mol���÷�Ӧ���ȣ���Ӧ�������������������������������Ե����ʵ�����CO2��CO��CO���е������ߣ�D����
O2(g)=CO2(g) H=��283kJ/mol���÷�Ӧ���ȣ���Ӧ�������������������������������Ե����ʵ�����CO2��CO��CO���е������ߣ�D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������������������������й�˵������ȷ����
A. ������������ȡ��ˮ����ͨ��ʹ��SO2����ԭ��
B. �����Ƽ���������������������ܽ�ȵIJ���
C. �ϳɰ����ø��¡���ѹ�ʹ�����Ҫ���������ƽ��ת����
D. ��ҵ����ϩֱ���������ƻ�������������ɫ��ѧ��ԭ�Ӿ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���ʵ����Ԫ�����ڱ��IJ��ֱ߽磬�����ϱ߽粢δ��ʵ�߱����
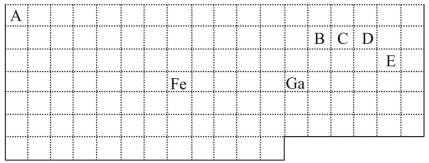
������Ϣ�ش��������⣺
��1�����ڱ��л�̬Gaԭ�ӵĵ����Ų�ʽΪ___��
��2��FeԪ��λ�����ڱ���___������Fe��CO���γ������Fe(CO)5����Fe(CO)5�����Ļ��ϼ�Ϊ___��
��3����֪��ԭ����Ŀ�͵�������(��۵�������)��ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������CO���ӻ�Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ___��___(�ѧʽ)����CO��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ�����___��
��4������VSEPR����Ԥ��ED4-���ӵĿռ乹��Ϊ___��B��C��D��Eԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ�����__(��д2�ֻ�ѧʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϵΪԪ�����ڱ��е���B�塢ԭ������Ϊ57~71��Ԫ�ء�
��1����(Dy)�Ļ�̬ԭ�ӵ����Ų�ʽΪ[Xe]4f106s2��������(Dy)ԭ����Χ�����Ų�ͼ��___________��
��2�����³��������籵ͭ�������к���Cu3+����̬ʱCu3+ �ĵ����Ų�ʽΪ________________��
��3���۲�����������ϵԪ�صĵ������������ж����п�����ʾ+3 �۵�Ԫ����___________(��Ԫ������)��������ϵԪ�صĵ�����(��λ��kJ mol-1)
Ԫ�� | I1 | I2 | I3 | I4 |
Yb(� | 604 | 1217 | 4494 | 5014 |
Lu(�壩 | 532 | 1390 | 4111 | 4987 |
La(�磩 | 538 | 1067 | 1850 | 5419 |
Ce(�棩 | 527 | 1047 | 1949 | 3547 |
��4��Ԫ����(Ce)�����γ������(NH4)2[Ce(NO3)6]��
���������������Ԫ�����縺���ɴ�С��˳��Ϊ________________(��Ԫ�ط��ű�ʾ)��
��д�����������̬�⻯��ˮ��Һ�д��ڵ������__________________(��дһ��)��
��Ԫ��Al Ҳ�����Ƴɼ��������̬�Ȼ������ӱ�ʾΪ(AlCl3)2��������Al ԭ���ӻ���ʽΪ_____________��������������ѧ��������______________(����ĸ)��
a.���Ӽ� b.���Լ� C.�Ǽ��Լ� d.��λ��
��5��PrO2(��������)�ľ���ṹ��CaF2��������������ԭ��λ�����ĺͶ�������PrO2(��������)�ľ�������________����ԭ������֪��������Ϊa pm���ܶ�Ϊ�� g�� cm-3��NA=_____________ (�ú�a�����Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������Ȳ���ṹ��ʽΪ![]() ��Ϊ��Ҫԭ�Ϻϳɾ�����ϩ���۱�ϩ����ȶ���ת����ϵͼ��
��Ϊ��Ҫԭ�Ϻϳɾ�����ϩ���۱�ϩ����ȶ���ת����ϵͼ��
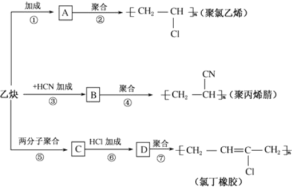
��1��д��A��B��C��D�������ʵĽṹ��ʽ��
A��________��B��________��C��________��D��________��
��2��д���йط�Ӧ�Ļ�ѧ����ʽ��
�ڣ�____________��
�ۣ�_____________��
�ݣ�___________��
�ߣ�_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ������������ӵ�ؿ�������λ��ѧ�ҡ�һ������ӵ�صķ�ӦʽΪLixC6+Li1��xCoO2![]() 6C+LiCoO2��x��1���乤��ԭ����ͼ��ʾ������˵������ȷ���ǣ� ��
6C+LiCoO2��x��1���乤��ԭ����ͼ��ʾ������˵������ȷ���ǣ� ��
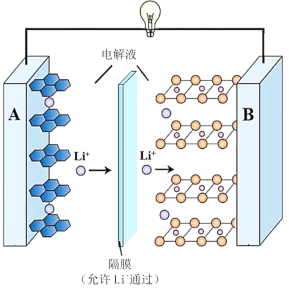
A.�ŵ�ʱA���缫ʽΪ��LixC6�Cxe-=6C+xLi+
B.�ŵ�ʱ����ת��0.3mol���ӣ�ʯī�缫������2.1g
C.���ʱ��A�������Դ������
D.�÷Ͼɵ�ؽ������ŵ紦�������������B������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȸʯ����Ҫ�ɷ�ΪCu2(OH)2CO3��ijͬѧ��ƵĴӿ�ȸʯ��ұ��ͭ�ķ�������(�����ȸʯ�����ʲ�����ˮ��ϡ����)��

(1)��Ӧ���ܹ۲쵽��������__________���йط�Ӧ�Ļ�ѧ����ʽΪ________��
(2)��Ӧ�ڼ���Ľ���������______���йط�Ӧ�����ӷ���ʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.0 L�����ܱ������з���0.10 mol X����һ���¶��·�����Ӧ��X(g)![]() Y(g)��Z(g) ��H��0��������������ѹǿp�淴Ӧʱ��t�ı仯��ϵ��ͼ��ʾ�����·�����ȷ���� ( )
Y(g)��Z(g) ��H��0��������������ѹǿp�淴Ӧʱ��t�ı仯��ϵ��ͼ��ʾ�����·�����ȷ���� ( )
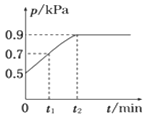
A. ���¶��´˷�Ӧ��ƽ�ⳣ��K��3.2
B. �ӷ�Ӧ��ʼ��t1ʱ��ƽ����Ӧ����v(X)��0.2/t1 mol��L��1��min��1
C. �����ƽ����ϵ��Y�İٷֺ������ɼ���һ������X
D. �����������䣬�ٳ���0.1 mol����X��ƽ�������ƶ���X��ת���ʼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ����С������ʵ���ʾ��ͼ��ͼ��ʾ��ͼ�С�������ʾ�������� M��һ�ִ�������������壬YΪ��һ�����壬E���к���ɫ���������ʵ����������ֻ��������������ѡȡ��Na2CO3��Na2O2��NaCl��Na2O��CaCl2��(NH4)2CO3����ʯ�ҵȹ��弰����ˮ���ݴ�ʵ�飬���������գ�
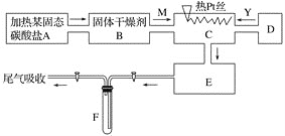
(1)A������װ�õ���Ҫ������ҩƷ��______________________��
(2)B����ѡ�ĸ������________����������______________________________��
(3)C�з�������Ҫ��Ӧ�Ļ�ѧ����ʽ��________________________________��
(4)��ȡY�����Dװ�����õ���Ҫ������__________________________��
��ȡY����Ļ�ѧ����ʽ��________________________��
(5)F�з�����Ӧ�Ļ�ѧ����ʽΪ__________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com