
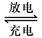 2PbSO4+2H2O回答下列 问题。(不考虑氢、氧的氧化还原)
2PbSO4+2H2O回答下列 问题。(不考虑氢、氧的氧化还原)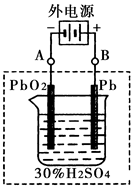
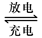 2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42- -2e- = PbSO4 ,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g;②该过程为放电的逆过程,所以在A电极上生成Pb,在B电极上生成PbO2;(2)阳极发生的是氧化反应,所以不能用铁作阳极材料,a错误;阳极反应方程式为:2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,故电解过程中阳极附近溶液的pH降低,所以b错误,c正确,1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子,故d正确,本题答案选择cd。
2PbSO4+2H2O,该反应中Pb作为负极,所以负极的电极反应式是Pb+SO42- -2e- = PbSO4 ,反应过程中消耗了硫酸,所以电解液中H2SO4的浓度将变小;该反应转移的电子数为2,所以当外电路通过2mol电子时,即有1mol的Pb发生反应,所以在负极增加一摩尔硫酸根的质量,即负极板的质量增加96g;②该过程为放电的逆过程,所以在A电极上生成Pb,在B电极上生成PbO2;(2)阳极发生的是氧化反应,所以不能用铁作阳极材料,a错误;阳极反应方程式为:2Cl--2e-=Cl2↑,Cl2在弱碱性条件下生成ClO-,故电解过程中阳极附近溶液的pH降低,所以b错误,c正确,1 mol二价镍全部转化为三价镍时,外电路中通过了1mol电子,故d正确,本题答案选择cd。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
 Li1-xCoO2+LixC6。下列有关说法正确的是
Li1-xCoO2+LixC6。下列有关说法正确的是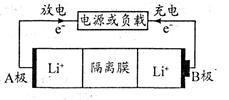
| A.放电时,负极反应LiCoO2 – xe- =Li(1-x)CoO2 + xLi+ |
| B.充电时,A极发生氧化反应 |
| C.充电时,Li+穿过隔离膜向B极移动 |
| D.当B极失去Xmol电子,电池消耗 6 mol C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
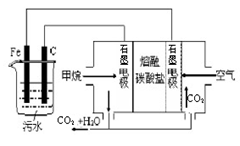
| A.铁电极为阳极,反应式为:Fe-3e-= Fe3+ |
| B.通入甲烷的石墨电极作负极,反应式为:CH4+8OH--8e-=CO2+6H2O |
| C.为增强污水的导电能力,可向污水中加入适量乙醇 |
| D.若阴极产生了44.8L气体,则理论上消耗同条件下的甲烷为11.2L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
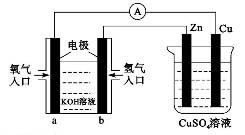
| A.该装置中Cu极为正极 |
| B.当铜极的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L |
C.b极反应的电极反应式为:H2一2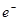 = 2H+ = 2H+ |
| D.一段时间后锌片质量减少 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
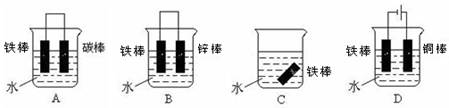
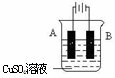
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
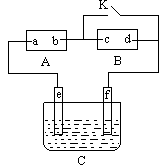
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
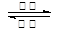 2PbSO4+2H2O)( )
2PbSO4+2H2O)( ) | A.铅蓄电池是生活里最常用的可充电电池,在充电时,电池的正极应接直流电源的正极 |
| B.铅蓄电池在放电时,电解液的酸性减弱 |
| C.铅蓄电池在放电时,PbO2作为负极,不断转化为PbSO4 |
| D.铅蓄电池在充电时,PbO2是氧化产物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com