
(10分)下图是工业生产硝酸铵的流程。
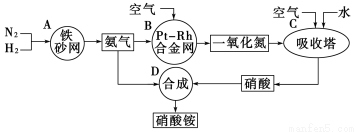
(1)吸收塔C中通入空气的目的是__________________ 。A、B、C、D四个容器中的反应,属于氧化还原反应的是________(填字母)。
(2)已知:4NH3(g)+3O2(g)===2N2(g) +6H2O(g) ΔH=-1266.8 kJ/mol
N2(g)+O2(g)===2NO(g) ΔH=+180.5 kJ/mol
写出氨高温催化氧化的热化学方程式:____________________________。
(3)已知:N2(g) +3H2(g)  2NH3(g) ΔH=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有______________(填字母)。
2NH3(g) ΔH=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有______________(填字母)。
A.升高温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充氮气
(4)在一定温度和压强下,将H2和N2按3 : 1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,求此时H2的转化率?(要有完整的计算过程,结果保留三位有效数字)
(10分) (1)使NO全部转化成HNO3 (或提供O2氧化NO)(2分); ABC(2分)
(2)4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH=-905.8 kJ/mol(2分)
(3)CD (2分)
(4)(2分)【解析】
设开始时H2的物质的量为3 mol,平衡时变化量为x mol,得
3H2 (g)+N2(g)  2NH3(g)
2NH3(g)
起始量(mol) 3 1 0
变化量(mol) x 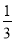 x
x  x
x
平衡量(mol) 3-x 1-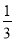 x
x  x
x
则平衡时混合气中NH3的气体体积分数= x÷
x÷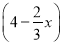 ×100%=17.6%
×100%=17.6%
解得x=0.9 mol
所以此时H2的转化率=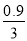 ×100%=30%
×100%=30%
【解析】
试题分析:(1)吸收塔中涉及的反应有:2NO+O2═2NO2;3NO2+H2O═2HNO3+NO;4NO2+O2+H2O═4HNO3;为使NO充分氧化而生成硝酸,应通入过量空气;题中涉及的化学反应有:
①N2+3H2?2NH3②4NH3+5O2 4NO+6H2O
③2NO+O2═2NO2④3NO2+H2O═2HNO3+NO⑤4NO2+O2+H2O═4HNO3
⑥NH3+HNO3═NH4NO3,其中①②③④⑤属于氧化还原反应,故答案为:使NO充分氧化(或者“提高NO的转化率”); A B C;
(2)已知:①4NH3(g)+3O2(g)═2N2(g)+6H2O(g),△H=-1266.8kJ/mol
②N2(g)+O2(g)═2NO(g),△H=+180.5kJ/mol,
利用盖斯定律①-2×②可得:4NH3(g)+5O2(g)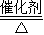 4NO(g)+6H2O(g),△H=-905.8KJ/mol;根据反应:
4NO(g)+6H2O(g),△H=-905.8KJ/mol;根据反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g),△H=-905.8KJ/mol; 转移的电子的物质的量
4NO(g)+6H2O(g),△H=-905.8KJ/mol; 转移的电子的物质的量
905.8KJ 20mol
Q 5mol
Q=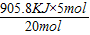 =226.45KJ,
=226.45KJ,
故答案为:4NH3(g)+5O2(g) 4NO(g)+6H2O(g),△H=-905.8KJ/mol; 226.45;
4NO(g)+6H2O(g),△H=-905.8KJ/mol; 226.45;
(3)为提高氢气的转化率,应是反应向正反应方向移动,本题中可采取的措施有:增大压强、循环利用和不断补充氮气、及时分离出氨气;故答案为:C D ; (4)设开始时H2的物质的量为3 mol,平衡时变化量为x mol,得
3H2 (g)+N2(g)  2NH3(g)
2NH3(g)
起始量(mol) 3 1 0
变化量(mol) x 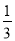 x
x 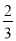 x
x
平衡量(mol) 3-x 1-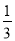 x
x 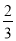 x
x
则平衡时混合气中NH3的气体体积分数=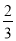 x÷
x÷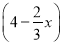 ×100%=17.6%
×100%=17.6%
解得x=0.9 mol
所以此时H2的转化率=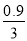 ×100%=30%
×100%=30%
考点: 氧化还原反应,热化学方程式,化学平衡的移动和物质的转化率计算。


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源:2014-2015学年吉林公主岭市高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.摩尔是七个基本物理量之一
B.阿伏伽德罗常数是没有单位的
C.氮气的摩尔质量是28g
D.1molH2O约含有6.02×1023个水分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:填空题
有一包白色粉末,含有Ba(NO3)2、CaCl2、K2CO3中的2种。为确定其成分,现做以下实验。结合资料卡片中的物质溶解性,试分析:
资料卡片:一些物质的溶解性
| OH- | CO | Cl- | NO |
Na+ | 溶 | 溶 | 溶 | 溶 |
Ca2+ | 微 | 不 | 溶 | 溶 |
Ba2+ | 溶 | 不 | 溶 | 溶 |
Mg2+ | 不 | 微 | 溶 | 溶 |
(1)将少量白色粉末加入足量水中,振荡,有白色沉淀生成。
通过上述现象可初步判断原白色粉末中一定含有的物质是 (填化学式)。
(2)过滤得到(1)中所产生的白色沉淀及滤液。
实验室中进行过滤操作时,通常需要下列玻璃仪器中的 (填序号)。
a. 玻璃棒 b. 普通漏斗 c. 烧杯 d. 容量瓶
(3)再继续向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成。
第(3)步实验及现象说明,原白色粉末中一定还含有的物质是 (填化学式),若将(2)中的白色沉淀溶于稀硝酸时,发生反应的化学方程式是
。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
能够鉴别溶液和胶体的方法是
A.过滤 B.观察颜色及状态 C.利用丁达尔效应 D.萃取
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高一上第一次质量检测化学试卷(解析版) 题型:选择题
摩尔是
A.物质的量的单位
B.物质的质量单位
C.物质的数量单位
D.既是物质的数量单位又是物质的质量单位
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
在密闭容器中发生如下反应:mA(g)+nB(g) pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是
pC(g)达到平衡后,保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍。下列说法中正确的是
A、m+n>p B、平衡向逆反应方向移动
C、A的转化率增大 D、C的体积分数增加
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高二上学期期中考试化学试卷(解析版) 题型:选择题
相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
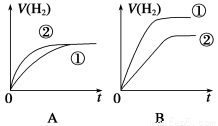
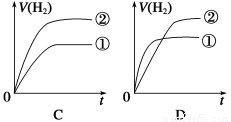
查看答案和解析>>
科目:高中化学 来源:2014-2015学年云南省玉溪市高一上学期期中化学试卷(解析版) 题型:实验题
(12分)现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL 0.2 mol·L-1的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④药匙 ⑤量筒 ⑥容量瓶 ⑦托盘天平。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。配制时还欠缺的仪器是 。
(2)经计算,需浓H2SO4的体积为 mL(精确到0.1)。
(3)配制过程有以下操作:
A.移液
B.量取
C.洗涤
D.定容
E.溶解
F.摇匀
其正确的操作顺序应是 (填序号)。
(4)在配制过程中,其他操作都准确,下列操作中,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②稀释后的H2SO4溶液未等冷却至室温就转移到容量瓶中
③定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
④转移前,容量瓶中含有少量蒸馏水
⑤定容时,俯视标线
(5)从上述容量瓶中移取25.00mL的稀硫酸溶液于100mL的容量瓶,加水稀释至刻度线。请问所得溶液中c(H+)= 。
(6)某研究小组欲利用氯气和二氧化硫通入水溶液中来制备100mL含0.4molH+的溶液,反应原理:Cl2+SO2+2H2O= H2SO4+2HCl,若忽略制备过程中气体的损耗,请问需标准状况下的氯气 L。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闵行区八校高二上学期期中联考化学试卷(解析版) 题型:选择题
要证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序为
①加入足量氯水 ②加入足量KMnO4溶液 ③加入少量KSCN溶液
A.③① B.③② C.①③ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com