
【题目】在密闭容器中充入1molH2和1molI2,压强为P(Pa),并在一定温度下反应:H2(g)+I2(g)![]() 2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”)
2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”)
(1)容积不变,加入1molH2,其正反应速率的变化是___。
(2)升高温度,其逆反应速率的变化是___。
(3)压强不变,加入1molHe,其正反应速率的变化是___。
科目:高中化学 来源: 题型:
【题目】硒(Se)是第四周期ⅥA族元素,是人体内不可或缺的微量元素,其氢化物H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的基础原料。
T℃时,向一恒容密闭容器中加入3molH2和lmolSe,发生反应H2(g)+Se(s)![]() H2Se(g)。
H2Se(g)。
①当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为液体H2Se,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3+、-CH3、CH3-都是重要的有机反应中间体,有关它们的说法不正确的是
A.它们均由甲烷去掉一个氢原子所得
B. CH3-与NH3、H3O+互为等电子体,几何构型均为三角锥形
C. CH3+中的碳原子采取sp2杂化,所有原子均共面
D.两个-CH3或一个CH3+和一个CH3-结合均可得到CH3CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活有密切联系,下列说法正确的是![]()
A.酸雨易导致土壤胶粒吸附![]() 使土壤酸化,影响铵态氮肥和钾肥的有效利用
使土壤酸化,影响铵态氮肥和钾肥的有效利用
B.汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的
C.高纯度的单晶硅用于制造登月车的光电池和光导纤维
D.铝及其合金是电气、工业、家庭广泛使用的材料,通常用电解氯化铝的方法制取铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:

(1)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中![]() 的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___。
的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___。
(2)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___、___;590℃之后,丁烯产率快速降低的主要原因可能是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应![]() ,为研究影响该反应速率的因素,在不同条件下进行4组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。下列说法不正确的是( )
,为研究影响该反应速率的因素,在不同条件下进行4组实验,Y、Z的起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。下列说法不正确的是( )

A.若实验②、④只改变一个条件,则由实验②、④得出结论:升高温度,化学反应速率加快
B.若实验①、②只改变一个条件,则由实验①、②得出结论:增大反应物浓度,化学反应速率加快
C.若实验②、③只改变一个条件,则实验③使用了催化剂
D.0~10min内,实验③的平均速率v(Y)=0.04 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香酯I的合成路线如下:
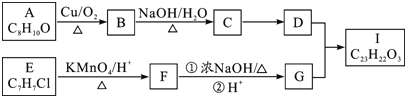
已知以下信息:
①A-I均为芳香族化合物,B能发生银镜反应,D的相对分子质量比C大4,E的苯环上的一溴代物有两种。
②![]()
③2RCH2CHO![]()
请回答下列问题:
(1)C→D的反应类型为___,E的名称为___。
(2)E→F与F→G的顺序能否颠倒___(填“能”或“否”),理由___。
(3)B与银氨溶液反应的化学方程式为___。
(4)I的结构简式为___。
(5)符合下列要求A的同分异构体还有___种。
①与Na反应并产生H2 ②芳香族化合物
其中核磁共振氢谱为4组峰,且面积比为6:2:1:1的是___(写出其中一种的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=___。已知:K300℃>K350℃,则该反应是___热反应。
(2)能使该反应的反应速率增大,且平衡向正反应方向移动的是___
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.16 g·Lˉ1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
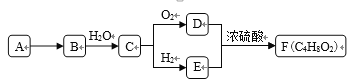
请回答:
(1)有机物D中含有的官能团名称是________。
(2)有机物A在高温下转化为B的化学方程式是_________________。
(3)下列说法正确的是________。
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
Ⅱ.已知:当一个碳原子上连有两个羟基时易发生下列转化:
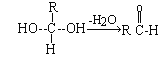
根据下图所示的反应路线及所给的信息填空。
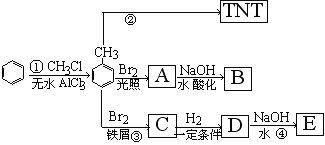
B遇石蕊试液变红,C的苯环上一元取代物只有2种同分异构体。
回答下列问题:
(1)A的结构简式为_____________,D的结构简式为_________________。
(2)③的反应类型为_________。
(3)反应②的化学方程式为____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com