
【题目】Ⅰ.A是天然气的主要成分,以A为原料在一定条件下可获得有机物B、C、D、E、F,其相互转化关系如图。已知烃B在标准状况下的密度为1.16 g·Lˉ1,C能发生银镜反应,F为有浓郁香味,不易溶于水的油状液体。
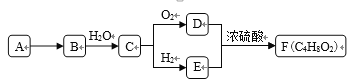
请回答:
(1)有机物D中含有的官能团名称是________。
(2)有机物A在高温下转化为B的化学方程式是_________________。
(3)下列说法正确的是________。
A.有机物E与金属钠反应比水与金属钠反应要剧烈
B.有机物D、E、F可用饱和Na2CO3溶液鉴别
C.实验室制备F时,浓硫酸主要起氧化作用
D.有机物C能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化
Ⅱ.已知:当一个碳原子上连有两个羟基时易发生下列转化:
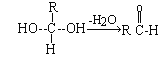
根据下图所示的反应路线及所给的信息填空。
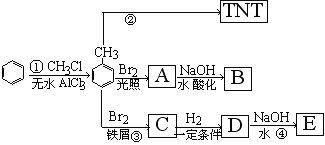
B遇石蕊试液变红,C的苯环上一元取代物只有2种同分异构体。
回答下列问题:
(1)A的结构简式为_____________,D的结构简式为_________________。
(2)③的反应类型为_________。
(3)反应②的化学方程式为____________________________。
【答案】羧基 ![]() BD
BD ![]()
![]() 取代反应
取代反应 
【解析】
Ⅰ.A是天然气的主要成分,则A为CH4;已知烃B在标准状况下的密度为1.16gL-1,则B的摩尔质量为:M(B)=22.4L/mol×1.16gL-1≈26g/mol;C能发生银镜反应,则C分子中含有醛基;F为有浓郁香味,不易溶于水的油状液体,则F为酯,根据转化关系可知F为CH3COOC2H5;C催化氧化得D,C与氢气发生还原反应生成E,则D为CH3COOH、E为CH3CH2OH、C为CH3CHO;B与水反应生成乙醛,且B的摩尔质量为26g/mol,则B为CH≡CH,据此进行解答;
Ⅱ.![]() 和CH3Cl在催化剂作用下发生取代反应生成
和CH3Cl在催化剂作用下发生取代反应生成![]() ;甲苯和浓硫酸、浓硝酸的混合液加热生成2,4,6-三硝基甲苯(
;甲苯和浓硫酸、浓硝酸的混合液加热生成2,4,6-三硝基甲苯(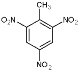 );甲苯与Br2在光照条件下发生取代反应生成A,A在NaOH水溶液中发生水解反应生成的B遇石蕊试液变红,可知B为
);甲苯与Br2在光照条件下发生取代反应生成A,A在NaOH水溶液中发生水解反应生成的B遇石蕊试液变红,可知B为![]() ,A为
,A为![]() ;
;![]() 和液溴在Fe粉作催化剂的作用下生成C,C的苯环上一元取代物只有2种同分异构体,则C为
和液溴在Fe粉作催化剂的作用下生成C,C的苯环上一元取代物只有2种同分异构体,则C为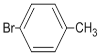 ,C再与H2发生加成反应生成
,C再与H2发生加成反应生成![]() ,
,![]() 再在NaOH溶液中发生水解反应生成的E为
再在NaOH溶液中发生水解反应生成的E为![]() ,据此分析解题。
,据此分析解题。
Ⅰ.(1)D的结构简式为D为CH3COOH,其含有官能团为羧基;
(2)A为CH4,B为CH≡CH,CH4在高温下转化为CH≡CH的化学方程式是![]() ;
;
(3)A.E为CH3CH2OH,乙醇与金属钠反应不如水与金属钠反应剧烈,故A错误;
B.D为CH3COOH、E为CH3CH2OH、F为CH3COOC2H5,乙酸与碳酸钠生成气体,乙酸乙酯不溶于饱和碳酸钠溶液,乙醇易溶于碳酸钠溶液,所以可用饱和Na2span>CO3溶液鉴别三者,故B正确;
C.实验室制备乙酸乙酯时,浓硫酸为催化剂和吸水剂,不体现氧化性,故C错误;
D.有机物C为CH3CHO,CH3CHO中含有官能团醛基,醛基能被新制碱性氢氧化铜悬浊液、酸性KMnO4溶液氧化,故D正确;
故答案为:BD;
Ⅱ.(1)由分析知:A的结构简式为![]() ,D的结构简式为
,D的结构简式为![]() ;
;
(2)反应③为![]() 和液溴在Fe粉作催化剂的作用下发生取代反应生成
和液溴在Fe粉作催化剂的作用下发生取代反应生成 ;
;
(3)反应②为甲苯和浓硫酸、浓硝酸的混合液加热生成TNT,反应的化学方程式为 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中充入1molH2和1molI2,压强为P(Pa),并在一定温度下反应:H2(g)+I2(g)![]() 2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”)
2HI(g)△H<0.写出下列条件下反应速率的变化(填“增大”,“减小”或“不变”)
(1)容积不变,加入1molH2,其正反应速率的变化是___。
(2)升高温度,其逆反应速率的变化是___。
(3)压强不变,加入1molHe,其正反应速率的变化是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氢气与氧气反应生成水蒸气的能量变化示意图。下列有关说法不正确的是( )

A.反应中断裂和形成的化学键均为共价键
B.该反应过程释放能量
C.断裂1mol液态水中的化学键需吸收930kJ能量
D.2mol O(g)形成1mol O2(g)释放498kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
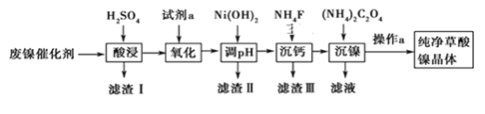
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(CaF2)=1.46×10-10;
③当某物质浓度小于1.0×10-5 mol·L-1时,视为完全沉淀。
请回答下列问题:
(1)在酸浸过程中会适当增大酸的浓度并不断快速搅拌,目的是______________。
(2)写出“沉镍”时发生反应的离子方程式:______________________________,当Ca2+沉淀完全时,溶液中 c(F-)> ________mol·L-1(写出计算式即可)。
(3)试剂a是一种绿色氧化剂,写出“氧化”时反应的化学反应方程式:_______________________________。
(4)操作a的内容包括过滤,洗涤,干燥。请用简洁语言描述洗涤的方法是__________________________。
(5)“调pH”时pH的调控范围为______≤PH<6.8。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能是下列的( )
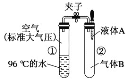
A.氢氧化钠溶液、二氧化碳B.水、氯化氢
C.氢氧化钠溶液、一氧化氮D.水、二氧化氮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲探究CO还原CuO,设计如图所示装置(夹持装置略去)。下列说法正确的是
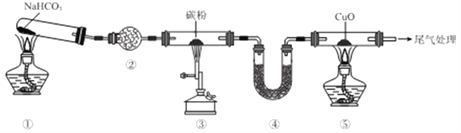
A. ②、④中均可盛装碱石灰
B. 加热的顺序为③、①、⑤
C. ①、③、⑤中均发生氧化还原反应
D. 可将尾气用导管通入到⑤的酒精灯处灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】探究Na2O2与水的反应,实验如图:(已知:H2O2 ![]() H+ + HO2-、HO2-
H+ + HO2-、HO2- ![]() H+ + O22-)下列分析不正确的是
H+ + O22-)下列分析不正确的是
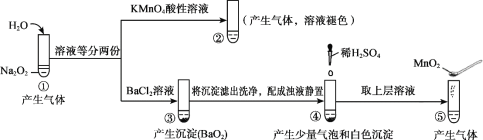
A. ①、⑤中产生的气体能使带火星的木条复燃
B. ①、④中均发生了氧化还原反应和复分解反应
C. ②、⑤中KMnO4与MnO2的作用不同,产生气体的量也不同
D. 通过③能比较酸性:HCl>H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近我国科学家在液流电池研究方面取得新进展。一种硫/碘体系(KI/K2S2)的液流电池工作原理如图所示。下列说法正确的是( )

A. 放电时电池右侧为负极,发生氧化反应
B. 放电时电池左侧的电极反应为S22-+2e-==2S2-
C. 充电时电解质溶液中K经交换膜向右侧移动
D. 充电时电池的总反应为3I-+S22-=I3-+2S2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等量的N2和H2的混合气体分别充入甲、乙、丙三个容器中,进行反应![]() ,经过相同的时间后,测得反应速率分别为甲:v(H2)=1 mol·L-1·min-1,乙:v(N2)=2 mol·L-1·min-1,丙:v(NH3)=3 mol·L-1·min-1。则三个容器中合成氨的反应速率大小关系为( )
,经过相同的时间后,测得反应速率分别为甲:v(H2)=1 mol·L-1·min-1,乙:v(N2)=2 mol·L-1·min-1,丙:v(NH3)=3 mol·L-1·min-1。则三个容器中合成氨的反应速率大小关系为( )
A.v(甲)>v(乙)>v(丙)B.v(乙)>v(丙)>v(甲)
C.v(丙)>v(甲)>v(乙)D.v(乙)>v(甲)>v(丙)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com