
【题目】反应N2+3H2![]() 2NH3,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )
2NH3,开始时N2的浓度为3 mol·L-1,H2的浓度为5 mol·L-1,3 min后测得NH3浓度为0.6 mol·L-1,则此时间内,下列反应速率表示正确的是( )
A.v(H2)=0.3 mol·L-1·min-1B.v(N2)=1.0 mol·L-1·min-1
C.v(NH3)=0.2 mol·L-1·s-1D.v(H2)=1.67 mol·L-1·min-1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列溶液均为![]() ,有关叙述正确的是( )
,有关叙述正确的是( )
A.碳酸氢钠溶液中![]()
B.碳酸钠溶液比碳酸氢钠溶液的pH小
C.碳酸钠溶液中![]()
D.碳酸钠溶液中滴加盐酸至pH=7,所得溶液的溶质只有NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铁氰化钾(K4[Fe(CN)6])双称黄血盐,是一种重要的化工原料。检验三价铁发生的反应为:K4[Fe(CN)6]+FeCl3=KFe[Fe(CN)6]↓(滕氏蓝)+3KCl,回答问题:
(1)写出基态Fe3+的核外电子排布式___。
(2)K4[Fe(CN)6]中的作用力除共价键外,还有___和___。
(3)黄血盐中N原子的杂化方式为____;C、N、O的第一电离能由大到小的排序为___,电负性由大到小的排序为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH-=CaCO3↓+H2O
B.Fe(OH)3溶于氢碘酸: Fe(OH)3 + 3H+ =Fe3+ + 3H2O
C.泡沫灭火器灭火原理:2A13++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
D.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热:Ba2++ 2OH-+NH4++ HCO3-![]() NH3↑+2H2O+BaCO3↓
NH3↑+2H2O+BaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数小于36的X、Y、Z、W、R五种元素,原子序数依次增大。五种元素中,仅R为金属元素,其原子序数为27。X价电子排布式为nsnnpn,元素Z基态原子s电子总数与p电子总数相等,W与其它四种元素能层数不同,且未成对电子数目为1个。根据判断出的元素回答下列问题:
(1)R2+离子核外电子排布式为________,X、Y、Z三种原子第一电离能由小到大的顺序为________(用具体元素符号表示)。
(2)1 mol配合物[R(XY)6]4-中含有σ键的数目为________。
(3)XZW2是一种高毒类物质,结构与甲醛(HCHO)相似,其沸点高于甲醛的主要原因是________。
(4)YW3为黄色、油状、具有刺激性气味的液体,该分子的立体构型为________(用文字描述)。
(5)某晶体的晶胞结构如图所示,则该化合物的化学式为________(R、Z用具体元素符号表示)。
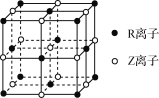
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、W六种元素在周期表中的位置如图所示,下列说法不正确的是
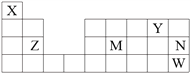
A. 原子半径:r(Z)>r(M)>r(Y)
B. 最高价氧化物对应水化物酸性:M>N
C. N的单质能与Z和W形成的化合物发生置换反应
D. X能与另五种元素形成化合物,且X的化合价不完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列填空:
(1)有下列分子或离子:①CS2,②PCl3,③H2S,④CH2O,⑤H3O+,⑥NH4+,⑦BF3,⑧SO2。粒子的立体构型为直线形的有________(填序号,下同);粒子的立体构型为V形的有________;粒子的立体构型为平面三角形的有________;粒子的立体构型为三角锥形的有____;粒子的立体构型为正四面体形的有____。
(2)俗称光气的氯代甲酰氯分子(COCl2)为平面三角形,但C—Cl键与C=O键之间的夹角为124.3°;C—Cl键与C—Cl键之间的夹角为111.4°,解释其原因:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一些净水器推销商在推销其产品时,进行所谓的“电解水法”实验,将纯净水与自来水进行对比。当电解装置插入纯净水和自来水中通电数分钟后,纯净水颜色无变化或略显黄色,而自来水却冒出气泡并生成灰绿色或红棕色的沉淀。根据上述现象,下列选项说法正确的是( )
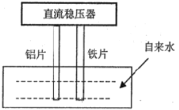
A.通电时,铝片做阳极,铁片做阴极
B.生成的气泡、红棕色或灰绿色的沉淀都是电解的直接或间接产物
C.通过对比,确实能说明自来水中含有大量对人体有毒有害的物质
D.铁片的电极反应:O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵分解反应为NH2COONH4(s)![]() 2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在一体积恒定的容器里,发生上面的反应,可以判断该反应已经达到平衡的是
A. 密闭容器中氨气的体积分数不变
B. 1 mol NH2COONH4分解同时有17g NH3消耗
C. 密闭容器中混合气体的密度不变
D. 混合气体的平均分子量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com