
����Ŀ�����ֶ�����Ԫ��A��B��C��D�����ʻ�ṹ��Ϣ���£�
��Ϣ����ԭ�Ӱ뾶��A��B��C��D��������Ԫ��֮���γɵ�ij���ַ��ӵı���ģ�ͼ������������£�
�ף�![]() �ǵ��������������֮һ���������������������Ҫ��Դ��Լռ�������ص�����֮����
�ǵ��������������֮һ���������������������Ҫ��Դ��Լռ�������ص�����֮����
�ң�![]() ��ɫ������ζ������ȼ���dz�����һ�ֻ�ʯ��Դ��
��ɫ������ζ������ȼ���dz�����һ�ֻ�ʯ��Դ��
����![]() ��ǿ�����Ե����ᣬ�����ֽ⣬����Ư���ԣ�������������ɱ���������������Ϣ�ش��������⡣
��ǿ�����Ե����ᣬ�����ֽ⣬����Ư���ԣ�������������ɱ���������������Ϣ�ش��������⡣
(1)��д��BC2���ӵĵ���ʽ��_______________��
(2)A���������У�EԪ�صĵ��ʻ�ԭ����ǿ��FԪ�ص�������������ԡ�E�������Ӧ�л�����X���ɡ���д������������Ӧ�����ӷ���ʽ��
��AԪ�صĵ��������ʼ�����Ӧ��_______________________________��
��F��C����Ԫ����ɵĻ�����Y����Ϊ���½ṹ�մɲ��ϣ�X��Y���ֻ���������Һ�з�����Ӧ��_________________________________________��
(3)���ʶ���Ԫ����ɺͼ���ͬ�������Ӿ���18���ӽṹ����ʢ��һ��Ũ�ȶ���Һ���Թ��У���μ��������ữ������������Һ���μӹ������Թ�����Һ������ػ�ɫ����ʼ���������ݳ���(����֤������)��Ƭ�̺�Ӧ��þ��ң������μ���Һ������һ��ʱ�䣬�Թܵײ����ֺ��ɫ��������ش�Ƭ�̺�Ӧ��þ��ҡ���ԭ������ǣ�
a________________________��b______________________��
(4)����Ԥ�⣺���������ԭ������Ϊ116�ŵ�Ԫ�أ��������ڱ��е�λ����_______��������____________Ԫ�أ���������ǽ�������
���𰸡� ![]() Cl2��H2O===H����Cl����HClO Al2O3��2OH��===2AlO
Cl2��H2O===H����Cl����HClO Al2O3��2OH��===2AlO![]() ��H2O ��Ӧ���ȣ��¶����� Fe3���д����� �������ڢ�A�� ����
��H2O ��Ӧ���ȣ��¶����� Fe3���д����� �������ڢ�A�� ����
�����������ֶ�����Ԫ��A��B��C��D������Ϣ�ڿ�֪����Ϊˮ����Ϊ���顢��Ϊ�����ᣬ�ٸ�����Ϣ��ԭ�Ӱ뾶��СA��B��C��D�ɵã�AΪClԪ�ء�BΪ̼Ԫ�ء�CΪ��Ԫ�ء�DΪ��Ԫ�ء�
(1)CO2������̼ԭ������ԭ��֮���γ�2�Թ��õ��Ӷԣ�����ʽΪ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(2)A���������У�EԪ�صĵ��ʻ�ԭ����ǿ����E��NaԪ�أ�FԪ�ص�ijЩ���ೣ������ˮ������F��AlԪ�أ�E�������Ӧ�л�����X��XΪNaOH��
(2)��������ˮ��Ӧ����HCl��HClO�����ӷ�Ӧ����ʽΪCl2+H2O=H++Cl-+HClO���ʴ�Ϊ��Cl2+H2O�TH++Cl-+HClO��
��Al��O����Ԫ����ɵĻ�����YΪAl2O3����������NaOH��Ӧ����ƫ�����ƺ�ˮ�����ӷ�Ӧ����ʽΪAl2O3+2OH-=2AlO2-+H2O���ʴ�Ϊ��Al2O3+2OH-�T2AlO2-+H2O��
(3)���ʶ���Ԫ����ɺͼ���ͬ�������Ӿ���18���ӽṹ������˫��ˮ����ʢ��һ��Ũ�ȶ���Һ���Թ��У���μ���������ϡ�����ữ������������Һ�����������ݳ���(����֤������)��˵��˫��ˮ�ֽ���������������ʱ��Ӧ2H2O2=2H2O+O2�������������ʼ�����٣����ŷ�Ӧ�Ľ����¶����ߣ����ұ��������Fe3+����ʹ��Ӧ���ʼӿ�����ң��ʴ�Ϊ����Ӧ���ȣ��¶����ߣ�Fe3+�д����ã�
(4)Ԫ�����ڱ���ǰ�������������������ɵ�Ԫ�������ǣ�2+8+8+18+18+32=86����ǰ�����ڿ�����Ԫ�ص������ǣ�86+32=118���ɼ�116��Ԫ��λ�ڵ������ڢ�A�壻���ڱ��ܴ��ϵ���Ԫ�صĽ���������ǿ����֪�������ڵ�PoԪ��Ϊ����Ԫ�أ����116��Ԫ��Ϊ����Ԫ�أ��ʴ�Ϊ���������ڢ�A�壻������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ķ���������ԭ���������ڰ����ӵ���������
A. 0.5mo1 C2H4 B. 11.2L(��״��) C2H2 ����
C. 23g Na D. 9g H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
�پ����з��Ӽ�������Խ����Խ�ȶ�����ԭ�Ӿ����й��ۼ�Խǿ���۵�Խ�ߡ��۸ɱ���CO2����ͨ������ͷ��Ӽ��������й������гɵķ��Ӿ��塡����Na2O��Na2O2�����У�������������֮����ȡ����������幹�͵ķ��ӣ����Ƕ���109��28�䣬�侧�����Ϳ�����ԭ�Ӿ������Ӿ��塡���Ӿ����ж����л�ѧ�����ߺ�4.8 g̼Ԫ�صĽ��ʯ�����еĹ��ۼ������ʵ���Ϊ0.8 mol
A. �٢ڢۢܢ� B. �ڢܢ� C. �ݢޢ� D. �ۢܢݢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ȡ﮺�﮵Ļ������ԭ�ϣ��õ�ⷨ�Ʊ�������﮵Ĺ���ԭ����ͼ��ʾ��������������ȷ����
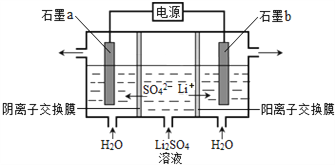
A. b��������Һ��pH����
B. a�������ķ�ӦΪ:2H2O �C 4e��= O2����4H+
C. �÷��Ʊ�LiOH���ɵõ�����������Ȳ�Ʒ
D. ����·��ͨ��1 mol����ʱ���ɵõ�2 molLiOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����X��Y��Z��W��R��QΪǰ������Ԫ�أ�ԭ��������������X��Y���������Ų��ɱ�ʾΪasa��bsbbpb��a��b����Y��Z��W��λ��P����ͬһ���ڵ�Ԫ�أ�Y��Wԭ�Ӻ����δ�ɶԵ�������ȣ�RW2��ZW2-Ϊ�ȵ����壬QΪ���ɽ���Ԫ�أ���ԭ�Ӻ���û��δ�ɶԵ��ӡ���ش��������⣺
��1��Q�����������Ų�ʽΪ_________ ,RW2�ķ������幹����_________________
��2��Y��Z��W������⻯���У�������С����_______���÷���ʽ��ʾ��, YW��Z2��Ϊ�ȵ����壬ZW�ĽṹʽΪ____________��������λ�������á�������ʾ����
��3��ZX3������X+��ϳ�ZX4+����������з����ı����____������ţ���

a.���Ŀռ乹�� b.Zԭ�ӵ��ӻ�����
c.X-Z-X�ļ��� d.���ĵ�����
��4��QR��ӫ���壬�����ϡ�Ϳ�ϡ����ϵ���ҵ��Ӧ�ù㷺������QR����ṹ��ͼ��ʾ��һ�������к��е�Qԭ����Ϊ____________����Rԭ������Ҿ�����ȵ�Rԭ����_____�����þ����ⳤ�����������Rԭ�ӵľ���֮��Ϊ_______
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�����̿�(��Ҫ�ɷ�MnO2��ͬʱ����FeCO3��Al2O3��SiO2��)Ϊ��Ҫԭ������KMnO4��һ������ͼ���£�
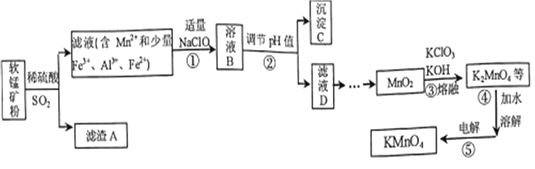
��֪��Mn(OH)2����������������Fe(OH)3��Al(OH)3����������������Ϊ4.0��10-38��1.3��10-33��
(1)����A�Ļ�ѧʽ��_________����ҺB�е���Ҫ��������______________��
(2)Ϊ�����������ʣ���������pH�����������____________������pH���������У���������
������________________��
(3)Ũ������MnO2��ӦҲ������Mn2+���仯ѧ����ʽ��___________________��
(4) K2MnO4�����ԡ����Ի����¶����绯����MnO4-��MnO2�������ԭ��Ӧ��֤_______________��
�����ܽ�ˮӦ������Ŀ����_____________________��
(5)�����������缫��Ӧʽ��____________���÷����ʱҪ������Ⱦ����ԭ����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�е�������Ũ����50 mL 1 mol/L��AlCl3��Һ��������Ũ����ȵ���
A��150 mL 1 mol/L��NaCl B��75 mL 3 mol/L��NH4Cl
C��150 mL 2 mol/L��KCl D��75 mL 2 mol/L��CaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��NO�������ɼ�������ŷ�β����NO�������乤��ԭ����ͼ��ʾ������˵����ȷ����

A. O2-�������ƶ�
B. �����ĵ缫��ӦʽΪ��NO��2e-+O2-=NO2
C. O2�ĵ缫��Ӧ������H2O
D. ��Ӧ���ĵ�NO��O2�����ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳ�ҩ���첫��·����ijһ�������£�

����˵���������
A. ����X������̼ԭ�ӿ�����ͬһƽ����
B. ����FeCl3��Һ����Z���Ƿ���X
C. �����ʵ�����X��Z �ֱ���H2�ӳɣ��������H2�����ʵ���֮��Ϊ3��5
D. �����ʵ�����X��Y�ֱ���NaOH��Ӧ���������NaOH�����ʵ���֮��Ϊ1��2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com