
【题目】根据下列图示所得出的结论正确的是( )
A.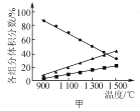 图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
图甲表示H2S(g)受热分解时各组分体积分数随反应温度的变化关系,说明反应生成H2和S
B.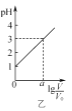 图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg
图乙表示V0 mL 0.1 mol·L-1的盐酸加水稀释至V mL,溶液的pH随lg![]() 的变化关系,则a=2
的变化关系,则a=2
C.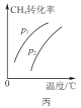 图丙表示密闭容器中CH4(g)+H2O(g)
图丙表示密闭容器中CH4(g)+H2O(g)![]() CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
CO(g)+3H2(g)到达平衡时,CH4的转化率与压强、温度的变化关系曲线,说明p1>p2
D.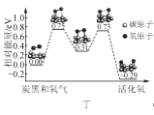 图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
图丁表示炭黑作用下O2生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收0.29 eV的能量
【答案】B
【解析】
A.一种物质的体积分数的变化量为50%-10%=40%,另一种生成物的体积分数的变化量为20%-10%=10%,不是1:1,不能说明反应生成H2和S,故A错误;
B.由溶液的pH随lg![]() 的变化关系,0.1 mol·L-1的盐酸加水稀释100倍,pH可由1变成3,即V0 mL 0.1 mol·L-1的盐酸加水稀释至V=100V0 mL,lg
的变化关系,0.1 mol·L-1的盐酸加水稀释100倍,pH可由1变成3,即V0 mL 0.1 mol·L-1的盐酸加水稀释至V=100V0 mL,lg![]() =2,则a=2,故B正确;
=2,则a=2,故B正确;
C.CH4(g)+H2O(g)![]() CO(g)+3H2(g)加压平衡逆向移动,甲烷的转化率降低,P2>P1,故C错误;
CO(g)+3H2(g)加压平衡逆向移动,甲烷的转化率降低,P2>P1,故C错误;
D.根据能量变化图分析,最终结果为活化氧,体系能量降低,则每活化一个氧分子放出0.29eV能量,故D错误;
故选B。


科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应的是( )
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mLNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol·L-1的盐酸,产生CO2气体的体积与所加盐酸体积之间的关系如图所示。下列判断正确的是
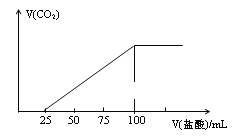
A.所得溶液溶质成分的物质的量之比为:n(NaHCO3):n(Na2CO3)=2: 1
B.所得溶液溶质成分的物质的量之比为:(NaOH):n(Na2CO3)=1: 3
C.原NaOH溶液的浓度为0.1mol/L
D.通入CO2体积为448mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前含有元素硒![]() 的保健品已开始涌入市场,已知它与氧同主族,而与钙同周期,下列关于硒的有关描述中不正确的是
的保健品已开始涌入市场,已知它与氧同主族,而与钙同周期,下列关于硒的有关描述中不正确的是
A.原子序数为24B.最高价氧化物为SeO3,为酸性氧化物
C.原子半径比钙小D.气态氢化物分子式为H2Se,受热较容易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液常用于蚀刻电路板,蚀刻后的酸性溶液中含有Cu2+、Fe2+、Fe3+、Cl-等。下列各组离子能在该酸性溶液中大量共存的是( )
A.Na+、Al3+、Cl-、SO42-B.Ca2+、Mg2+、NO3-、ClO-
C.K+、NH![]() 、SO32-、AlO2-D.Ba2+、K+、I-、NO3-
、SO32-、AlO2-D.Ba2+、K+、I-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苋菜甲素、3-丁烯基苯酞、藁本内酯是传统中药当归、川芎中的活性成分。下列有关说法正确的是( )
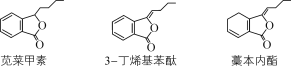
A.苋菜甲素、藁本内酯互为同分异构体
B.1 mol 3-丁烯基苯酞与溴水反应最多消耗4 mol Br2
C.3-丁烯基苯酞通过还原反应可制得苋菜甲素
D.藁本内酯与足量H2加成的产物分子中含有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源,它的制取与应用一直是人类研究的热点。
(1)用甲醇和水蒸气在催化剂、加热条件下制氢的相关热化学方程式如下:
CH3OH(g)=CO(g)+2H2(g);ΔH=+90.7 kJ/mol
CO(g)+H2O(g)=CO2(g)+H2(g);ΔH=-41.2 kJ/mol
①反应CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)能自发进行的原因是________。
CO2(g)+3H2(g)能自发进行的原因是________。
②将一定比例的CH3OH(g)和H2O(g)的混合气体,以相同速率通过装有不同催化剂的反应器。CH3OH转化率随催化剂的使用时长变化如图1所示,催化剂CuAl2O4与催化剂Cu/Zn/Al相比,优点有____________________。
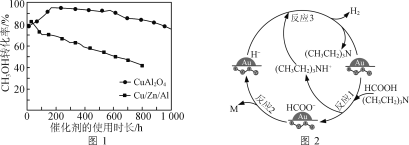
③向Cu(NO3)2、Al(NO3)3混合溶液中滴加NaOH溶液可获得沉淀物[Cu(OH)2、Al(OH)3],以便于制取CuAl2O4。为确保Cu2+、Al3+完全沉淀(浓度≤10-5 mol/L),应控制混合液pH的最小整数值为________{Ksp[Cu(OH)2]=2.2×10-20,Ksp[Al(OH)3]=1.3×10-33}。
(2)用Au/ZrO2作催化剂,在(CH3CH2)3N作用下HCOOH分解制氢的原理如图2所示。反应2中生成物M的化学式为__________________,图示反应中只有氢元素化合价发生变化的是反应________(填“1”“2”或“3”)。
(3)如图是电解氨水和KOH混合溶液制氢的装置示意图。生成N2的电极反应式为______________。
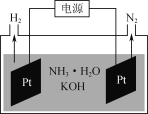
(4)富氧条件下,H2还原NOx包括两个阶段:第一阶段为H2、NOx在催化剂作用下转变为H2O、N2、NH3;第二阶段NH3在载体酸的作用下生成NH4+,NH4+将NOx还原为N2。写出NO与O2的物质的量之比为1∶1时,NH4+与NO、O2反应生成N2的离子反应方程式:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
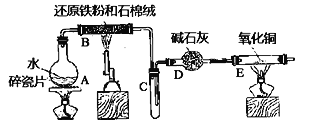
回答下列问题:
(1)装置B中发生反应的化学方程式是__________
(2)E中出现______________的现象。
(3)该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3·6H2O晶体。
①欲检验溶液中含有Fe3+,选用的试剂为____________,现象是__________
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的的原因:___________。
③将此滤液中FeCl2完全氧化为FeCl3最好选择_______做氧化剂。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钟南山院士指出,实验证明中药连花清瘟胶囊对治疗新冠肺炎有明显疗效,G是其有效药理成分之一,存在如图转化关系:
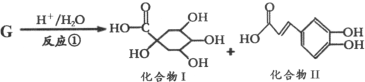
下列有关说法正确的是
A.化合物Ⅱ中所有碳原子可能都共面
B.化合物Ⅰ分子中有3个手性碳原子
C.化合物G、Ⅰ、Ⅱ均能发生氧化反应、取代反应、消去反应
D.若在反应中,G与水按1:1发生反应,则G的分子式为C16H20O10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com