
【题目】关于氮的变化关系图如图:
![]()
则下列说法不正确的是( )
A.路线①②③是工业生产硝酸的主要途径
B.路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径
C.上述所有反应都是氧化还原反应
D.上述路线的所有反应中只有I属于氮的固定
【答案】D
【解析】
根据转化关系图,确定化合价的变化和物质的转化关系,利用所学知识进行解题。
A.工业上生产硝酸的流程是:氮气和氢气生成氨气,氨气与氧气反应4NH3+5O2![]() 4NO+6H2O路线①,一氧化氮与氧气反应2NO+O2=2NO2路线②,二氧化氮被水吸收3NO2+H2O═2HNO3+NO路线③,路线①②③是工业生产硝酸的主要途径,A正确;
4NO+6H2O路线①,一氧化氮与氧气反应2NO+O2=2NO2路线②,二氧化氮被水吸收3NO2+H2O═2HNO3+NO路线③,路线①②③是工业生产硝酸的主要途径,A正确;
B.在放电条件下,氮气和氧气发生化合反应:N2+O2![]() 2NO路线Ⅰ,NO不稳定,易被氧气氧化为二氧化氮:2NO+O2═2NO2路线Ⅱ,二氧化氮溶于水生成硝酸:3NO2+H2O═2HNO3+NO路线Ⅲ,B正确;
2NO路线Ⅰ,NO不稳定,易被氧气氧化为二氧化氮:2NO+O2═2NO2路线Ⅱ,二氧化氮溶于水生成硝酸:3NO2+H2O═2HNO3+NO路线Ⅲ,B正确;
C.从氮的变化关系图可知:N从N2(0价)→NO(+2价)[NH3(-3价)]→NO2(+4价)→HNO3(+5价),都是氧化还原反应,C正确;
D.氮的固定是将氮气单质转化为氮的化合物,N2→NO和N2→NH3都属于氮的固定,D错误。
答案选D。


科目:高中化学 来源: 题型:
【题目】有8种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯(![]() ) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
A. ③④⑤⑧ B. ④⑤⑦⑧ C. ④⑤⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,对应的现象以及结论都正确的是
选项 | 实验 | 现象 | 结论 |
A | 碘酒滴到土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
B | 大试管中CH4和Cl2按照1∶1混合,放于光亮处 | 试管内气体颜色变浅,试管壁出现油状液滴,管中有白雾 | 光照条件下,CH4和Cl2发生了化学变化 |
C | 向20%蔗糖溶液中加入少量稀硫酸,加热,再加入新制氢氧化铜后再加热至沸腾 | 无明显现象 | 蔗糖未发生水解 |
D | 小块鸡皮上滴加3~5滴浓硝酸 | 鸡皮由白变黄 | 蛋白质都能发生颜色变化 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】山梨酸是应用广泛的食品防腐剂,其分子结构如图所示。下列说法错误的是
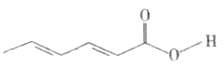
A.山梨酸的分子式为C6H8O2
B.1 mol山梨酸最多可与2 mol Br2发生加成反应
C.山梨酸既能使稀KMnO4酸性溶液褪色,也能与醇发生置换反应
D.山梨酸分子中所有碳原子可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )。
A.用浓盐酸与二氧化锰反应制取少量氯气:MnO2+4HCl![]() Mn2+ + 2Cl-+ Cl2↑+2H2O
Mn2+ + 2Cl-+ Cl2↑+2H2O
B.在NaHCO3溶液中滴加少量Ca(OH)2:![]() + Ca2+ + OH═ CaCO3↓+ H2O
+ Ca2+ + OH═ CaCO3↓+ H2O
C.氯气与水反应:Cl2 + H2O ═ 2H+ + Cl- +ClO-
D.NaClO溶液中通入少量的SO2:3ClO﹣+H2O+SO2═Cl﹣+![]() +2HClO
+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )

A.1:3B.2:3
C.6:1D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图所示:

请你根据上图推断:
(1)原溶液中一定存在的阴离子有_______________,显___(填“酸”“碱”或“中”)性。
(2)实验③中产生无色无味气体所发生的化学方程式为__________________________________。
(3)写出实验④中A点对应沉淀的化学式:__________。
(4)写出实验④中,由A→B过程中所发生反应的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚硅酸铁是目前无机高分子絮凝剂研究的热点,一种用钢管厂的废铁渣(主要成分Fe3O4,少量碳及二氧化硅)为原料制备的流程如下:
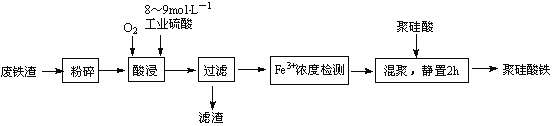
(1)废铁渣进行“粉碎”的目的是____________。
(2)“酸浸”需适宜的酸浓度、液固比、酸浸温度、氧流量等,其中酸浸温度对铁浸取率的影响如右图所示:
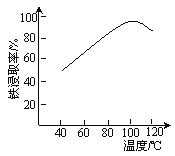
①加热条件下酸浸时,Fe3O4与硫酸反应的化学方程式为___________。
②酸浸时,通入O2的目的是_____________,该反应的离子方程式为_________。
③当酸浸温度超过100℃时,铁浸取率反而减小,其原因是____________。
(3)滤渣的主要成分为____________(填化学式)。
(4)“Fe3+浓度检测”是先用SnCl2将Fe3+还原为Fe2+;在酸性条件下,再用K2Cr2O7标准溶液滴定Fe2+(Cr2O72-被还原为Cr3+),该滴定反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧熔融碳酸盐燃料电池是一种高温电池(600﹣700℃),具有效率高、噪音低、无污染等优点。氢氧熔融碳酸盐燃料电池的工作原理如图所示。下列说法正确的是( )
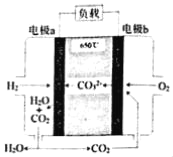
A.电池工作时,熔融碳酸盐只起到导电的作用
B.负极反应式为H2﹣2e﹣+CO32﹣═CO2+H2O
C.电子流向是:电极a﹣负载﹣电极b﹣熔融碳酸盐﹣电极a
D.电池工作时,外电路中流过0.2mol电子,消耗3.2gO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com