
【题目】氯丁橡胶M是理想的电线电缆材料,工业上可由有机化工原料A或E制得,其合成路线如下图所示。

完成下列填空:
(1)A的名称是_______,反应③的反应类型是_____。
(2)写出反应②的化学反应方程式_____。
(3)为研究物质的芳香性,将E三聚、四聚成环状化合物,写出它们的结构简式_____。鉴别这两个环状化合物的试剂为_______。
(4)以下是由A制备工程塑料PB的原料之一1,4-丁二醇(BDO)的合成路线:
![]()
写出上述由A制备BDO的化学反应方程式__________。
【答案】1,3—丁二烯 加聚反应 CH2=CHCHClCH2Cl+KOH 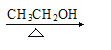 CH2=CHCCl=CH2+H2O+KCl )
CH2=CHCCl=CH2+H2O+KCl )![]() 、
、![]() 溴水或酸性高锰酸钾溶液 CH2=CHCH=CH2+Cl2
溴水或酸性高锰酸钾溶液 CH2=CHCH=CH2+Cl2![]() ClCH2CH=CHCH2Cl、ClCH2CH=CHCH2Cl+2NaOH
ClCH2CH=CHCH2Cl、ClCH2CH=CHCH2Cl+2NaOH![]() HOCH2CH=CHCH2OH+2NaCl、HOCH2CH=CHCH2OH+H2
HOCH2CH=CHCH2OH+2NaCl、HOCH2CH=CHCH2OH+H2![]() HOCH2CH2CH2CH2OH
HOCH2CH2CH2CH2OH
【解析】
根据氯丁橡胶M的结构简式可知,C的结构简式为CH2=CHCCl=CH2;A与氯气反应生成B,则根据A的分子式可知,A的结构简式为CH2=CHCH=CH2,因此B的结构简式为CH2=CHCHClCH2Cl,根据B和C的结构简式可知,B→C发生了消去反应;C发生加聚反应生成高分子M;E二聚得到CH2=CHC≡CH,则E是乙炔;据以上分析解答。
(1)结合以上分析可知,A的结构简式为CH2=CHCH=CH2,A的名称是1,3—丁二烯,反应③的反应类型是加聚反应;
(2)反应②是卤代烃的消去反应,反应的化学反应方程式为CH2=CHCHClCH2Cl+KOH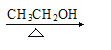 CH2=CHCCl=CH2+H2O+KCl;
CH2=CHCCl=CH2+H2O+KCl;
(3)E二聚得到CH2=CHC≡CH,则E是乙炔,因此乙炔三聚、四聚成环状化合物的结构简式分别为![]() 、
、![]() 。苯不能使酸性高锰酸钾溶液褪色,也不能与溴水发生反应导致溴水褪色,而
。苯不能使酸性高锰酸钾溶液褪色,也不能与溴水发生反应导致溴水褪色,而![]() 含有碳碳双键,能使酸性高锰酸钾溶液褪色或溴水褪色,则鉴别这两个环状化合物的试剂为酸性高锰酸钾溶液或溴水;
含有碳碳双键,能使酸性高锰酸钾溶液褪色或溴水褪色,则鉴别这两个环状化合物的试剂为酸性高锰酸钾溶液或溴水;
(4)要得到1,4-丁二醇,则需要ClCH2CH2CH2CH2Cl进行水解反应,因此可以利用1,3—丁二烯发生1,4—加成,最后再与氢气加成即可,则有关反应的化学方程式为CH2=CHCH=CH2+Cl2![]() ClCH2CH=CHCH2Cl;ClCH2CH=CHCH2Cl+2NaOH
ClCH2CH=CHCH2Cl;ClCH2CH=CHCH2Cl+2NaOH![]() HOCH2CH=CHCH2OH+2NaCl;HOCH2CH=CHCH2OH+H2
HOCH2CH=CHCH2OH+2NaCl;HOCH2CH=CHCH2OH+H2![]() HOCH2CH2CH2CH2OH。
HOCH2CH2CH2CH2OH。


 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:高中化学 来源: 题型:
【题目】常温下,向![]() 溶液中,不断通入HCl气体
溶液中,不断通入HCl气体![]() 忽略溶液体积变化
忽略溶液体积变化![]() ,得到
,得到![]() 和
和![]() 与pH的变化关系如图所示,则下列说法不正确的是
与pH的变化关系如图所示,则下列说法不正确的是![]()
A.溶液中水的电离程度:![]()
B.在y点时,通入的HCl气体在标准状况下的体积为![]()
C.随着HCl的通入,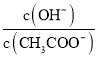 不断减小
不断减小
D.该温度下,![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 时,有
时,有![]() 的一组醋酸和醋酸钠的混合溶液,溶液中
的一组醋酸和醋酸钠的混合溶液,溶液中![]() 、
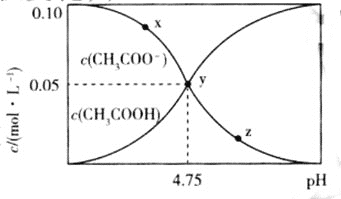
、![]() 与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是
与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述正确的是 ![]()
![]()

A.![]() 的溶液中:
的溶液中:![]()
B.该温度下醋酸的电离平衡常数为![]()
C.![]() 的溶液中:
的溶液中:![]()
D.向W点所表示的溶液中加入等体积的![]() 溶液:
溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
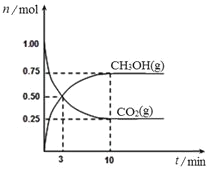
![]() 。某温度下,在容积为1L的密闭容器中充入1mol
。某温度下,在容积为1L的密闭容器中充入1mol![]() 和
和![]()
![]() ,在一定条件下反应,测得
,在一定条件下反应,测得![]() 、
、![]() 的物质的量随时间的变化关系如图所示。下列说法正确的是
的物质的量随时间的变化关系如图所示。下列说法正确的是
A.从反应开始到平衡,![]() 的平均反应速率
的平均反应速率![]()
![]()
B.此温度下,该反应的平衡常数为![]()
C.缩小体积,既能增大反应速率,又能提高![]() 的转化率
的转化率
D.欲增大平衡状态时![]() ,可采用升高温度的方法
,可采用升高温度的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构简式如图所示。下列叙述正确的是( )

A. 迷迭香酸与溴单质只能发生取代反应
B. 1 mol迷迭香酸最多能和9 mol氢气发生加成反应
C. 迷迭香酸可以发生水解反应、取代反应和酯化反应
D. 1 mol迷迭香酸最多能和5 mol NaOH发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂制备净水剂硫酸铁铵晶体![]() 的一种方案如下:
的一种方案如下:

下列说法不正确的是![]()
A.滤渣A的主要成分是![]()
B.“合成”反应要控制温,温度过高,产率会降低
C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等
D.相同条件下,![]() 净水能力比
净水能力比![]() 强
强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充放电的化学方程式为2K2S2+KI3![]() K2S4+3KI;装置(Ⅱ)为电解池的示意图,当闭合开关K时,X附近溶液先变红。则下列说法正确的是
K2S4+3KI;装置(Ⅱ)为电解池的示意图,当闭合开关K时,X附近溶液先变红。则下列说法正确的是![]() ( )
( )
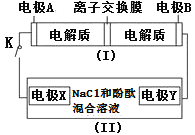
A.闭合K时,K+从左到右通过离子交换膜
B.闭合K时,电极X是阳极
C.闭合K时,电极A的反应式为3I--2e-=I3-
D.闭合K时,当有0.1molK+通过离子交换膜,X电极上产生气体2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有四种短周期元素,它们的结构、性质等信息如下表所述:
元素 | 结构、性质等信息 |
A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
B | B与A同周期,其最高价氧化物的水化物呈两性 |
C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
请根据表中信息填写:
(1)D﹣的结构示意图是___。
(2)C元素的气态氢化物的化学式为:___;其检验方法:___。
(3)B元素在周期表中的位置___;离子半径:B___A(填“大于”或“小于”)。
(4)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为___,与D的氢化物的水化物反应的离子方程式为___。
II.在2L密闭容器内,800℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(1)NO的平衡浓度c/span>(NO)=___。
(2)图中表示NO2变化的曲线是___,用O2表示0~2s内该反应的平均速率υ=___。
(3)能说明该反应已达到平衡状态的是___。
a.υ(NO2)=2υ(O2) b.容器内气体压强保持不变
c.υ逆(NO)=2υ正(O2) d.容器内气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.6 g金属钠投入到足量水中,得ag溶液;将4.8 g金属镁投入到足量盐酸中,得bg溶液,假设水的质量与盐酸的质量相等,则反应后两溶液的质量关系式为 ( )
A.a=bB.a>b
C.a<bD.无法判断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com