


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、收集一定量的火山气体通入足量BaCl2溶液中,只能生成BaSO4一种沉淀 |
| B、②③④属于酸性氧化物 |
| C、⑤属于强电解质 |
| D、①②③④属于非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
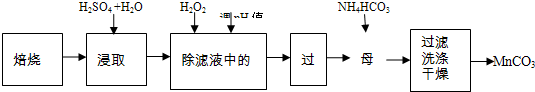
| 化学式 | 开始沉 淀时的 pH值 | 沉淀完 全时的 pH值 |
| Mn(OH)2 | 8.8 | 10.4 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe (OH)3 | 2.7 | 3.7 |
| Zn(OH)2 | 6.4 | 7.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
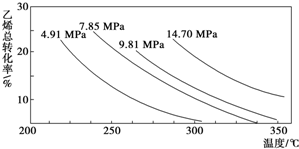 工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为CH2═CH2(g)+H2O(g)?CH3CH2OH(g),副产物有乙醛、乙醚及乙烯的聚合物等.如图是乙烯的总转化率随温度、压强的变化关系,下列说法正确的是( )| A、合成乙醇的反应一定为放热反应 |
| B、目前工业上采用250~300℃,主要是因为在此温度下乙烯的转化率最大 |
| C、目前工业上采用加压条件(7 MPa左右),目的是提高乙醇的产率和加快反应速率 |
| D、相同催化剂下,在300℃14.70 MPa乙醇产率反而比300℃7.85 MPa低得多,是因为加压平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、“雾霾”不属于自然现象 |
| B、PM2.5的产生与人类活动有关 |
| C、PM2.5分散在空气中形成的混合物具有丁达尔效应 |
| D、开发利用新能源,减少化石燃料的使用是缓解雾霾天气发生的重要措施 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com