
钒及化合物用途广泛。工业上常用含少量Al2O3的钒铁矿(FeO×V2O5)碱熔法提取V2O5。简要流程如下:
已知:①焙烧时可发生反应:V2O5 + Al2O3+2Na2CO3 2NaVO3 +2NaAlO2 +2CO2
2NaVO3 +2NaAlO2 +2CO2
②常温下物质的溶解度:NaVO3~21.2 g /100g水;HVO3~0.008 g /100g水
(1)“浸出渣B”的主要成分是 。(写化学式)
(2)生产中,不直接用H2SO4浸泡“烧渣A”获取HVO3的原因是 。
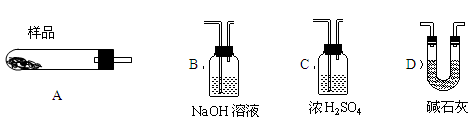
(3)“操作①”包括 、洗涤。如果不洗涤,则产品中可能含有的金属阳离子是 、 。下列装置(部分夹持仪器省去)可用在实验室进行“操作②”的是 。(填序号)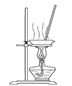

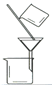
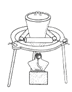
A B C D
(4)NaVO3用于原油的脱硫技术,由V2O5溶于NaOH溶液中制取,反应的离子方程式为 。
(1)Fe2O3或Fe3O4,或者Fe2O3和Fe3O4 (2分)
(2)H2SO4与NaVO3反应生成难溶的HVO3,HVO3包裹在一些烧渣的表面,阻碍了反应的进行,从而降低了HVO3产率,且使产生的HVO3不纯。另外,铁的氧化物会和硫酸反应生成铁离子,增加干扰离子,消耗硫酸,浪费资源。(4分)
(3)过滤(2分) Na+、Al3+(2分) D (2分)
(4)V2O5 +2OH 2VO3-+ H2O (2分)(可以没有加热符号)
2VO3-+ H2O (2分)(可以没有加热符号)
解析试题分析:(1)依题意,焙烧时不仅发生反应:V2O5+Al2O3+2Na2CO3 =2NaVO3+2NaAlO2+2CO2↑,而且FeO被空气中的氧气氧化为氧化铁(或四氧化三铁或既有氧化铁又有四氧化三铁),因为+2价的铁元素在高温下易被氧化;由于加入的碳酸钠过量,则氧化铝、五氧化二钒全部转化为可溶性的钠盐,加入足量水浸取时,铁的氧化物难溶于水,则浸出渣B的主要成分是Fe2O3或Fe3O4,或者Fe2O3和Fe3O4;(2)由已知信息②可知,H2SO4与NaVO3反应生成难溶的HVO3,HVO3包裹在一些烧渣的表面,阻碍了反应的进行,从而降低了HVO3产率,且使产生的HVO3不纯;另外,铁的氧化物会和硫酸反应生成铁离子,增加干扰离子,消耗硫酸,浪费资源,因此不采取硫酸浸取烧渣;(3)由于HVO3的溶解度很小,HVO3难溶于水,从浸出液中分离难溶物的方法是过滤、洗涤,由此确定操作①的方法;如果不洗涤,HVO3吸附了可溶性的硫酸钠、硫酸铝典礼处的钠离子和铝离子;HVO3是难溶性酸,与硅酸类似,受热可以分解,加热固体物质只能在坩埚中进行实验,因此选D;(4)五氧化二钒与NaOH溶液反应生成钒酸钠和水,不涉及氧化还原反应,说明五氧化二钒具有酸性氧化物的性质,氧化物应保留化学式,则该反应为V2O5 +2OH- = 2VO3-+ H2O;
考点:考查物质制备化学工艺流程,涉及浸出渣的主要成分、解释浸取方式的原因、混合物分离与提纯的方法、洗涤除去的金属阳离子、高温加热固体的实验仪器及装置、离子方程式。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
二氧化铈(CeO2)是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下: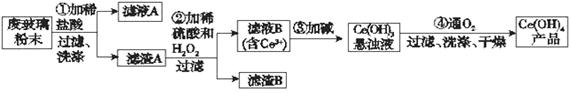
(1)洗涤滤渣A的目的是为了除去____________(填离子符号),检验该离子是否洗净的方法是_________________________________________________________。
(2)第②步反应的离子方程式是______________________________________,滤渣B的主要成分是___________________。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP______________(填“能”或“不能”)与水互溶。实验室进行萃取操作时用到的主要玻璃仪器有_______________、烧杯、玻璃棒、量筒等。
(4)取上述流程中得到的Ce(OH)4产品0.536 g,加硫酸溶解后,用0.100 0 mol·L-1 FeSO4标准溶液滴定至终点时(铈被还原为Ce3+),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质量分数为___________(结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
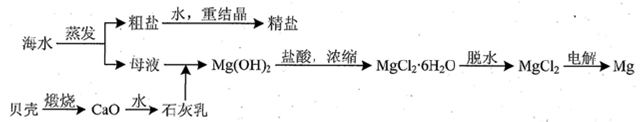
海洋是生命的摇篮、资源的宝库。中国要实施海洋强国战略,实现由海洋大国向海洋强国迈进的梦想。海洋经济已经成为拉动我国国民经济发展的重要引擎,海水的综合开发、利用是海洋经济的一部分,海水中可提取多种化工原料,下面是工业上对海水的几项综合利用的示意图。其流程如下图所示:
(1)写出①、②反应的离子方程式:
①______________________,②______________________。
(2)工业上利用电解饱和食盐水产生的氢气和氯气制取盐酸,为了体现绿色化学理念,使氯气充分反应,采取将氯气在氢气中燃烧的办法,可避免氯气燃烧不完全污染空气,请写出氯气在氢气中燃烧的实验现象:______________________。
(3)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制后可得到饱和NaC1溶液。现有下列除杂试剂:A.盐酸 B.氢氧化钡溶液 C.碳酸钠溶液。精制时加入过量除杂试剂的正确顺序是______________。(填序号)
(4)金属镁在空气中燃烧时,除生成MgO外,还有少量Mg3N2生成。把等物质的量的金属镁分别放在:A.纯氧气(O2)中;B.二氧化碳气体中;C.空气中。完全燃烧后,得到的固体物质的质量由大到小的顺序是______________。(填序号)
(5)将电解饱和NaCl溶液生成的氯气通入氢氧化钠溶液中可以得到NaClO。某化学兴趣小组探究NaClO与尿素CO(NH2)2的反应产物,通过实验发现产物除某种盐外,其余产物都是能参与大气循环的物质,则该反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海水中主要离子的含量如下:
| 成分 | 含量/(mg/L) | 成分 | 含量/(mg/L) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Mg2+ | 1272 |
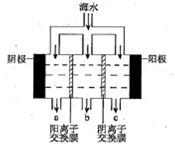
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有三瓶无色溶液的标签损坏了,只知道它们分别是盐酸、BaCl2溶液和Na2CO3溶液。甲、乙两位同学各用一种试剂,一次性鉴别都取得了成功。甲用的一种指示剂是_________;乙用的一种酸溶液是__________。丙同学没用任何试剂也鉴别成功了,他的鉴别过程是:取样于试管中,编号为a、b、c,然后将三种溶液两两混合,发现a加入b中有气泡产生,a加入c中有白色沉淀产生,则a、b、c分别是________、________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成,由蛇纹石制取碱式碳酸镁的实验步骤如下:
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致 溶解,产生 沉淀。
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl-、Br-(溴离子)、SO42-、Na+、Mg2+、Ca2+等,都是重要资源。
(1)写出步骤①、②、④分离提纯的方法:
① ; ② ; ④ 。
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 。
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 。向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体。
(4)检验淡水中是否含有Cl-的操作现象及结论 。
(5)写出加入试剂a后,发生反应的离子方程式 。
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和石灰乳制取漂白粉的化学方程式 ________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
(1)硫酸渣的成分中属于两性氧化物的是 , 写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式: ;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是_________;(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
鉴别下列各组物质,按要求回答问题。
(1)稀硫酸、稀盐酸
①可选作鉴别的试剂有(填编号,可多选)_________。
A.BaCl2溶液 B.Mg(NO3)2溶液 C.Na2CO3溶液
②鉴别反应的离子方程式:_________________________。
(2)饱和碳酸钠溶液、澄清石灰水
①可选用鉴别的试剂有(填编号,可多选)____。
a.盐酸 b.NaCI c.硝酸 d.BaCl2溶液
②依次写出鉴别中有明显现象的反应的离子方程式:________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com