
����Ŀ�����ԭ����ԭ���ԭ���ǵ绯��������Ҫ���ݡ�ij��ȤС��������̽��ʵ�飺
(1)��ͼΪijʵ��С������������ԭ��Ӧ��Ƶ�ԭ���װ�ã��÷�Ӧ�����ӷ���ʽΪ_____________����Ӧǰ���缫������ȣ�һ��ʱ������缫�������12g��������ͨ��_______mol���ӡ�

(2)�����������䣬����CuCl2��Һ��ΪNH4Cl��Һ��ʯī�缫�ķ�ӦʽΪ________________��
(3)��ͼ�������������䣬�������Ż�����ͭ������ʯī������n�ͣ���װ����ʯī(2)�缫�Ϸ����ķ�ӦʽΪ_________________��

���𰸡�Fe+Cu2+=Cu+Fe2+ 0.2 2H++2e-=H2�� 2Cl--2e-=Cl2��
��������
��1�������Է�������ԭ��Ӧ֪ʶ����д��������������Ӧ������������仯���м��㣻
��2���Ȼ���У�笠�����ˮ�����Һ��ʾ���ԣ���������������
��3�������������䣬�������Ż�����ͭ������ʯī������n�ͣ�����װ���ǵ��أ���װ����ԭ��ء�
(1)��Ƶ�ԭ���װ�õ��Է�������ԭ��Ӧ�ǣ�Fe+Cu2+=Cu+Fe2+�������ת������x����64g/mol��0.5x+56g/mol��0.5x=12g�����x=0.2mol���ʴ�Ϊ��Fe+Cu2+=Cu+Fe2+��0.2��
(2)�Ȼ���У�笠�����ˮ�����Һ��ʾ���ԣ�ʵ���ǣ�NH4++H2ONH3H2O+H+����������2H++2e-=H2�����ʴ�Ϊ��2H++2e-=H2����
(3)�����������䣬�������Ż�����ͭ������ʯī������n�ͣ�����װ���ǵ��أ���װ����ԭ��أ�Fe�Ǹ�����Cu˿������������������ͭ������ʯī�缫���������ü��Ϸ����ķ�ӦʽΪ2Cl--2e-=Cl2�����ʴ�Ϊ��2Cl--2e-=Cl2����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���Ʊ���ЧƯ��NaClO2��ʵ��������ͼ��ʾ����ӦI�з����ķ�ӦΪ3NaClO3+4SO2+3H2O====2ClO2+Na2SO4+3H2SO4+NaCl������˵������ȷ����

A. ��Ӧ����H2O2����ԭ��
B. ��Ʒ�к���SO42����Cl��
C. NaClO2��Ư��ԭ����SO2��ͬ
D. ʵ���ҽ��нᾧ����ͨ���������н���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߡ�����������ʾ���ʱ仯�Ļ�ѧ������������( )
A.ϡ������Һ��ϡ�������Ƶ��к��ȣ�H��(aq)��OH��(aq)��H2O(l) ��H����57.3 kJ�� mol��1
B.FeCl3��Һˮ������ӷ���ʽ��Fe3��+3H2O![]() Fe (OH)3+3H+
Fe (OH)3+3H+
C.�Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H=-38.6kJ��mol��1��һ�������£���0.5mol N2(g)��1.5molH2(g)�����ܱյ������з�Ӧ����NH3(g)�������19.3kJ
2NH3(g) ��H=-38.6kJ��mol��1��һ�������£���0.5mol N2(g)��1.5molH2(g)�����ܱյ������з�Ӧ����NH3(g)�������19.3kJ
D.CO(g)��ȼ������283.0 kJ��mol��1����2CO2(g)��2CO(g)+O2(g) ��H=+566.0 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������ܴﵽʵ��Ŀ�ĵ���
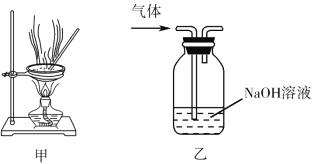
A. �þ�ˮʪ���pH��ֽ������Һ��pH
B. ��4.0 g NaOH��������100 mL����ƿ�У���ˮ���̶ȣ�����1.000 mol��L1NaOH��Һ
C. ��װ�ü�����AlCl3��Һ����ˮAlCl3����
D. ��װ���ҳ�ȥʵ����������ϩ�е�����SO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̽���С����ݺ�°��Ƽ�ԭ������������Ƶķ����Ʊ�̼�����ơ�ʵ��װ������ͼ��ʾ(ͼ�мг֡��̶��õ�����δ����)������˵����ȷ����

A. ��װ����ʢ�ŵ��DZ���ʳ��ˮ
B. ��װ���е���Һ����ǣ�����̼�����ƾ�������
C. ��װ���е��۵�©����Ҫ�����Ƿ�ֹ������������Ⱦ����
D. ʵ���������̼�����ƵIJ����������ᾧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������( AlN)��һ���������ǽ������ϣ�������AlN +NaOH+H2O=NaAlO2+NH3����ij����С�����ü�ͼ��ʾװ�òⶨ��Ʒ��AlN�ĺ��������ʲ���Ӧ��������˵������ȷ����

A. �������е�Һ��ӦΪˮ
B. �ó���©�������Һ©���������ڿ��Ʒ�Ӧ����
C. ��Ӧ����ʱ��a��b����Һ��IJ�ֵ��Ϊ������������
D. ��������������ȷ,ʵ�����ʱ����ͼ���������AlN����ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ij�¶���KW=10��12����0.05mol/LH2SO4��Һ��pH=____ ��0.01mol/LNaOH��Һ��pH=______ ��
(2)�����������������ˮ���йص�����______��
��������FeCl3������ˮ��
��ʵ��������AlCl3��Һʱ��Ӧ�Ȱ������ڽ�Ũ�������У�Ȼ���ˮϡ��
��Ϊ����FeCl3��Һ��Ҫ����Һ�м���������
����NaHCO3��Al2(SO4)3������Һ������ĭ����
��ʵ����ʢ��Na2CO3��Һ���Լ�ƿӦ����Ƥ���������ò�����
��NH4Cl��ZnCl2��Һ���������еij����
�߳���ʹ������泥�����������ǿ����ľ�����̬���ʲ��ܻ��ʩ��
A.�٢ܢߡ�����B.�ڢݢ� C.�ۢޢ� D.ȫ���й�
(3)��1 mol N2��ȫת��ΪNH3�ķ�Ӧ��Ϊ��H=��92 kJ/mol����1 mol H��H����1 mol N![]() N ����Ҫ�������ֱ���436 kJ��946 kJ�����1 mol N��H����Ҫ��������__________kJ��
N ����Ҫ�������ֱ���436 kJ��946 kJ�����1 mol N��H����Ҫ��������__________kJ��
(4)��֪25�� ʱ�������Ka=1.8��10��5 ̼���Ka1=4.3��10��7 Ka2=5.6��10��11 ���Т�NaHCO3��Һ��CH3COONa��Һ��NaOH��Һ��Na2CO3��25 mL��Ũ�Ⱦ�Ϊ0.1 mol��L��1������Һ��pH�ɴ�С��˳��Ϊ_________ (�����)
(5)Na2CO3��Һ���Ⱥ������ǿ����ϻ�ѧƽ���ƶ�ԭ������ԭ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��װ�õ������������ȷ����
A.![]() ������Ҷ������ɫ�صķ���
������Ҷ������ɫ�صķ���
B. �����ڹ��˿�����С�ij����������ڹ��˽�״����
�����ڹ��˿�����С�ij����������ڹ��˽�״����
C.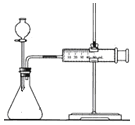 ������ijЩ��ѧ��Ӧ���ʵIJⶨ����װ�������Եļ�����£�������װ�ú�,�رշ�Һ©������������Ͳ����������һ�ξ��룬Ȼ�����֣��۲���Ͳ�Ƿ��ܻص�ԭ���̶ȴ�
������ijЩ��ѧ��Ӧ���ʵIJⶨ����װ�������Եļ�����£�������װ�ú�,�رշ�Һ©������������Ͳ����������һ�ξ��룬Ȼ�����֣��۲���Ͳ�Ƿ��ܻص�ԭ���̶ȴ�
D.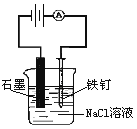 ��������ģ���ȼҵ
��������ģ���ȼҵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H2Sת��Ϊ�������õ���Դ����Դ�о��������Ҫ���⡣ijת������ԭ����ͼ����װ�ù���ʱ����������������ǣ� ��
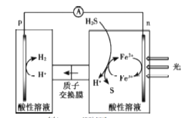
A.p�缫�ĵ缫��Ӧ��2H++2e-=H2
B.�÷�����ʵ����H2S��Ч����S��H2
C.���պ�n�缫�ĵ缫��Ӧ��H2S-2e-=2H++S
D.����Fe3+/Fe2+�⣬I3-/I-Ҳ��ʵ����ͼ��ʾѭ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com