
【题目】下列图示与对应的叙述正确的是( )
A.图甲表示相同温度下,在不同容积的容器中进行反应2BaO2(s)![]() 2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(s)+O2(g),O2的平衡浓度与容器容积的关系
B.图乙表示2NO2(g)![]() N2O4(g)中反应物与生成物的浓度随时间的变化,且在t1时刻达到平衡
N2O4(g)中反应物与生成物的浓度随时间的变化,且在t1时刻达到平衡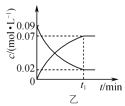
C.图丙表示向0.1mol·L-1NH4Cl溶液中滴加0.1mol·L-1盐酸时,溶液中![]() 随盐酸体积的变化关系
随盐酸体积的变化关系
D.图丁表示向pH、体积均相同的HCl、CH3COOH溶液中分别加入过量锌粉,产生的H2体积随时间的变化,其中曲线a表示HCl溶液
【答案】A
【解析】
A.反应2BaO2(s)![]() 2BaO(s)+O2(g)中,只有一种物质(O2)是气体,平衡常数为K=c(O2),平衡常数只与温度有关,温度不变,K不变,即c(O2)不变,A正确;
2BaO(s)+O2(g)中,只有一种物质(O2)是气体,平衡常数为K=c(O2),平衡常数只与温度有关,温度不变,K不变,即c(O2)不变,A正确;
B.反应2NO2(g)![]() N2O4(g)的系数比是2:1,理论上物质浓度的变化量之比等于系数比,从图中可以看出,NO2的减少量为0.05mol/L,N2O4的增加量为0.07mol/L,比例不是2:1,B错误;
N2O4(g)的系数比是2:1,理论上物质浓度的变化量之比等于系数比,从图中可以看出,NO2的减少量为0.05mol/L,N2O4的增加量为0.07mol/L,比例不是2:1,B错误;
C.NH4Cl溶液中有水解平衡:NH4++H2O ![]() NH3H2O+H+,加入HCl后
NH3H2O+H+,加入HCl后![]() 增大,平衡左移,
增大,平衡左移,![]() 减小,所以
减小,所以![]() 增大,C错误;
增大,C错误;
D.pH、体积均相同的HCl、CH3COOH溶液中,CH3COOH溶液的浓度大,放出的H2总量多。由于有大量CH3COOH分子没有电离,随着反应的进行,CH3COOH ![]() CH3COO-+H+,平衡右移,溶液中H+得到补充,反应速率比HCl快,因此曲线a表示CH3COOH溶液,曲线b表示HCl溶液,D错误;
CH3COO-+H+,平衡右移,溶液中H+得到补充,反应速率比HCl快,因此曲线a表示CH3COOH溶液,曲线b表示HCl溶液,D错误;
故选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.按要求填空
(1)5.4gH2O物质的量为____________mol,约含有___________________个原子;
(2)已知1.204×1023个X气体的质量是6.4g。则X气体的摩尔质量是_________ g/mol;
(3)同温同压下,同体积的甲烷CH4和CO2质量之比为________,质子数之比_______;
(4)VLAl2(SO4)3溶液中含Al3+ag,该Al2(SO4)3溶液的物质的量浓度为_____mol/L,取出![]() L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是_____mol/L。
L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是_____mol/L。
Ⅱ.按要求书写下列反应的方程式
(1)亚硫酸氢钠电离方程式(NaHSO3)________________________________________________;
(2)醋酸溶液与NaHCO3溶液反应的离子方程式为________________________________;
(3)0.8molL﹣1NaHSO4与0.4molL﹣1Ba(OH)2溶液等体积混合,反应的离子方程式为___________;
(4)黑火药爆炸的化学方程式为________________________________。
Ⅲ.请配平以下化学方程式
(1)____FeSO4+____K2O2+____H2O =____ Fe(OH) 3+____ Fe2(SO4) 3+____KOH
(2)_____BiO3-+_____Mn2++____=_____Bi3++_____ MnO4- +____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验课上,老师要求学生用硫酸铜溶液与氢氧化钠溶液制备Cu(OH)2,为了缩短实验时间,老师让学生将反应容器放在沸水浴中进行反应,结果出现了如下两种不同的实验现象:
操作 | 现象 | |
实验一 | 向NaOH溶液中滴加CuSO4溶液 | 黑色沉淀 |
实验二 | 向CuSO4溶液中滴加NaOH溶液 | 蓝色沉淀 |
(1)甲同学认为实验一中产生的黑色沉淀是___(填化学式),理由是___。
(2)为验证推测结果是否正确,甲同学将黑色沉淀过滤、洗涤、干燥后称得质量为ag,并按照如图所示装置进行实验,实验前后称得干燥管E的质量分别为cg和dg。

为确保实验的准确性,甲同学认为应在装置A反应一段时间后再接上装置E,点燃D中的酒精灯,其理由是___。乙同学认为甲同学的装置仍有不足,应在E的末端连接一个气囊,气囊的作用有两个:___。甲同学改进实验装置后完成实验,若a、c、d满足关系式:___,则证明甲同学对黑色沉淀的推测是正确的。
(3)丙同学认为实验二中的蓝色沉淀应为Cu(OH)2,丁同学立即提出反对意见,认为该蓝色沉淀一定不是Cu(OH)2。为确认实验二中蓝色沉淀的成分,丁同学从实验时药品的加入顺序考虑,可能是反应物的用量不同导致产物的不同,并上网查阅资料知,当NaOH溶液少量时会生成碱式硫酸铜[Cu2(OH)2SO4],反应的离子方程式为___。
(4)进一步查阅资料可知碱式硫酸铜为蓝色物质,难溶于水、可溶于酸。请你设计实验,验证实验二中生成的蓝色沉淀含有SO42-:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CH3CH=CH2、NH3、O2为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的化学方程式分别为:反应Ⅰ.2C3H6+2NH3+3O2![]() 2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2
2C3H3N(g)+6H2O(g);反应Ⅱ.C3H6+O2![]() C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与
C3H4O(g)+H2O(g)。反应相同时间,丙烯腈产率与反应温度的关系如图a所示,丙烯腈和丙烯醛的平衡产率与![]() 的关系如图b所示。下列说法正确的是(丙烯腈的选择性=
的关系如图b所示。下列说法正确的是(丙烯腈的选择性=![]() ×100%)( )
×100%)( )
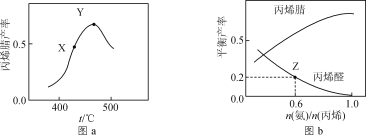
A.其他条件不变,增大压强有利于提高丙烯腈平衡产率
B.图a中X点所示条件下,延长反应时间能提高丙烯腈产率
C.图a中Y点所示条件下,改用对丙烯腈选择性更好的催化剂能提高丙烯腈产率
D.由图b中Z点可知,该温度下反应Ⅱ的平衡常数为K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同质量的氢气、甲烷(CH4)、水,其中含分子数最多的是________;等物质的量的三种物质含氢原子最多的是________。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92 g该氧化物的体积为448 mL,则该氧化物的物质的量为______,该氧化物的摩尔质量为______。
(3)某化学兴趣小组对某品牌矿泉水进行检测时,发现1.0 L该矿泉水中含有45.6 mg Mg2+,Mg2+的物质的量浓度为______。
(4)现有0.1 mol·L-1 Na2SO4和0.3 mol·L-1 H2SO4的混合溶液100 mL,向其中逐滴加入0.2 mol·L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。(忽略混合过程中的体积变化)
①当加入50 mL Ba(OH)2溶液时,所得溶液中SO42-离子的物质的量浓度为________mol·L-1。
②当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌。“一滴香”的分子结构如图所示,下列说法正确的是

A. 该有机物分子式为:C7H10O3
B. 该有机物所有质子可能在同—平面
C. 该有机物能发生取代、加成、氧化、还原反应
D. 该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“摩尔盐”是分析化学中的重要试剂,化学式为(NH4)2Fe(SO4)2·6H2O。“摩尔盐”在一定条件下分解的方程式为:4[(NH4)2Fe(SO4)2·6H2O] ![]() 2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
2Fe2O3+3SO3+5SO2↑+N2↑+6NH3↑+31H2O。回答下列问题:
(1)铁元素在元素周期表中的位置为_____,其价层电子排布图为________。
(2)组成“摩尔盐”的非金属元素中第一电离能最大的元素为________。“摩尔盐”的分解产物中属于非极性分子的化合物是________。
(3)NH3 的沸点比N2O 的沸点_____(填“高”或“低”),其主要原因是________________。
(4)K3[Fe(CN)6]常用于检验Fe2+,K3[Fe(CN)6]中除了离子键以外还存在的化学键为_______,与CN- 互为等电子体的单质的分子式为________。HCN 分子中σ键和π键的个数之比为________。
(5)FeO 晶胞结构如下图所示,FeO 晶体中Fe2+配位数为______,若该晶胞边长为acm,则该晶胞密度为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂电池具有能量密度大、质量轻、寿命长等诸多优点,被广泛应用于移动电话、笔记本电脑中。从某锂电池废料(主要成分为LiMn2O4,杂质为Fe、Cu等)中分离得到Li2SO4、MnCO3的一种工艺流程如图所示:

回答下列问题:
(1)研磨锂电池废料的主要目的是___________________。
(2)滤渣Ⅰ的主要成分为MnO2,写出向浆液中通入SO2发生反应的化学方程式:___________________。
(3)滤液Ⅰ中的金属阳离子有Cu2+、Fe3+和Li+,向滤液Ⅰ中加入氧化铜粉末的目的是___________________;向滤液Ⅱ中通入H2S发生反应的离子方程式为___________________。
(4)滤液Ⅲ经过操作Ⅰ后可得到Li2SO4,其中操作Ⅰ主要包括_____、_____、过滤、洗涤、干燥;在实验室中检验Li2SO4晶体是否洗涤干净的方法是__________。
(5)写出向MnSO4溶液中加入NH4HCO3生成MnCO3的化学方程式:___________________。
(6)现取18.1g该锂电池废料(LiMn2O4的质量分数为80.0%)模拟以上工艺流程进行实验,最终得到16.2gMnCO3,该实验中产率为_____(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下列各图示中不能较长时间看到Fe(OH)2白色沉淀的是________(填序号)。

II.ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2,成为自来水的消毒剂。已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与氯气反应:2NaClO2+Cl2=2ClO2+2NaCl。下图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略)。其中E中盛有CCl4液体(用于除去ClO2中的未反应的Cl2)。

(1)仪器P的名称是________________。
(2)写出装置A中烧瓶内发生反应的离子方程式:______________________________。
(3)B装置中所盛试剂是________________。
(4)F为ClO2收集装置,应选用的装置是________(填序号),其中与E装置导管相连的导管口是________(填接口字母)。

III.如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。

现欲用该浓硫酸配制成1mol/L的稀硫酸,现实验室仅需要这种稀硫酸220mL。试回答下列问题:
(1)用量筒量取该浓硫酸____________mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是____。
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是__________。
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,仰视容量瓶刻度线
(4)某同学用固体Na2CO3配制500 mlL 0.1molL-1溶液的过程如图所示:

你认为该同学的错误步骤有__________处。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com