
【题目】将物质的量均为a mol的钠和铝一同投入m g足量的水中,所得溶液的密度为ρg/cm3,则此溶液的物质的量浓度为 ( )
A.1000aρ / (50a+m) mol/L B.aρ / (46a+m) mol/L
C.1000aρ / (46a+m) mol/L D.1000aρ / (47a+m) mol/L
【答案】C
【解析】
试题分析:钠和铝投入足量水中发生反应:2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由方程式可知,amol的钠反应生成amol氢氧化钠,生成氢气0.5amol;amol氢氧化钠与amol铝恰好反应生成amol偏铝酸钠,同时生成氢气1.5amol.溶液为偏铝酸钠溶液。所以氢气的质量为(0.5amol+1.5amol)×2g/mol=4ag;所以溶液质量m(溶液)=m(金属)+m(H2O)-m(H2)=amol×23g/mol+amol×27g/mol+mg-4ag=(46a+m)g,所以溶液的体积为![]() =
=![]() mL,所以溶液的物质的量浓度为
mL,所以溶液的物质的量浓度为 =
=![]() mol/L,故选C。
mol/L,故选C。


科目:高中化学 来源: 题型:
【题目】【化学选修3:物质结构与性质】铝、铁在生活、生产中有着广泛的用途,请回答下列问题。
(1)Fe2+的最外层电子排布式____________。元素Fe与Mn的第三电离能分别为I3(Fe)、I3(Mn),则I3(Fe)______I3(Mn)(填“>”、“<")。
(2)第四周期中,与Al原子未成对电子数相同的金属元素有____种。气态氯化铝的分子组成为(AlCl3)2,其中Al、Cl均达8e-稳定结构,Al原子的杂化方式为__________。根据等电子原理,AlO2-的空间构型为_____。
(3)Fe(CO)5的熔点为-20℃,沸点为103℃,易溶于乙醚,其晶体类型为______,晶体中σ键和π键的数目之比为______。
(4)科学家们发现某些含铁的物质可催化尿素合成肼(N2H4),沸点:N2H4>C2H6的主要原因为____________。
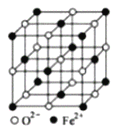
(5)FeO晶体的晶胞如图所示,己知:FeO晶体的密度为ρg/cm3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-最短核间距为______pm(用ρ和NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
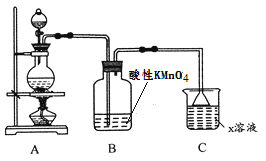
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为_____________________。
(2)C装置的作用___________________。
(3)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是_______________。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为_______。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、Al2O3及不溶于强酸的SiO2)可制备Fe2O3。①用稀盐酸浸取炉渣,过滤;②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
a.除去Al3+的离子方程式是______________________________。
b.步骤②中滤液氧化的目的是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平.现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
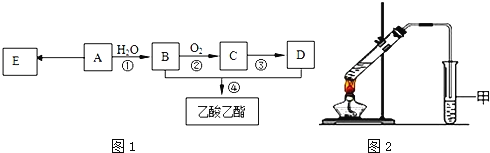
(1)A分子中官能团的名称是______,D中官能团的名称是______;反应①的反应类型是______反应.
(2)反应②的化学方程式是______,反应④的化学方程式是______.
(3)E是常见的高分子材料,合成E的化学方程式是______.
(4)某同学用如图2所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体.
①实验开始时,试管甲中的导管不伸入液面下的目的是______.
②上述实验中饱和碳酸钠溶液的作用是(填字母)______.
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.加速酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第ⅢA族),它们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子的电子排布式____________。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是______________;
②写出Al2Cl6分子的结构式_______________;
③单分子A1Cl3的立体构型是__________,缔合双分子Al2Cl6中Al原子的轨道杂化类型是_______。
(3)晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图),若其中有两个原子为10B,其余为11B,则该结构单元有____________种不同的结构类型。

(4)金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm3,计算确定其晶胞的类型(简单、体心或面心立方)________________;晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A只含有C、H、O三种元素,常用作有机合成的中间体。16.8 g该有机物燃烧生成44.0 g CO2和14.4 g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O—H键和位于分子端的C≡C键,核磁共振氢谱上有三个峰,峰面积之比为6∶1∶1。
(1)A的分子式是____________。
(2)下列物质中,一定条件下能与A发生反应的是_________________。
A.H2B.Na C.酸性KMnO4溶液 D.Br2
(3)A的结构简式是________________________。
(4)有机物B是A的同分异构体,1 mol B可与1 mol Br2加成。该有机物中所有碳原子在同一个平面上,没有顺反异构现象。B的结构简式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是国内外允许使用的一种食品添加剂,在食品工业中发挥着护色、防腐、漂白和抗氧化的作用。我国对于SO2的添加量有明确规定(如图所示)。

某研究小组用图装置对市售黄花菜中的SO2进行测定。其中,溶液X为黄花菜进行充分浸泡后所得浅黄色浸泡液,Y为加入的试剂。(Y的浓度及体积均未标出)查阅资料发现,在水溶液中正四价硫元素主要以SO32-形式存在,且SO2与SO32-化学性质相似。因此,该小组同学将SO2的测定问题转化为溶液中SO32-的测定。
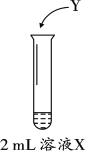
(1)结合化学知识解释浸泡液X中存在SO32-的原因是______。
(2)甲同学预测可用Na2S溶液验证X中是否含有SO32-,该预测应用的是Na2S的______性。查阅资料发现该反应较为复杂,因此未做进一步验证。
(3)乙同学为验证X中是否含有SO32-,进行了实验i:
实验序号 | 试剂Y | 现象 |
i | 酸性KMnO4溶液 | ① |
根据实验i 的现象得出结论:X中含有SO32-。实验i的现象是________,SO32-在反应后转化为_________。
(4)丙同学认为也可以用H2O2溶液来验证X中是否含有SO32-,进行了实验ii:
实验序号 | 操作 | 现象 |
ii | a.向X中加入适量H2O2溶液,振荡 | 无明显现象 |
b.继续滴加 ,振荡 | 无明显现象 | |
c.再滴加 ,振荡 | 白色沉淀 |
通过实验ii可证明X中含有SO32-,写出操作b、c中滴加试剂的化学式____、 _____ 。
(5)丁同学认为丙的实验方案不严谨,设计了对比实验ⅲ,证明了X中含有SO32-。实验ⅲ的方案是(从操作、现象、结论方面描述)________ 。
(6)为测定市售黄花菜中SO2含量,进行实验ⅳ:
实验序号 | 操作 |
ⅳ | a.将50克黄花菜研碎,用一定浓度氢氧化钠溶液浸泡; b.加稀硫酸酸化; c.加入淀粉指示剂; d.用浓度为0.01mol/L的I2溶液滴定,消耗0.01mol/L的I2溶液5.00 mL。 |
查阅资料发现:碘元素的常见价态有-1,0,+1,+3,+5,+7。
① 将黄花菜用氢氧化钠溶液浸泡的目的是(用化学方程式表示)__________。
② 写出滴定反应的化学方程式____________。
③ 该市售黄花菜中SO2残留量是________毫克/千克。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时。有c(CH3COOH)+ c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液,c(CH3COOH)、c(CH3COO-) 与pH的关系如图所示。下列有关溶液的叙述不正确的是。
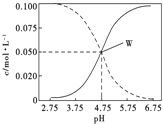
A. pH=5.5的溶液中c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B. 溶液中:c(H+)+ c(Na+)=c(CH3COO-)+c(OH-)
C. 由W点可以求出25℃时CH3COOH的电离常数
D. pH=4的溶液中: c(H+)+ c(Na+)+c(CH3COOH)=0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某香料I的一种合成路线如下:

回答下列问题:
(1)C的名称为______________;H所含官能团名称是______________。
(2)B→C的反应类型是______________;写出I的结构简式:______________。
(3)G分子最多有______________个原子共平面。
(4)写出A→B的化学方程式:____________________________。
(5)J是I的同分异构体,同时满足下列条件的J的结构有_______种。其中,一种核磁共振氢谱有6个峰且峰的面积之比为1∶1∶1∶2∶2∶3的结构简式为______________。
①能使溴的四氯化碳溶液褪色
②能与碳酸氢钠溶液反应产生CO2
③属于芳香族化合物,且苯环上的一氯代物只有2种
(6)参照上述流程,以乙烯和OHC-CHO为原料合成HOOCCH=CHCOOH,设计合成路线:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com