
����Ŀ��SO2�ǹ���������ʹ�õ�һ��ʳƷ���Ӽ�����ʳƷ��ҵ�з����Ż�ɫ��������Ư�Ϳ����������á��ҹ�����SO2������������ȷ�涨(��ͼ��ʾ)��

ij�о�С����ͼװ�ö����ۻƻ����е�SO2���вⶨ�����У���ҺXΪ�ƻ��˽��г�ֽ��ݺ�����dz��ɫ����Һ��YΪ������Լ���(Y��Ũ�ȼ������δ���)�������Ϸ��֣���ˮ��Һ�����ļ���Ԫ����Ҫ��SO32-��ʽ���ڣ���SO2��SO32-��ѧ�������ơ���ˣ���С��ͬѧ��SO2�IJⶨ����ת��Ϊ��Һ��SO32-�IJⶨ��
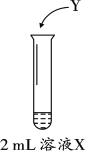
(1)��ϻ�ѧ֪ʶ���ͽ���ҺX�д���SO32-��ԭ����______��
(2)��ͬѧԤ�����Na2S��Һ��֤X���Ƿ���SO32-����Ԥ��Ӧ�õ���Na2S��______�ԡ��������Ϸ��ָ÷�Ӧ��Ϊ���ӣ����δ����һ����֤��
(3)��ͬѧΪ��֤X���Ƿ���SO32-��������ʵ��i��
ʵ����� | �Լ�Y | ���� |
i | ����KMnO4��Һ | �� |
����ʵ��i ������ó����ۣ�X�к���SO32-��ʵ��i��������________��SO32-�ڷ�Ӧ��ת��Ϊ_________��
(4)��ͬѧ��ΪҲ������H2O2��Һ����֤X���Ƿ���SO32-��������ʵ��ii��
ʵ����� | ���� | ���� |
ii | a����X�м�������H2O2��Һ���� | ���������� |
b�������μ� ���� | ���������� | |
c���ٵμ� ���� | ��ɫ���� |
ͨ��ʵ��ii��֤��X�к���SO32-��д������b��c�еμ��Լ��Ļ�ѧʽ____�� _____ ��
(5)��ͬѧ��Ϊ����ʵ�鷽�����Ͻ�������˶Ա�ʵ������֤����X�к���SO32-��ʵ�����ķ�����(�Ӳ����������۷�������)________ ��
(6)Ϊ�ⶨ���ۻƻ�����SO2����������ʵ������
ʵ����� | ���� |
�� | a����50�˻ƻ������飬��һ��Ũ������������Һ������ b����ϡ�����ữ�� c���������ָʾ���� d����Ũ��Ϊ0.01mol/L��I2��Һ�ζ�������0.01mol/L��I2��Һ5.00 mL�� |
�������Ϸ��֣���Ԫ�صij�����̬��-1��0��+1��+3��+5��+7��
�� ���ƻ���������������Һ���ݵ�Ŀ����(�û�ѧ����ʽ��ʾ)__________��
�� д���ζ���Ӧ�Ļ�ѧ����ʽ____________��
�� �����ۻƻ�����SO2��������________����/ǧ�ˡ�
���𰸡�SO2��H2O��Ӧ����H2SO3, H2SO3�ɵ������H+��SO32- ��ԭ ��ɫ SO42- ���� BaCl2��Һ ȡ��ҺX���μ����ᣬ�ٵμ��Ȼ�����Һ����������ɫ���������ʵ������֤��X����SO32- SO2+2NaOH = Na2SO3+H2O Na2SO3+I2+H2O=Na2SO4+2HI 64
��������
(1)����ҺX�д���SO32-��ԭ����SO2��H2O��Ӧ����H2SO3, H2SO3�ɵ������H+��SO32-��
(2)��ΪNa2S��SO32-���Է�����Ӧ��2S2-+ SO32-+6H+=3S![]() +3H2O���÷�Ӧ��Na2S����ԭ�����𰸣���ԭ����
+3H2O���÷�Ӧ��Na2S����ԭ�����𰸣���ԭ����
��3��X�к��е�SO32-���������ԣ����л�ԭ�ԣ�����������KMnO4��Һ��Ӧ����Һ����ɫ�������ķ�ӦΪ5SO32-+ 2MnO4-+6H+=5 SO42-+2 Mn2++3H2O��SO32-�ڷ�Ӧ��ת��ΪSO42-;�𰸣���ɫ��SO42-��
(4) X�к���SO32-����������H2O2��Һ������ӦΪ��SO32- +H2O2= SO42-+H2O,������Һ�м���ϡ���ᣬû�з�Ӧ�������ټ�BaCl2��Һ���ɰ�ɫ�������������Բ���b��c�еμӵ��Լ�Ϊ�����BaCl2��Һ���𰸣����� �� BaCl2��Һ��
(5)��ͬѧ��Ϊ����ʵ�鷽�����Ͻ�������˶Ա�ʵ������֤����X�к���SO32-��ʵ�����ķ�������ȡ��ҺX���μ����ᣬ�ٵμ��Ȼ�����Һ����������ɫ���������ʵ������֤��X����SO32- ��
(6)�� ���ƻ���������������Һ������Ϊ�˳�ȥ�ƻ�����SO2 ����Ӧ�Ļ�ѧ����ʽ��SO2+2NaOH = Na2SO3+H2O���𰸣�SO2+2NaOH = Na2SO3+H2O��
����Ũ��Ϊ0.01mol/L��I2��Һ�ζ����ۻƻ����е���ȡҺ���ζ���Ӧ�Ļ�ѧ����ʽ��Na2SO3+I2+H2O=Na2SO4+2HI���𰸣�Na2SO3+I2+H2O=Na2SO4+2HI��
����Ũ��Ϊ0.01mol/L��I2��Һ�ζ�������0.01mol/L��I2��Һ5.00 mL����Ϸ�Ӧ����ʽ��Na2SO3+I2+H2O=Na2SO4+2HI��n(SO2)=n (Na2SO3)=n(I2)= 0.01mol/L![]() /1000mL
/1000mL![]() L-1=5
L-1=5![]() 10-5mol,���ۻƻ�����SO2����������5
10-5mol,���ۻƻ�����SO2����������5![]() 10-5mol
10-5mol![]() 64g/mol=3.2
64g/mol=3.2![]() 10-3g���������ۻƻ�����SO2����=��3.2
10-3g���������ۻƻ�����SO2����=��3.2![]() 10-3g
10-3g![]() 1000��
1000��![]() 50/1000=64����/ǧ��;�𰸣�64��
50/1000=64����/ǧ��;�𰸣�64��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50 mL 18 mol��L��1��H2SO4��Һ�м���������ͭƬ�����ȡ���ַ�Ӧ����ԭ��H2SO4�����ʵ����� ��
A. ��0.45 mol B. ����0.45 mol
C. ��0.45��0.90 mol֮�� D. ����0.45 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣��ش������й����⣺
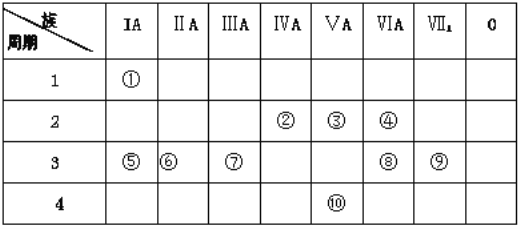
(1)��������Ԫ���зǽ����Խ�ǿ��Ԫ����_________����Ԫ�ط��ű�ʾ������ЩԪ�ص�����������Ӧ��ˮ�����м�����ǿ���� _________ (�ѧʽ)��
(2)д��Ԫ��������ǿ�����Ե��⻯��ĵ���ʽ��_______________��
(3)д��һ�����١��ۡ�������Ԫ���γɵij������ӻ����________________��
(4)�õ���ʽ��ʾ�ޡ����γɻ�����Ĺ��̣�_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�����Ϊa mol���ƺ���һͬͶ��m g������ˮ�У�������Һ���ܶ�Ϊ��g/cm3�������Һ�����ʵ���Ũ��Ϊ ( )
A��1000a�� / (50a+m) mol/L B��a�� / (46a+m) mol/L
C��1000a�� / (46a+m) mol/L D��1000a�� / (47a+m) mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC2H4O2�Ľṹ������![]() ��
��![]() ���֣�Ϊ����ṹ����������������������______________��________________��
���֣�Ϊ����ṹ����������������������______________��________________��
(1)��Ϊ![]() ������������Ӧ����____�������գ��˴Ź���������Ӧ����_____���塣
������������Ӧ����____�������գ��˴Ź���������Ӧ����_____���塣
(2)��Ϊ![]() ��������������______�������գ��˴Ź���������Ӧ��______���塣
��������������______�������գ��˴Ź���������Ӧ��______���塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������C��H��O���л���3.24 gװ��Ԫ�ط���װ�ã�ͨ��������O2ʹ֮��ȫȼ�գ������ɵ���������ͨ��CaCl2��(A)�ͼ�ʯ��(B)�����A������������2.16 g��B��������9.24 g����֪���л������Է�������Ϊ108��
(1)ȼ�մ��л���3.24 g������O2����g��
(2)����л���ķ���ʽ��
(3)���л���1��������1����������д������ͬ���칹��Ľṹ��ʽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й���Ũ�������Ե���������ȷ����
A. Ũ���������ˮ�ԡ���ˮ�Ժ�ǿ�����Ե�����
B. Ũ���������������е�ˮ�����������������������������ĸ����
C. Ũ����������չ����е�ʪ��ˮ���ᾧˮ�����еĽᾧˮ
D. �ڷ�ӦC12H22O11![]() 12C��11H2O��Ũ��������ˮ��
12C��11H2O��Ũ��������ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Li4Ti5O12��LiFePO4��������ӵ�صĵ缫���ϣ���������������Ҫ�ɷ�ΪFeTiO3������������MgO��SiO2�����ʣ����Ʊ��������������£�

�ش��������⣺
��1������1Ϊ_______________������AΪ_________________������Һ���м���˫��ˮ��������___________________________________��
��2���������������Ҫ��TiOCl42����ʽ���ڣ�д����Ӧ��Ӧ�����ӷ���ʽ__________��
��3��TiO2��xH2O������˫��ˮ����ˮ��Ӧ40 min����ʵ�������±���ʾ��
�¶�/�� | 30 | 35 | 40 | 45 | 50 |
TiO2��xH2Oת����% | 92 | 95 | 97 | 93 | 88 |
����40��ʱTiO2��xH2Oת������ߵ�ԭ��_______________________________��
��4��������Һ�ڡ���c(Mg2+)=0.02 mol/L������˫��ˮ�����ᣨ����Һ�������1������ʹFe3+ǡ�ó�����ȫ����Һ��c(Fe3+)=1��10-5 mol/L����ʱ�Ƿ���Mg3(PO4)2�������ɣ�_____________________________________________����ʽ���㣩��FePO4��Mg3(PO4)2��Ksp�ֱ�Ϊ1.3��10-22��1.0��10-24��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ̼��þ�ͼ�ʽ̼����þ������Ϊ�������ϡ�������ʯ��ȡ��ʽ̼��þ��ʵ�鲽�����£�
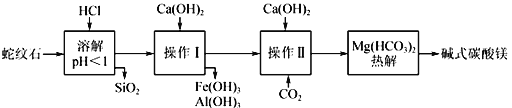
������ʯ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ�
��1������ʵ���У�����ѭ��ʹ�õ�������______���ѧʽ����
��2���������е�Ca(OH)2Ҫ��������ԭ����____________________________��
��3��д��������������Mg(HCO3)2�Ļ�ѧ����ʽ��____________________________________��
��4��Ϊȷ����ʽ̼����þ[MgaAlb(OH)c(CO3)d��xH2O]����ɣ���������ʵ�飺��ȷ��ȡ5.085 g��Ʒ������ϡ�����ַ�Ӧ������CO2 0.840 L���ѻ���ɱ�״���£�������ȡһ������Ʒ�ڿ����м��ȣ���Ʒ�Ĺ�������ʣ�������Ʒ��ʣ������/������Ʒ����ʼ������100%)���¶ȵı仯��ͼ��ʾ(��Ʒ��270��ʱ����ȫʧȥ�ᾧˮ��600 �����ϲ�������Ϊ����������Ļ�����
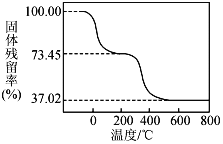
��������ʵ�����ݼ���5.085 g��ʽ̼����þ��Ʒ�е�n(OH-)��д��������̣�_______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com