
【题目】Ⅰ.宜城市鄂西化工厂以铬铁矿(主要成分为 FeO 和 Cr2O3,含有 Al2O3、SiO2 等杂质)为主要原料生产化工原料红矾钠(主要成分 Na2Cr2O7·2H2O),工艺流程如下图:
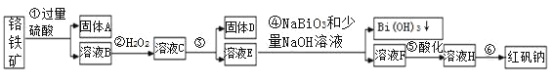
i.常温,NaBiO3不溶于水,有强氧化性,碱性条件下,能将Cr3+转化为 CrO42-。ii.
金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
开始沉淀的pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
沉淀完全的pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
(1)步骤③需加氢氧化钠溶液,此时pH要调到5的目的是__________________。
(2)写出④反应的离子方程式____________________________________。
(3)将溶液 H 经过蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠粗晶体,精制红矾钠粗晶体需要采用的操作是______________(填操作名称)。
Ⅱ.经检测鄂西化工厂的工业废水中含 5.00×10-3 mol·L-1 的 Cr2O72-,其毒性较大。该化工厂的科研人员为了变废为宝,将废水处理得到磁性材料 Cr0.5Fe1.5FeO4(Fe 的化合价依次为+3、+2),又设计了如下工艺流程:
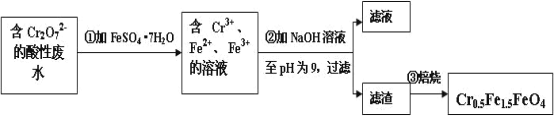
(1)第①步反应的离子方程式是_________________________________________。
(2)欲使 1L 该废水中的 Cr2O72-完全转化为 Cr0.5Fe1.5FeO4。理论上需要加入FeSO4·7H2O的质量为_________g (已知 FeSO4·7H2O 的摩尔质量为 278 g/mol)。
【答案】使 Fe3+、Al3+均完全转化为 Fe(OH)3 和 Al(OH)3 沉淀而除去 3NaBiO3+2Cr3+ +7OH-+H2O=3Bi(OH)3+2CrO42-+3Na+ 重结晶 Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O 13.9
【解析】
I.由流程图可知,铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)加过量硫酸FeO、Cr2O3和Al2O3都溶解,SiO2不溶,经过滤分离得到固体A和溶液B,则固体A为SiO2;溶液B中含有Fe2+、Al3+、Cr3+,加入H2O2目的是将Fe2+氧化为Fe3+,第③步是调溶液pH,使Fe3+形成氢氧化铁沉淀,同时Al3+变成氢氧化铝沉淀而除去,固体D为氢氧化铁和氢氧化铝混合物;第④步加入NaBiO3和少量NaOH溶液将Cr3+转化为CrO42-;第⑤步中酸化是使CrO42-转化为Cr2O72-;第⑥步经蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠
Ⅱ.(1)第①步反应中Cr2O72-在酸性条件下将Fe2+氧化为Fe3+,自身被还原为Cr3+;
(2)根据Cr原子计算Cr0.5Fe1.5FeO4的物质的量,结合Cr0.5Fe1.5FeO4的物质的量利用Fe原子守恒计算FeSO4·7H2O质量。
(1)从氢氧化物形成沉淀的pH表格可知,③为加入物质来调节溶液的pH,使 Fe3+、Al3+均完全转化为 Fe(OH)3 和 Al(OH)3 沉淀而除去;
(2)常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-,则反应④的离子方程式为3NaBiO3+2Cr3++7OH-+H2O=2CrO42-+3Na++3Bi(OH)3↓;
(3)精制红矾钠粗晶体需要采用的操作是重结晶;
Ⅱ.(1)Cr2O72-有较强氧化性,FeSO4·7H2O中Fe2+有一定的还原性,Cr2O72-在酸性条件下将Fe2+氧化为Fe3+,自身被还原为Cr3+,根据守恒元素守恒及所处环境可知,还应有水生成,反应离子方程式为Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O;
(2)1 L废水中含n(Cr2O72-)=5.00×10-3 mol.根据Cr原子、Fe原子守恒,可得:
Cr2O72-~4Cr0.5Fe1.5FeO4~10FeSO4·7H2O,
所以理论上n(FeSO4·7H2O)=10n(Cr2O72-)=5.00×10-3 mol×10=0.05 mol,
所以m(FeSO4·7H2O)=0.05 mol×278 g·mol-1=13.9 g。


科目:高中化学 来源: 题型:
【题目】常见有机物A、B、C、D、E、G间的转化关系如下图所示(以下变化中,某些反应条件及产物未标明)。B是天然有机高分子化合物,C、D可发生银镜反应,在相同条件下,G蒸气密度是氦气的22倍。
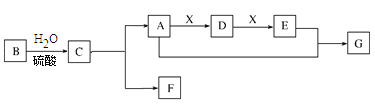
(1)B的分子式为_____、G、的结构简式为_____。
(2)E中官能团的名称_____。
(3)A的同分异构体的结构简式_____。
(4)A→D反应的化学方程式:_____、其反应类型是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在调节好pH和Fe2+浓度的废水中加H2O2,能氧化降解污染物。现用该方法降解污染物p-CP,控制H2O2、Fe2+和p-CP的初始浓度相同,设计如下对比实验探究温度、pH对该降解反应速率的影响,测得p-CP的浓度随时间变化的关系如下图。
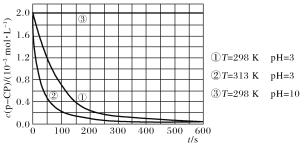
下列结论或推断不正确的是( )
A.实验①、②表明适当升高温度,降解反应速率增大
B.根据推断,在原来条件下适当升高温度和调高pH,p-CP的分解速率可能保持不变
C.313 K、pH=3时,在0~100 s内,p-CP的分解平均速率约为1.8×10-2mol·L-1·s-1
D.室温下调节溶液pH=10,可使催化剂失去活性, p-CP几乎不分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某纯碱样品含有少量![]() 杂质,某兴趣小组用如图所示装置测定纯碱样品中
杂质,某兴趣小组用如图所示装置测定纯碱样品中![]() 的质量分数(铁架台、铁夹等均已略去)。
的质量分数(铁架台、铁夹等均已略去)。
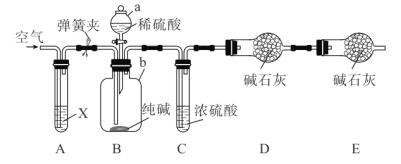
实验步骤如下:
Ⅰ.按图连接装置,并检查气密性;
Ⅱ.准确称量盛有碱石灰的干燥管![]() 的质量为
的质量为![]() ;
;
Ⅲ.准确称量![]() 纯碱样品放入容器
纯碱样品放入容器![]() 中;
中;
Ⅳ.打开分液漏斗![]() 的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
Ⅴ.打开弹簧夹,往试管![]() 中缓缓鼓入空气数分钟,最后称得干燥管
中缓缓鼓入空气数分钟,最后称得干燥管![]() 的质量为
的质量为![]() 。
。
请回答下列问题:
(1)检查装置![]() 气密性的方法为____________。
气密性的方法为____________。
(2)装置![]() 中试剂
中试剂![]() 应选择_____,目的是________。
应选择_____,目的是________。
(3)装置![]() 的作用是____,步骤
的作用是____,步骤![]() 中“缓缓鼓入空气数分钟”的目的是____________。
中“缓缓鼓入空气数分钟”的目的是____________。
(4)根据实验中测得的有关数据,计算纯碱样品![]() 的质量分数为___(保留三位有效数字),若没有装置
的质量分数为___(保留三位有效数字),若没有装置![]() ,会导致测量结果____(填“偏大”“偏小”或“无影响”)。
,会导致测量结果____(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图六个操作是常见物质的分离提纯操作,则有关这的说法不正确的是


A. 操作1、操作2、操作6都可以是蒸馏,也可以是蒸发
B. 操作2可以是蒸发浓缩、冷却结晶、过滤
C. 操作3可以是洗剂、干燥
D. 操作4、操作5分别是萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA 表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,0. 1mol Cl2 溶于水,转移的电子数目为0. 1NA
B.常温常压下,18g H2O 中含有的原子总数为3NA
C.标准状况下,11. 2L CCl4中含有的分子数目为0. 5NA
D.常温常压下,2. 24L CO 和CO2 混合气体中含有的碳原子数目为0. 1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
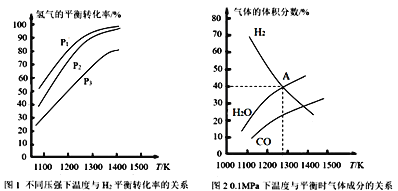
(1)该反应的平衡常数表达式为K=___。
(2)由图1可知,该反应ΔH__0(填“>”或“<”),p1、p2、p3由大到小的顺序为___。
(3)由图2可知,A点时H2的平衡转化率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)北京奥运会祥云火炬将中国传统文化、奥运精神以及现代高科技融为一体。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“” ___。
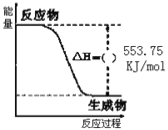
②写出表示丙烷燃烧热的热化学方程式:___。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___。
(2)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)═H2O(l) △H1=Q1kJ/mol
C2H5OH(g)═C2H5OH(l) △H2=Q2kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g) △H3=Q3kJ/mol
若使23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为___kJ。
②碳(s)在氧气供应不充分时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+![]() O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有___。
O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com