
����Ŀ���ڵ��ں�pH��Fe2��Ũ�ȵķ�ˮ�м�H2O2��������������Ⱦ����ø÷���������Ⱦ��p��CP������H2O2��Fe2����p��CP�ij�ʼŨ����ͬ��������¶Ա�ʵ��̽���¶ȡ�pH�Ըý��ⷴӦ���ʵ�Ӱ�죬���p��CP��Ũ����ʱ��仯�Ĺ�ϵ����ͼ��
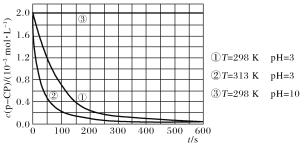
���н��ۻ��ƶϲ���ȷ����(����)
A.ʵ��١��ڱ����ʵ������¶ȣ����ⷴӦ��������
B.�����ƶϣ���ԭ���������ʵ������¶Ⱥ͵���pH��p��CP�ķֽ����ʿ��ܱ��ֲ���
C.313 K��pH��3ʱ����0��100 s�ڣ�p��CP�ķֽ�ƽ������ԼΪ1.8��10��2mol��L��1��s��1
D.�����µ�����ҺpH��10����ʹ����ʧȥ���ԣ� p��CP�������ֽ�
���𰸡�C
��������
A��о������¶ȱ����Է�Ӧ���ʵ�Ӱ�죬�������¶ȸ߷�Ӧʱ��̣��������ʴ�A��ȷ��
B���ͼ��֪����ԭ���������ʵ������¶���ʹ�ֽ�������������pH�ͷֽ����ʣ���p��CP�ķֽ������п�����ԭ�����ϱ��ֲ��䣬��B��ȷ��
C�����ͼ������313 K��pH��3ʱ����0��100 s�ڣ�p��CP�ķֽ�ƽ������ԼΪ1.8��10��5mol��L��1��s��1����C����
D����ߢ۱����ڵ�����ҺpH��10ʱ��p��CP��Ũ�Ȳ��䣬�ֽ����ʼ���Ϊ�㣬��D��ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�����߲ˡ�����Ʒ�и�����ά����C�������ԵĿ�˥�����ã����ױ�����������ij����С�����õ�ζ�����ij��֭��ά����C�ĺ������仯ѧ����ʽ��ͼ��ʾ������˵���в���ȷ����

A.������ӦΪ������ԭ��Ӧ
B.�ζ�ʱ���õ�����Һ��ָʾ��
C.�ζ�ʱӦ��������ƿʹ��Ӧ���
D.����ά����C�ķ���ʽΪC6H6O6
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[KAl(SO4)2��12H2O]���������������й㷺��;������ˮ�ľ�������ֽ��ҵ����ʩ������ʳƷ��ҵ�ķ��ͼ��ȡ������������ķ�����������(��Al��Al2O3������SiO2��FeO��xFe2O3)���Ʊ������������������£��ش��������⣺
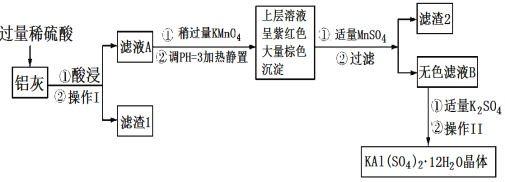
��1��������ˮ��ԭ����______________(�����ӷ���ʽ��ʾ)��
��2����������________��������������Ũ����__________�����ˡ�ϴ�ӡ����
��3��������ҺA���Ƿ����Fe2�����Լ���__________(ֻ��һ���Լ�)��
��4��������Ͷ������������Һ����������Ļ�ѧ����ʽ��__________������ҺA�м��������ط�����Ӧ�����ӷ���ʽΪ(��������MnO4-ת��ΪMn2��)��_______��
��5����֪����pH��3�����������£�MnO4-����Mn2����Ӧ����MnO2������MnSO4������Ӧ�����ӷ���ʽΪ��________������2���е�������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��A��B��C��D��Eԭ��������������A��B���γ�4��10���ӵķ��ӣ�C��Eͬ���壬D��Eͬ���ڣ�C��D���γ����ӻ�����D2C��D2C���������ӵĵ��Ӳ�ṹ��ͬ���ҵ�������Ϊ30��
��ش���������![]() ��Ԫ�ط��ű�ʾ
��Ԫ�ط��ű�ʾ![]() ��
��
��1��Ԫ��A��һ��ͬλ������������������ȣ�����ͬλ�صķ�����______��
��2��Ԫ��B�����ڱ��е�λ����______��
��3��Ԫ��A��B�γ�10���ӵķ��ӣ���ˮ��Һ�ʼ��ԣ��õ��뷽��ʽ��ʾ______��
��4��Ԫ��A��B��C�γɵ�ԭ�Ӹ�����Ϊ4��2��3���Σ�����______![]() ��������������������
��������������������![]() ��������еĻ�ѧ������Ϊ______��
��������еĻ�ѧ������Ϊ______��
��5��Ԫ��C��D�γɻ�����D2C2�ĵ���ʽΪ______������ˮ��Ӧ�����ӷ���ʽΪ______��
��6��Ԫ��C��D��E��F�γɼ����ӵİ뾶��С�����˳��Ϊ______��
��7��Ԫ��E��F��ȣ�Ԫ��ԭ�ӵõ���������ǿ����______�������ӷ���ʽ֤��______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڷ�ӦA(g)+3B(g)2C(g)+2D(g)�����з�Ӧ���������ǣ� ��
A.v(D)=0.30mol��L-1��s-1B.v(A)=0.50mol��L-1��s-1
C.v(B)=0.60mol��L-1��s-1D.v(C)=0.50mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵļ��鷽����ȷ���ǣ� ��
A.����ϡ���ᣬ������ɫ��ζ�����壬����Һ��һ������![]()
B.�ȼ���ˮ���ټ�![]() ��Һ����Һ��ΪѪ��ɫ������Һ��һ������
��Һ����Һ��ΪѪ��ɫ������Һ��һ������![]()
C.�ýྻ�IJ�����պȡ��Һ�ھƾ��������գ�����ʻ�ɫ������Һ��һ������![]()
D.����Һ�м���ϡ���������ԣ������������ټ���![]() ��Һ������ɫ����������Һ�ж�����
��Һ������ɫ����������Һ�ж�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��WΪԭ������������������ֶ�����Ԫ�أ�����ZΪ����Ԫ�أ�X��WΪͬһ����Ԫ�ء�X��Z��W�γɵ����������ֱ�Ϊ�ס��ҡ�����x��y2��z��w�ֱ�ΪX��Y��Z��W�ĵ��ʣ����ǻ������ת����ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��

A.��Ӧ�١�������������ԭ��Ӧ�������ڷ�������ԭ��Ӧ
B.Y�����Ӱ뾶��Z�����Ӱ뾶С
C.��Ӧ�ۿ���֤��X�ķǽ�����ǿ��W
D.һ�������£�x���Ӧ���ɶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����.�˳��ж����������Ը�����(��Ҫ�ɷ�Ϊ FeO �� Cr2O3������ Al2O3��SiO2 ������)Ϊ��Ҫԭ����������ԭ�Ϻ췯��(��Ҫ�ɷ� Na2Cr2O7��2H2O)��������������ͼ��
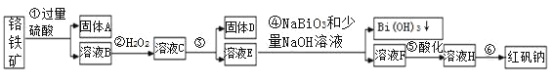
i.���£�NaBiO3������ˮ����ǿ�����ԣ����������£��ܽ�Cr3+ת��Ϊ CrO42����ii��
�������� | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
��ʼ������pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
������ȫ��pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
(1)������������������Һ����ʱpHҪ����5��Ŀ����__________________��
(2)д���ܷ�Ӧ�����ӷ���ʽ____________________________________��
(3)����Һ H ��������Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ����T�ú췯�ƴ־��壬���ƺ췯�ƴ־�����Ҫ���õIJ�����______________(���������)��
��.���������������Ĺ�ҵ��ˮ�к� 5.00��10-3 mol��L-1 �� Cr2O72-���䶾�Խϴû������Ŀ�����ԱΪ�˱��Ϊ��������ˮ�����õ����Բ��� Cr0.5Fe1.5FeO4��Fe �Ļ��ϼ�����Ϊ+3��+2��������������¹������̣�
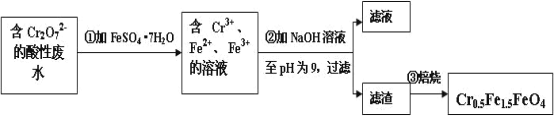
(1)�ڢٲ���Ӧ�����ӷ���ʽ��_________________________________________��
(2)��ʹ 1L �÷�ˮ�е� Cr2O72-��ȫת��Ϊ Cr0.5Fe1.5FeO4����������Ҫ����FeSO4��7H2O������Ϊ_________g (��֪ FeSO4��7H2O ��Ħ������Ϊ 278 g/mol)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019����Ԫ�����ڱ�����150���꣬�ڼ��ѧ��Ϊ�������ڱ������˲�иŬ�����й���ѧԺԺʿ���������������ֲⶨ������49In����9��Ԫ�����ԭ����������ֵ��������Ϊ�����±�������﨣�37Rb��ͬ���ڡ�����˵������ȷ����
A. In�ǵ������ڵڢ�A��Ԫ��
B. 11549In����������������IJ�ֵΪ17
C. ԭ�Ӱ뾶��In>Al
D. ���ԣ�In(OH)3>RbOH
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com