
【题目】在甲、乙两烧杯溶液中,分别含有大量Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3 种,已知甲烧杯的溶液呈碱性,则乙烧杯溶液中大量存在的离子是( )
A. K+、H+、CO32- B. CO32-、OH-、Cl- C. K+、CO32-、Cl- D. Cu2+、H+、Cl-
科目:高中化学 来源: 题型:
【题目】图为浓硫酸与铜片反应的装置.请回答: 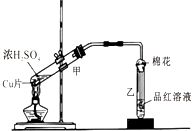
(1)浓硫酸与铜片反应的方程式为 .
(2)反应过程中,甲中的现象是 .
(3)下列说法中,不正确的是 .
A.该反应中浓硫酸表现酸性、氧化性、吸水性
B.试管乙中含有碱液的棉花,其作用是吸收过量的SO2 , 防止环境污染
C.含0.02mol溶质的浓硫酸与足量的铜片反应,能收集到224mL的SO2(标准状况)
D.反应一段时间后,将水缓慢倒入试管甲中,溶液显蓝色.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得到分子式为C5H10的两种产物Y、Z.Y、Z经催化加氢后都可得到2﹣甲基丁烷.则X的结构简式可能为( )
A.CH3CH2CH2CH2CH2Cl
B.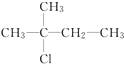
C.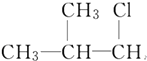
D.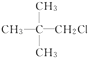
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Science 杂志在2017年春节发表了南京理工大学的论文,报道了世界上首个成功合成的五氮阴离子盐 (N5)6(H3O)3(NH4)4Cl(白色固体),这是全氮含能材料中里程碑式的突破。该盐可简略表示如下,下列分析不合理的是( )
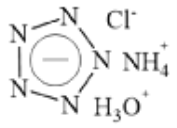
A. 五氮阴离子的化学式为 ![]() B. 该盐中氮元素的化合价均为-3价
B. 该盐中氮元素的化合价均为-3价
C. 该盐遇强碱能释放出NH3 D. 该盐中五氮阴离子具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置中,A是氯气发生仪器,C、D 为气体净化装置(C中装有饱和食盐水,D中装有浓硫酸),E是硬质玻璃管装有细铁丝网,F为干燥的空广口瓶,烧杯G 中装有氢氧化钠溶液. 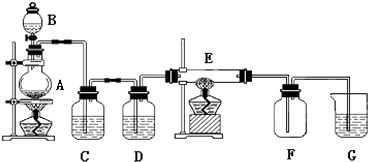
请回答下列问题:
(1)仪器A的名称是;
(2)实验室制氯气的化学方程式:MnO2+4HCl(浓);
(3)C装置的作用是;D装置的作用是;
(4)E中发生化学反应的方程式为:;
(5)烧杯G中发生反应的化学方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个相同的密闭容器中分别充入CO2、H2、O2三种气体,当它们的温度和密度都相同,这三种气体的压强(p)从大到小的顺序是
A.p(H2)>p(CO2)>p(O2)B.p(H2)>p(O2)>p(CO2)
C.p(CO2)>p(H2)>p(O2)D.p(O2)>p(CO2)>p(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含原子数相同的是
A. 5.6LCH4(标准状况)和17.5g N2
B. 16gO2和24gO3
C. 224mL H2(标准状况)和0.1mol CO2
D. 标准状况下,11.2LH2O和0.5molSO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁和铝的碱式碳酸盐是中和胃酸药物的主要成分。欲测定某种镁和铝的碱式碳酸盐的成分进行了以下实验,根据以下实验记录,回答下列问题:
(1)称取6.02g该碱式碳酸盐,加入4.0mol/L盐酸使其溶解,当加入42.5mL时开始产生CO2,当加入盐酸至45.0mL时恰好完全溶解,该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=__________;
(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,试计算确定该碱式碳酸盐的化学式 __________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com