
【题目】在刚刚过去的一年中,发生了许多与化学相关的大事件.下列说法正确的是( )
A.被称为“史上最严”的新![]() 环境保护法
环境保护法![]() 正式实施,我们要运用化学原理从源头上减少和消除工业生产对环境的污染
正式实施,我们要运用化学原理从源头上减少和消除工业生产对环境的污染
B.天津港爆炸事故救援过程中,消防员若发现存放金属钠、电石、甲苯二异氰酸酯等化学品的仓库起火,应立即用泡沫灭火器将火扑灭
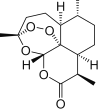
C.世界卫生组织认为青蒿素![]() 结构如图所示
结构如图所示![]() 联合疗法是当下治疗疟疾最有效的手段,烃类物质青蒿素已经拯救了上百万生命
联合疗法是当下治疗疟疾最有效的手段,烃类物质青蒿素已经拯救了上百万生命
D.某品牌化妆品在广告中反复强调产品中不含任何化学成分,是“十年专注自然护肤”的优质产品
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】据了解,铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。考古学家将铜锈分为无害锈(形成了保护层)和有害锈(使器物损坏程度逐步加剧,并不断扩散),结构如图所示。

下列说法正确的是
A. Cu2(OH)3Cl属于有害锈
B. Cu2(OH)2CO3属于复盐
C. 青铜器表面刷一层食盐水可以做保护层
D. 用NaOH溶液法除锈可以保护青铜器的艺术价值,做到“修旧如旧”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃类化合物A,其蒸汽对氢气的相对密度是42,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为____,名称为____。
(2)A中有多少碳原子处于同一平面____;
(3)已知A、B、C有如图转化关系:
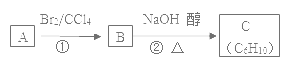
则反应②的化学方程式为___;反应的类型是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制碱制得的纯碱中含有NaHCO3和NaCl杂质。某实验小组对此碱样品进行检查。
(1)取此碱样品10g,加热到质量不再减少,冷却称重,称得质量为9.845g,该样品中NaHCO3的质量分数为__________________________。
(2)另取10g固体样品,加蒸馏水溶解,配成250mL一定物质的量浓度的溶液,配制过程中必需使用的化学仪器有______________________(填字母)
A.烧杯 B.250mL容量瓶C.漏斗 D.胶头滴管 E.玻璃棒 F.试管
(3)量取上述配制好的溶液25mL,向其中加入过量盐酸至 不再产生气泡,共收集到190.4mL(标准状况)气体,该反应过程的离子方程式为______________________、_______________________。10g该样品中含____________gNaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
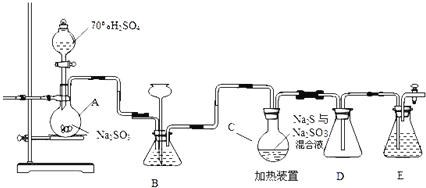
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq)![]() Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)装置A中发生的化学反应方程式为 ______
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 ______ 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 ______
a.蒸馏水 b.饱和Na2SO3溶液 c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是 ______ 。
(4)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是 ______ ,装置E的作用为 ______
(5)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O35H2O,其中可能含有Na2SO3、Na2SO4等杂质,利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: ______ 。
已知:Na2S2O35H2O遇酸易分解:S2O32+2H+=S↓+SO2↑+H2O,供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知KMnO4与浓盐酸在常温下反应能产生Cl2。若用下图所示的实验装置来制备纯净、干燥的氯气,并使它与金属反应。每个虚线框表示一个单元装置,其中错误的是
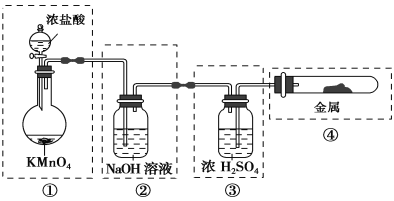
A. ①和②B. ②C. ②和③D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气具有很强的氧化性,工业上保存氯气通常使用干燥的钢瓶。但如果瓶口位置发生漏气,且漏气不明显时,我们可以使用浓氨水来检验。下列有关说法不正确的是( )
A.钢瓶盛装氯气前,如未能干燥氯气,则会有2Fe + 3Cl2 = 2FeCl3 反应发生
B.已知氯气与氨水反应为8NH3 + 3Cl2 = N2 + 6NH4Cl ,每有1mol Cl2参加反应,转移电子为2mol
C.氯气输送时应该使用金属管道或者抗腐蚀类高分子材料管道
D.自来水使用氯气进行消毒,是因为其氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据物质的量的相关公式,完成下列问题。(注意书写单位)
(1)3.01×1023个NH3分子的物质的量__。
(2)0.5molH2SO4含有的氧原子的物质的量__。
(3)2.3gNO2的物质的量__。
(4)标况下,33.6LN2的物质的量___。
(5)0.5mol /LK2SO4溶液中,c(K+)=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯二氧化硅可用来制造光纤。某稻壳灰的成分为
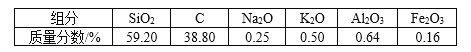
通过如下流程可由稻壳灰制备较纯净的二氧化硅。

请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中属于两性氧化物的是________。
(2)步骤①中涉及SiO2的离子反应方程式为______________。
(3)滤渣A的成分有________和_________(填化学式)。
(4)滤渣B的成分是________(填化学式)。
(5)过滤所需的玻璃仪器除烧杯和玻璃棒外,还有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com