
【题目】锂离子电池已经成为应用最广泛的可充电电池,某种锂离子电池的结构示意图如下,它在放电时有关离子转化关系如图所示,下列说法正确的是

A. Li+透过膜除允许Li+通过外,还允许H2O分子通过
B. 充电时,电池内部发生的总反应为Li++Fe2+![]() Li+Fe3+
Li+Fe3+
C. 充电时,钛电极与外电源的负极相连
D. 放电时,进入贮罐的液体发生的离子反应方程式为:S2O82-+Fe2+=Fe3++2SO42-
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )

A. 由图1可知,T1<T2,该反应正反应为吸热反应
B. 由图2可知,该反应m+n﹤p
C. 图3中,表示反应速率v正>v逆的是点3
D. 图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1molH2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1mol任何物质体积均为22.4L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成有机化合物J的流程如下所示。
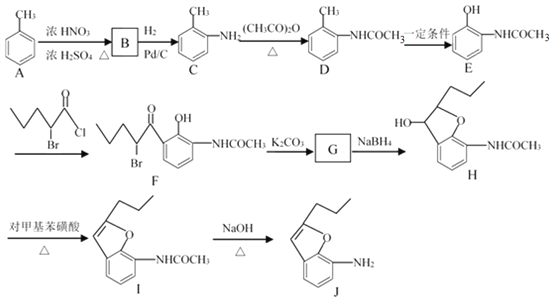
回答下列问题:
(1)B的名称为______。
(2)C![]() D的反应类型为______,H
D的反应类型为______,H![]() I的反应类型为______。
I的反应类型为______。
(3)同时满足下列条件D的同分异构体数目为______。
①能发生银镜反应;②分子结构中含有—NH2;③苯环上有两个取代基,且苯环上的一氯代物有2种。若满足①②条件,且苯环上的一氯代物只有1种,则其中一种物质的结构简式为______。
(4)G的分子式为C13H15O3N,由F生成G的化学方程式为______。
(5)已知:苯胺(![]() )易被氧化,请以乙苯和(CH3CO)2O为原料制备
)易被氧化,请以乙苯和(CH3CO)2O为原料制备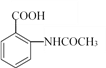 ,参照上述合成过程,写出相应的合成路线流程图(无机试剂任选)_________。
,参照上述合成过程,写出相应的合成路线流程图(无机试剂任选)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应,属于氧化还原反应的是( )
A. CaCO3![]() CaO + CO2 ↑ B. 2NaOH +CO2
CaO + CO2 ↑ B. 2NaOH +CO2![]() Na2CO3+ H2O
Na2CO3+ H2O
C. NaOH+HCl==NaCl+H2O D. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究证明高铁酸钠(Na2FeO4) 是一种“绿色环保高效”消毒剂, 比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.用氯气和氢氧化钠溶液反应制备NaClO溶液
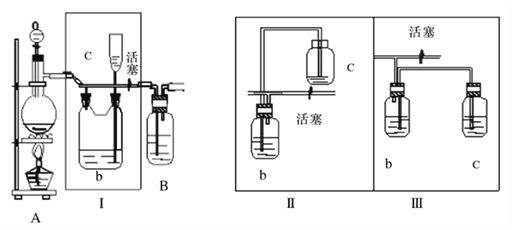
(1)A是氯气发生装置,写出实验室用此装置制取氯气的离子方程式__________。
(2)I装置的作用是__________ 。
(3)用图示的II或III代替I是否可行? __________。简要说明理由__________ 。
(4)将产生的氯气通入D装置中制NaClO溶液
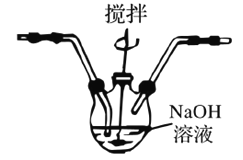
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
5NaCl+NaClO3+3H2O 为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________。
II.制备Na2FeO4
(1)将Fe(NO3)3溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是______。过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是__________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年11月16日新闻报道“阿斯利康哮喘”新药获批上市,哮喘率降低近51%,有机物Z可用于治疗哮喘、系统性红斑狼疮等。其合成路线如下图所示
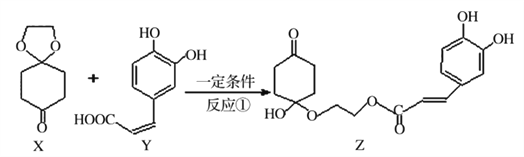
(1)化合物X的有_______种化学环境不同的氢原子。
(2)下列说法正确的是_______.
A.X是芳香化合物 B.Ni催化下Y能与5molH2加成
C.Z能发生加成、取代及消去反应 D. lmolZ最多可与5molNaOH反应
(3)Y与过量的溴水反应的化学方程式为_________。
(4)X可以由_______(写名称)和M(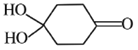 ) 分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N (分子式为C6H8O2),则N的结构简式为_____(己知烯醇式不稳定,会发生分子重排,例如:
) 分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N (分子式为C6H8O2),则N的结构简式为_____(己知烯醇式不稳定,会发生分子重排,例如: 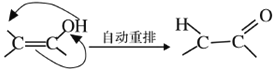 )。
)。
(5)Y也可以与环氟丙烷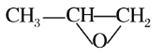 )发生类似反应①的反应,其生成物的结构简式为_________(写一种);Y的同分异构体很多种,其中有苯环、苯环上有二个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有_____种。
)发生类似反应①的反应,其生成物的结构简式为_________(写一种);Y的同分异构体很多种,其中有苯环、苯环上有二个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有_____种。
(6)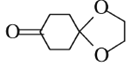 可由
可由 和有机物H分子间脱去一分子水而得,则H的名称为________;通常采用
和有机物H分子间脱去一分子水而得,则H的名称为________;通常采用![]() 为原料合成
为原料合成 ,请参照题目路线图设计该合成路线(无机试剂任选) _______。(合成路线常用的表示方式为:
,请参照题目路线图设计该合成路线(无机试剂任选) _______。(合成路线常用的表示方式为:  )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是( )
A. 1摩尔H2O质量为18g
B. 摩尔是国际科学界建议采用的一种物理量,简称摩,符号为 mol
C. 22.4LO 2 中所含氧气分子为1 摩尔
D. 1mol 氧含 6.02×10 23 个O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用元素的化合价推测物质的性质是化学研究的重要手段.如图是硫元素的常见化合价与部分物质类别的对应关系:
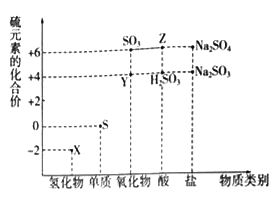
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有_______(填化学式).
(2)将X与Y混合,可生成淡黄色固体.该反应中氧化剂与还原剂的物质的量之比为_______.
(3)检验物质Y的方法是_______________________________.
(4)Z的浓溶液与铜单质在一定条件下可以发生化学反应,该反应的化学方程式为_______.
(5)Na2S2O3是重要的化工原料.从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(6)已知Na2SO3能被K2Cr207氧化为Na2SO4则24mL 0.05molL﹣1的Na2SO3溶液与 20mL 0.02molL﹣1的溶液恰好反应时,Cr元素在还原产物中的化合价为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com