
【题目】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上综合利用铝土矿的部分工艺流程如下。
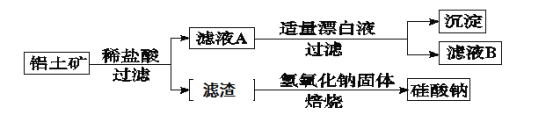
(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
该过程中涉及某氧化还原反应如下,请完成:
□Fe2++□ClO-+ = □Fe(OH)3↓+□C1-+ 。
(2)检验滤液B中是否还含有Fe2+的方法为: 。
(3)将滤液B中的铝元素以沉淀形式析出,选用的最好试剂为 (填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
(4)由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、冷却结晶、 (填操作名称)、洗涤。
(5)滤渣的主要成分是 (填化学式),其与NaOH固体焙烧制备硅酸钠,可采用的装置为 (填代号),该反应的化学方程式是 。
【答案】(1)2Fe2++ClO-+5H2O=2Fe(OH)3↓+C1-+4H+
(2)加入铁氰化钾溶液产生蓝色沉淀或滴加高锰酸钾溶液,紫红色褪去
(3)c (4)过滤 (5)SiO2 B SiO2+2NaOH=Na2SiO3+H2O(焙烧)
【解析】
试题分析:(1)根据方程式可知,铁元素的化合价从+2价升高到+3价,失去1个电子。氯元素的化合价从+1价降低到-1价,得到2个电子,则根据电子的得失守恒可知,还原剂与氧化剂的物质的量之比是2:1。根据原子守恒与电荷守恒可知,反应前有水参加,反应后有氢离子生成,因此配平后的方程式是2Fe2++ClO-+5H2O=2Fe(OH)3↓+C1-+4H+。
(2)亚铁离子具有还原性,因此检验亚铁离子的实验操作可以是取少量滤液B,加入高锰酸钾溶液,紫红色褪去,说明含有亚铁离子。
(3)滤液B中的铝元素以Al3+的形式存在,要以沉淀形式析出,需要加入碱液。由于氢氧化铝是两性氢氧化物,所以不能选择强碱,最好选择弱碱氨水,答案选c。
(4)冷却结晶后有晶体析出,因此分离出晶体的实验操作应该是过滤。
(5)二氧化硅与盐酸不反应,因此滤渣的主要成分是二氧化硅。A、该实验操作是蒸发,不能熔融二氧化硅和氢氧化钠,A错误;B、装置是铁坩埚,可以熔融二氧化硅和氢氧化钠,B正确;C、装置是试管,不能熔融二氧化硅和氢氧化钠,C错误;D、装置是烧杯,烧杯不能熔融氢氧化钠,D错误,答案选b。


科目:高中化学 来源: 题型:
【题目】月球表面土壤里有1种非常有用的资源3He——可控核聚变的原料,有关叙述正确的是( )
A. 在3He中存在:质子数=中子数=核外电子数
B. 3He和4He是同种原子
C. 核聚变时,原子核发生了变化,发生了化学反应
D. 3He和4He互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
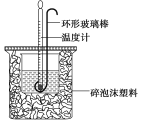
【题目】实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和下图所示装置进行测定中和热的实验,得到表中的数据
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.3 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 20.5 | 20.6 | 24.9 |
(1)碎泡沫塑料的作用是____________________环形玻璃搅拌棒可不可以用铜丝搅拌棒代替,为什么
(2)该实验测得的中和热数值为 kJ·mol-1, (盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算)。
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值 (“偏大”、“偏小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“共建生态文明,共享绿色未来”。下列做法不符合这一主题的是( )
A.将绿色化学应用于化工生产中
B.综合利用化石燃料
C.以可降解餐具代替耐用型餐具
D.选择合适的“低碳”的出行方式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明铜和稀硝酸反应产生一氧化氮气体,某学校学生实验小组设计了一个实验,其装置如下图所示(加热装置与固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是可控制气体流向,用于鼓入空气的双连打气球。
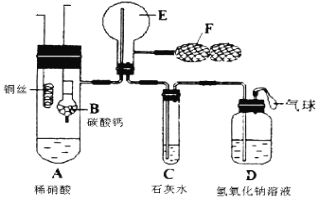
(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为 。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为 。
(3)装置E中开始时出现浅红棕色,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深。假设装置E的体积为66mL,空气残留量为10mL,要鼓入 mL的空气才能将NO全部氧化(设氧气占空气体积的1/5,且所有气体都在同温同压下)。
(4)一段时间后,C中白色沉淀溶解,其原因是 、 (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2、漂白液(有效成分为NaClO)在生产、生活中广泛用于杀菌、消毒。
(1)电解NaCl溶液生成氯气的化学方程式为 。
(2)Cl2溶于H2O、NaOH溶液即获得氯水、漂白液。
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是 。
②25℃,Cl2与H2O、NaOH的反应如下:
反应Ⅰ | Cl2+H2O |
反应Ⅱ | Cl2+2OH- |
不直接使用氯水而使用漂白液做消毒剂的原因是 。
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:Fe-2e-=Fe2+;ClO发生的电极反应式是 。
(4)研究漂白液的稳定性对其生产和保存有实际意义.30℃时,pH=11的漂白液中NaClO的质量百分含量随时间变化如图所示:
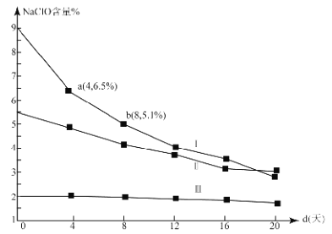
①分解速率v(Ⅰ) v(Ⅱ)(填“>”“<”或“=”),原因是 。
②NaClO分解的化学方程式是 。
③4d-8d,Ⅰ中v(NaClO)= mol/(L·d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com