
【题目】制取物质、探究物质的性质是学习化学必备的素养之一。
回答下列问题。
(1)实验室从含碘废液(除水外含CCl4、I2、I-等)中回收碘,其实验流程如下。

回答下列问题:
①物质X的名称为________;
②操作Ⅰ选用的装置为______(填标号);

③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为___。
④氧化剂Y可用Cl2,也可以用H2O2。将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为________。
(2)某研究小组查阅资料知:氧化性的强弱顺序为:Cl2>IO3->I2。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。

①NaOH溶液的作用是______,反应的离子方程式为___________。
②溶液由黄色最后变为无色所发生反应的离子方程式为____________。
【答案】 四氯化碳 B SO32-+I2 +H2O=SO42-+2I-+2H+ 1:1 吸收尾气Cl2 Cl2+2OH-=H2O+Cl-+ClO- 5Cl2+I2 +6H2O=2IO3-+10Cl-+12H+
【解析】(1)①亚硫酸钠与单质碘发生氧化还原反应生成碘离子和硫酸根离子,四氯化碳不溶于水,分液即得到四氯化碳,因此物质X的名称为四氯化碳;②操作Ⅰ是分液,需要利用分液漏斗,选用的装置为B;③含碘废液中加入稍过量的Na2SO3溶液将I2还原为I-,反应的离子方程式为SO32-+I2+H2O=SO42-+2I-+2H+。④1molCl2得到2mol电子,1molH2O2得到2mol电子,所以根据电子得失守恒可知将同物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为1:1。(2)①氯气有毒,需要尾气处理,则NaOH溶液的作用是吸收尾气Cl2,反应的离子方程式为Cl2+2OH-=H2O+Cl-+ClO-。②通入Cl2一段时间后,KI溶液变为黄色,说明有单质碘生成,继续通入Cl2,溶液黄色变浅,最后变为无色,根据氧化性强弱顺序可判断生成的单质碘继续被氯气氧化为碘酸,因此溶液由黄色最后变为无色所发生反应的离子方程式为5Cl2+I2+6H2O=2IO3-+10Cl-+12H+。


科目:高中化学 来源: 题型:
【题目】在人类社会的发展进程中,金属起着重要的作用。
(1)以下有关金属单质的叙述正确的是_______。
A.金属钠非常活泼,在实验室中保存在石蜡油或煤油中
B.用坩埚钳夹住一小块铝箔,在酒精灯上加热,可观察到铝箔熔化,并有熔融物滴下
C.铁单质与水蒸气反应的化学方程式为:2Fe+3H2O(g)![]() Fe2O3+3H2
Fe2O3+3H2
(2)把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得浊液中逐渐加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图所示。
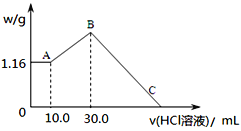
①A点的沉淀物的化学式为______________。
②写出A点至B点发生反应的离子方程式:_________________。
③某溶液中溶有MgCl2和AlCl3两种溶质,若把两者分开,应选用的试剂为:NaOH溶液、_______和盐酸。
④C点(此时沉淀恰好完全溶解)HCl溶液的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学用如图所示装置设计实验,检验碳与浓硫酸反应的产物。
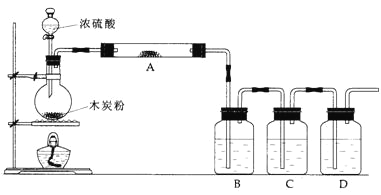
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式:___________。
(2)仪器A中应加入的试剂是______,作用是____________。
(3)仪器B中应加入的试剂是_____,作用是________。
(4)该实验小组在C中加入过量的酸性KMnO4溶液,D中加入澄清的石灰水,可根据__________现象判断产物中存在CO2气体。C中发生反应的离子方程式为:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原子的摩尔质量是M g/mol,则一个此原子的真实质量约为( )
A. M克 B. 1 / M克 C. M / ( 6.02×1023 )克 D. ( 6.02×1023 ) / M克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
酸 | 碱 | 盐 | 酸性氧化物 | 碱性氧化物 | |
A | H2SO4 | Na2CO3 | Cu2(OH)2CO3 | SO3 | Fe2O3 |
B | HCl | NaOH | NaCl | CO2 | Na2O2 |
C | NaHSO4 | NaOH | CuSO4·5H2O | SO2 | MgO |
D | HNO3 | KOH | NaHCO3 | Mn2O7 | CaO |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.强酸性溶液:K+、HCO3、Br、Ba2+
B.滴加酚酞溶液显红色的溶液:Fe3+、NH4+、Cl、NO3
C.强酸性溶液:Cu2+、Na+、Mg2+、SO42
D.含有大量HCO3的溶液:Na+、NO3、Cl、OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃与金属镁在无水乙醚中反应,可得格氏试剂R﹣MgX,它可与醛、酮等羰基化合物加成: ![]() ,所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一.现欲合成(CH3)3C﹣OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
,所得产物经水解可以得到醇,这是某些复杂醇的合成方法之一.现欲合成(CH3)3C﹣OH,下列所选用的卤代烃和羰基化合物的组合正确的是( )
A.乙醛和氯乙烷
B.甲醛和1﹣溴丙烷
C.甲醛和2﹣溴丙烷
D.丙酮和一氯甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下均能通过一步反应实现的是( )
A. NaAlO2(aq)![]() AlCl3
AlCl3![]() Al2O3 B. N2
Al2O3 B. N2![]() NO2
NO2![]() HNO3
HNO3
C. NaCl(饱和)![]() NaHCO3
NaHCO3![]() Na2CO3 D. FeS2
Na2CO3 D. FeS2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用可再生的物质制备乙酸乙酯的绿色合成路线之一如图所示: 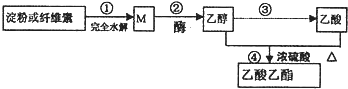
下列说法正确的是( )
A.常温下,M能与银氨溶液发生反应
B.④的反应类型属于酯化反应,不属于取代反应
C.用饱和碳酸钾溶液能鉴别乙醇、乙酸和乙酸乙酯
D.淀粉和纤维素的化学式均为(C6H10O5)n , 二者互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com