
下列说法正确的是( )
A、我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料
B、需要通过化学反应才能从海水中获得食盐和淡水
C、水晶项链和餐桌上的瓷盘都是硅酸盐制品
D、粗硅制备单晶硅涉及氧化还原反应
科目:高中化学 来源: 题型:
黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2
8Cu+4FeO+2Fe2O3+16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是___________(填元素符号)。
(2)上述冶炼过程产生大量SO2。下列处理方案中合理的是________(填代号)。
a.高空排放
b.用于制备硫酸
c.用纯碱溶液吸收制Na2SO3
d.用浓硫酸吸收
(3)过二硫酸钾(K2S2O8)具有强氧化性,可将I-氧化为I2: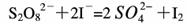
通过改变反应途径Fe3+、Fe2+均可催化上述反应。试用离子方程式表示Fe3+对上述反应催化的过程。________、___________(不必配平)
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
据以上信息回答下列问题:
a.除去Al3+的离子方程式是______________。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸 稀硫酸 KSCN溶液 KMnO4溶液 NaOH溶液 碘水
所选试剂为_____________。
证明炉渣中含有FeO的实验现象为___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。
反应的化学方程式是__________________________________;样品中铝的质量是_______________g。
(2)若取a g样品将其点燃,恰好完全反应,该反应的化学方程式是:
_________________________,氧化铁与铝的质量比是_____________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X和Y是两种单质,它们之间的反应是X+Y==X2++Y2-,现有下列叙述:①X被氧化;②X是氧化剂;
③Y2-是还原产物;④X2+具有氧化性;⑤Y2-具有还原性;⑥Y单质的氧化性比X2+的氧化性强,在上述说法中正确的是( )。
A.①②③ B.①②⑥ C.①③④⑤⑥ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
在钢铁的冶炼中,常用CO气体通入红热的氧化铁中,发生的反应是:Fe2O3+3CO 2Fe+3CO2。请填空:
2Fe+3CO2。请填空:
(1)在上述反应中,________元素的化合价升高,则该元素的原子________电子,发生氧化反应;而________元素的化合价降低,则该元素的原子________电子,发生________反应。
(2)该反应中________是氧化剂,发生了________反应;________是还原剂,发生了________反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
| Ⅰ | Ⅱ | |
| A | 将少量浓氨水滴入Al2(SO4)3溶液 | 将少量Al2(SO4)3溶液滴入浓氨水 |
| B | 将少量SO2通入Ba(OH)2溶液 | 将过量SO2通入少量Ba(OH)2溶液 |
| C | 将0.1mol Cl2通入含0.2molFeBr2的溶液中 | 将0.3mol Cl2通入含0.2mol FeBr2溶液 |
| D | 将过量BaCl2溶液与少量Na2SO4溶液相混合 | 将少量Ba(OH)2溶液与过量MgSO4溶液相混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO—+4OH— =2FeO42— +3Cl— +5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是( )
A.高铁酸钠中铁显+6价 B.湿法中FeO42—是氧化产物
C.干法中每生成1mol Na2FeO4 转移4mol电子
D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
(1)纯铁比碳素钢易生锈 (2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性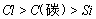
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)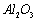 在工业上用于制作耐高温材料,也用于电解法治炼铝
在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
A.(1)(4)(6)(7) B.(4)(6)(9)(10)
C.(3)(5)(6)(8) D.(5)(6)(8)(9)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列中心原子的杂化轨道类型和分子几何构型不正确的是
A.PCl3中P原子sp3杂化,为三角锥形 B.BCl3中B原子sp2杂化,为平面三角形
C.CS2中C原子sp杂化,为直线形 D.H2S分子中,S为sp杂化,为直线形
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com