
| A、过量氯气通入溴化亚铁溶液中:3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 |
| B、过量二氧化碳通入四羟基合铝酸钠溶液中:CO2+[Al(OH)4]-═Al(OH)3↓+HCO3- |
| C、在溶液中亚硫酸氢铵与等物质的量的氢氧化钠混合:HSO3-+OH-═SO32-+H2O |
| D、碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ |


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
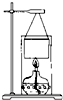 某学校化学科研小组使用一些废旧物品组装了一个简易装置,用来测定乙醇的燃烧热,过程如下:
某学校化学科研小组使用一些废旧物品组装了一个简易装置,用来测定乙醇的燃烧热,过程如下:| 1 |
| 2 |
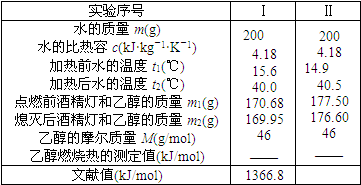
| m×c×(t2-t1)×M |
| m1-m2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入适量6 mol?L-1的盐酸 |
| B、加入少量醋酸钠固体 |
| C、加热 |
| D、加入少量金属钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、再滴加AgNO3溶液,观察是否有黄色沉淀产生 |
| B、再加入CCl4振荡后,观察下层液体颜色是否变为紫红色 |
| C、再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生 |
| D、再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变血红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ag++Cl-→AgCl↓ |
| B、Ag++Cl2+H2O→AgCl↓+2H++ClO- |
| C、Ag++Cl2→AgCl↓Cl- |
| D、Ag++Cl2+H2O→AgCl↓+H++HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HX、HY、HZ均为弱酸 |
| B、在HX、HY、HZ中以HX酸性相对最强 |
| C、在X-、Y-、Z-中,Z-最易水解 |
| D、中和1mol HY,需要的NaOH小于1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体的分散质能透过滤纸 |
| B、胶体的分散质粒子直径在10-7~10-9m之间 |
| C、胶体是纯净物,其它分散系是混合物 |
| D、胶体能产生丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述弱酸溶液的pH=2 |
| B、加入等体积0.01 mol?L-1 NaOH溶液后,所得溶液的pH=7 |
| C、加入等体积0.01 mol?L-1 NaOH溶液后,所得溶液的pH>7 |
| D、加入等体积0.01 mol?L-1NaOH溶液后,所得溶液的pH<7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com