
【题目】按要求填空
(1)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________。
(2)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________。
(3)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则n=________。
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则C的摩尔质量为____________。
(5)在某温度下,NaOH的溶解度为20g,该温度下将80gNaOH投入220g水中,充分搅拌后,静置,测得溶液的密度为1.2g/mL,则该溶液中溶质的物质的量浓度为____________。
【答案】17∶16 4∶3 (a-b)M/18b 5(a+b-d) g·mol-1 5.0 mol·L-1
【解析】
(1)将等物质的量的NH3和CH4混合,根据m=nM可知混合气体中NH3与CH4的质量比为摩尔质量之比,即为17:16。
(2)1分子氨气和甲烷含有的氢原子个数分别是3和4,因此要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为4:3。
(3)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将a g该化合物加热至结晶水全部失去,剩余的残渣为b g,则![]() ,解得n=(a-b)M/18b。
,解得n=(a-b)M/18b。
(4)已知a g A和b g B恰好完全反应生成0.2 mol C和d g D,则根据根据质量守恒定律可知C的质量是(a+b-d)g,所以C的摩尔质量为(a+b-d)g÷0.2mol=5(a+b-d)g·mol-1。
(5)在某温度下,NaOH的溶解度为20g,该温度下将80gNaOH投入220g水中,实际溶解的氢氧化钠质量是![]() ,充分搅拌后,静置,溶液的质量是264g,测得溶液的密度为1.2g/mL,溶液体积是
,充分搅拌后,静置,溶液的质量是264g,测得溶液的密度为1.2g/mL,溶液体积是![]() 220mL=0.22L,溶质的物质的量是44g÷40g/mol=1.1mol,则该溶液中溶质的物质的量浓度为1.1mol÷0.22L=5.0 mol·L-1。
220mL=0.22L,溶质的物质的量是44g÷40g/mol=1.1mol,则该溶液中溶质的物质的量浓度为1.1mol÷0.22L=5.0 mol·L-1。


科目:高中化学 来源: 题型:
【题目】硼镍镧合金具有很强的储氢能力。
(1)用价层电子对互斥理论推测三氟化硼分子的立体构型为______,硼原子的杂化类型为_____。
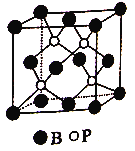
(2)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。如图是磷化硼晶体的晶胞示意图,已知该晶胞的棱长为516pm,最近的B和P原子之间的距离为____pm。该晶体的晶体类型是________。
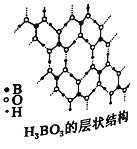
(3)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图)。
①1molH3BO3的晶体中有_____mol氢键。
②硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2O,它电离生成少量[B(OH)4]-和H+,则硼酸为_______元酸,[B(OH)4]-含有的化学键类型为_______。
(4)镧镍合金、铜钙合金及铈钴合金都具有相同类型的晶胞结构,其中铜钙合金的结构单元如图所示。试回答下列问题:
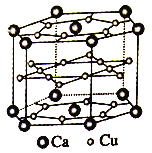
①在元素周期表中Ca位于______区。
②铜原子的基态原子核外电子排布式__________。
③已知镧镍合金LaNin晶胞体积为9.0×10-23cm,储氢后形成LaNinH4.5的合金(氢进入晶胞空隙,体积不变),则LaNin中,n=_____(填数值);氢在合金中的密度为_____(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】准确量取25.00mL KMnO4溶液,最好选用的仪器是
A. 25mL量筒 B. 25mL酸式滴定管
C. 25mL碱式滴定管 D. 有刻度的50mL烧杯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了测定某有机物A的结构,设计如下实验:
①将2.3g该有机物完全燃烧,测得生成0.1molCO2和2.7g 水;
②用质谱仪测定其相对分子质量,得到如图所示的质谱图;
③用核磁共振仪处理该化合物,得到如下图所示核磁共振氢谱,图中三个峰的面积之比是1∶2∶3。
试回答下列问题:


(1)有机物A的相对分子质量是____。
(2)有机物A的实验式是____。
(3)____(填“能”或“不能”)根据A的实验式确实A的分子式,若能,说明原因___。
(4)某有机化合物A在足量的氧气中完全燃烧只生成CO2和H2O,同温同压下,其蒸气对氢气的相对密度为37。用元素分析仪分析得知,A分子中含碳、氢的质量分数分别为64.9%和13.5%,则A的分子式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:A+B=C下列条件的改变一定能使化学反应速率加快的是:
A. 增加A的物质的量 B. 升高体系的温度
C. 增加体系的压强 D. 减少C的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】需要配制500 mL 0.5 mol·L-1氢氧化钠溶液,经测定实际所配氢氧化钠溶液的浓度为0.45 mol·L-1。可能的原因是( )
A. 转移时溶液没有冷却至室温 B. 容量瓶没有烘干
C. 称量氢氧化钠固体时砝码放反了 D. 定容时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温常压下,8 g O2含有4NA个电子
B. 1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C. 标准状况下,22.4 L盐酸含有NA个HCl分子
D. 0.05 mol液态KHSO4中含有0.1NA个阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是![]() ,并含少量的
,并含少量的![]() 、
、![]() 、MgO、CaO等,生产工艺流程图如下:
、MgO、CaO等,生产工艺流程图如下:
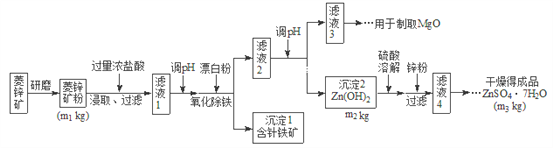
(1)将菱锌矿研磨成粉的目的是_______________。
(2)写出Fe3+水解的离子方程式_________________。
(3)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为__________。
沉淀化学式 |
|
|
|
|
开始沉淀的pH |
|
|
|
|
沉淀完全的pH |
|
|
|
|
开始溶解的pH |
|
|
|
|
Ksp |
|
|
|
|
(4)工业上从“滤液3”制取MgO过程中,合适的反应物是________选填序号。
![]() 大理石粉
大理石粉 ![]() 石灰乳 c纯碱溶液 d氨水
石灰乳 c纯碱溶液 d氨水
(5)“滤液4”之后的操作依次为________、_______、过滤,洗涤,干燥。
(6)分析图中数据,菱锌矿粉中![]() 的质量分数不低于__________用代数式表示
的质量分数不低于__________用代数式表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氨的下列叙述中,不正确的是( )
A.实验室制氨气的方法是加热NH4Cl
B.液氨是纯净物
C.氨易液化,因此可用来作制冷剂
D.氨极易溶于水,因此可用来作喷泉实验
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com