
��¯ˮ���Ȼή��ȼ�ϵ������ʡ�Ӱ���¯��ʹ����������������ɰ�ȫ������
ij��¯ˮ������Ҫ�ɷ���CaCO3��CaSO4��Mg(OH)2��Fe2O3������ϴ���ɳ�ȥ��ˮ���������ԭ������ͼ��ʾ��
��1����ϴʱ��Ϊʹˮ���������ܽ⣬����ѡ�õ��������������� �����ţ���
����
| A������ | B������ | C������ | D��ϡ���� |

��1��D��2��  ��3��
��3�� 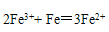
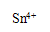
��4�� ����ҺPH����ƽ��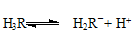 �����ƶ����ԣ�H3R�İٷֺ�����С H2R-
�����ƶ����ԣ�H3R�İٷֺ�����С H2R-
���������������1����ʹ��ϡ�����������������ƣ�����ڷ�Ӧ��ı��棬ʹ��Ӧ�ﲻ����ȫ��Ӧ�ʲ���ѡ���ᡣ��2����ˮ�������ữ֮��ֻ��������Dz��������̼���ƣ��������ܽ�ȸ�С��̼��ƣ�3��Fe3+���������Կ�������л�ԭ�Ե�����Ӧ�����������ӣ��ḯʴ���ʹܵ����ݵ�ʧ����������ȵ�ԭ����Ħ�������������ӣ�����������ӣ��ܹ��õ���Ħ���ĵ��ӣ�����һĦ��Sn2+ת��Ϊ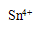 ��4��
��4��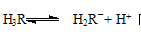 ����PHֵ������������Ũ�Ȼ��С��ƽ�������ƶ�������H3R��������١�H3R��H2R����HR2����R3����ͼ���б�ʾ�����߷ֱ�Ϊa��b��c��d���Դ�ͼ���Ͽ���B��ʽ��ߵ����Ժ���������H2R��
����PHֵ������������Ũ�Ȼ��С��ƽ�������ƶ�������H3R��������١�H3R��H2R����HR2����R3����ͼ���б�ʾ�����߷ֱ�Ϊa��b��c��d���Դ�ͼ���Ͽ���B��ʽ��ߵ����Ժ���������H2R��
���㣺�����ܽ�ƽ�⼰ƽ���ƶ������֪ʶ��


 ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
HAΪ������ǿ�ڴ����һԪ���ᣬ������������ȷ����
| A��0. 1 mol?L��1 HA��c(H+)= c(OH��)+ c(A��) |
| B��0. 1 mol?L��1 HA�� 0. 1 mol?L��1NaOH �������Һ�����ԣ�c(Na+)= c(A��) |
| C��0. 1 mol?L��1 NaA ��c(Na+)> c(OH��)>c(A��)> c(H+) |
| D��0. 1 mol?L��1 HA�м�������NaA���壬HA�ĵ��볣����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������Һ��,�й����ʵ���Ũ�ȹ�ϵ��ȷ����
A�������£���10 mL pH��3.0�Ĵ�����Һ�м���ˮϡ�ͺ���Һ�� ��Ҫ��С
��Ҫ��С
B��pH��8.0��KHS��Һ��,c(K+)> c(HS-)> c(OH-)> c(S2-)> c(H+)
C����0.2 mol��L��1��ijһԪ��HA��Һ��0.1 mol��L��1NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ�У�2c(OH��)��c (A��)��2c(H��)��c(HA)
D���������������Ͱ�ˮ��ϣ���ַ�Ӧ��������Һ�����ԣ�������Һ�����ʵ���Ũ�ȹ�ϵΪ��c(NH3��H2O)��c(HCl)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��5�֣���ʢ��1 mL 0.1 mol/L MgCl����Һ���Թ��еμӣ��Σ�1��Լ0.05mL����mol/L NaOH��Һ���а�ɫ�������ɣ��ٵμӣ���0.��mol/LFeCl3��Һ�����á����Թ۲쵽�������� �������������ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��6�֣�����Ũ��Ϊ0.lmol/L�����ֵ������Һ����Na2CO3��NaHCO3��NaAlO2��CH3COONa��NaOH
��֪��
��1������������Һ��pH�ɴ�С��˳��Ϊ________��������ţ�
��2����������Һϡ����ͬ�ı���ʱ����pH�仯������________���������)
��3��������������Һ�зֱ����AlCl3��Һ���ܲ�����ɫ�������_______���������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣����¶�t���£�ijBa(OH)2��ϡ��Һ��c(H+)=10-amol/L��c(OH-)=10-bmol/L����֪a+b=12�������Һ����μ���pH=b��NaHSO4����û����Һ�IJ���pH���±���ʾ��
| ��� | �������������/mL | �������Ƶ����/mL | ��Һ��pH |
| �� | 33.00 | 0.00 | 8 |
| �� | 33.00 | x | 7 |
| �� | 33.00 | 33.00 | 6 |
 )��c(
)��c( )��c(
)��c( )��c(
)��c( )��c(
)��c( )
) )��c(
)��c( )��c(
)��c( )��2c(
)��2c( )��c(
)��c( )
) )��c(
)��c( )��c(
)��c( )��c(
)��c( )
) )��c(
)��c( )��c(
)��c( )�ֱ����
)�ֱ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣�Ԫ�ؼ��仯�����������������о��й㷺����;��
��.����ѧ�ḻ��ʣ�
���ڳ����£����ܻ�����ϡ���ᷴӦ��������ɫ��Һ����ͭ��ȣ������������ �����ǿ����������
��Cr( OH)3��Al( OH)3���ƣ�Ҳ���������������ˮ�д�����ʽ�ͼ�ʽ����ƽ�⣬����ʽ���뷽��ʽ�� ��
(3)��ҵ�Ͼ�����������Ⱦ����֮һ������K2Cr2O7���Է�ˮ��������ڣ�����������NaCl����Fe��ʯīΪ�缫���е�⡣һ��ʱ�������Cr(OH)3��Fe(OH)3������ȥ(��֪Ksp[ Fe(OH)3]=4.0��10-38��Ksp[Cr(OH)3]=6.0��l0-31)����֪�������Һ��c( Fe3+)Ϊ2.0��10��13mol/L������Һ��c(Cr3+)Ϊ mol/L��
��.����A��H����ͼ��ʾת����ϵ(����������δ�г�)��A��E��F��G��Ϊ���壬DΪ���ؽ���֮һ��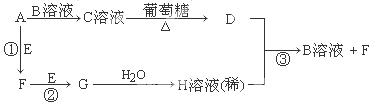
��ش��������⣺
��1��A������ ���ӣ�����ԡ��Ǽ��ԡ�����C��Һ�е��������� (д��ѧʽ��������ˮ�ĵ���)��
��2����Ӧ�ٵĻ�ѧ����ʽΪ ����Ӧ�۵����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪����ʱ��0.1 mol/LijһԪ��HA��ˮ����0.1%�������룬�ش��������⣺
(1)����Һ��c(H��)�� ��
(2)HA�ĵ���ƽ�ⳣ��K�� ��
(3)�����¶�ʱ��K (���������С�����䡱)��
(4)��HA�������c(H��)ԼΪˮ�������c(H��)�� ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ˮ��þʯ(��Ҫ�ɷ�ΪMgCl2��6H2O)Ϊԭ��������ʽ̼��þ����Ҫ�������£�
(1)Ԥ������������Mg(OH)2�������ɣ���֪������Mg(OH)2��Ksp��1.8��10��11������Һ��c(OH��)��3.0��10��6 mol��L��1������Һ��c(Mg2��)�� ��
(2)���������е���ҺŨ���ᾧ��������Ҫ�������ʵĻ�ѧʽ
(3)�������ռ�ʽ̼��þ�õ�MgO��ȡ��ʽ̼��þ4.66 g���������������أ��õ�����2.00 g�ͱ�״����CO2 0.896 L��ͨ������ȷ����ʽ̼��þ�Ļ�ѧʽ��
(4)����ˮ�ⲻ��ȫ�����ü�ʽ̼��þ�н�����MgCO3�����Ʒ��þ���������� (����ߡ��������͡����䡱)��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com