
【题目】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:

相关金属离子[c0(Mn+)=0.1 mol·L1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______________________________________。
(2)“氧化”中添加适量的MnO2的作用是将________________________,检验生成离子试剂___________。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间,除铝的离子反应方程式是__________。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)氧化中除了添加适量MnO2还可以用H2O2来氧化,写出该离子反应_______________。
(6)写出“沉锰”的离子方程式_______________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,z=___________。
时,z=___________。
(8)写出Fe2+和HNO3的离子反应__________。
【答案】SiO2(不溶性硅酸盐) MnO2+MnS+2H2SO4=2MnSO4+S+2H2O 将Fe2+氧化为Fe3+ KSCN溶液 4.7 Al3++3NH3·H2O=Al(OH)3↓+3NH4+ NiS和ZnS 2Fe2++H2O2+2H+=2Fe3+ +2H2O Mn2++2![]() =MnCO3↓+CO2↑+H2O
=MnCO3↓+CO2↑+H2O ![]() 3Fe2+ +4H++NO3-=3Fe3++NO↑+2H2O
3Fe2+ +4H++NO3-=3Fe3++NO↑+2H2O
【解析】
(1)SiO2难溶于硫酸;“溶浸”中二氧化锰能氧化硫化锰生成硫酸锰、硫和水;
(2)MnO2具有氧化性,可以将Fe2+氧化为Fe3+;KSCN溶液遇Fe3+变红;
(3)Fe3+完全沉淀的pH是2.8,Al3+完全沉淀的pH是4.7;氨水与硫酸铝反应生成氢氧化铝沉淀和硫酸铵;
(4)加入Na2S除去Zn2+和Ni2+,生成沉淀NiS和ZnS;
(5)H2O2和Fe2+反应,氧化产物是Fe3+、还原产物是H2O;
(6)“沉锰”过程中硫酸锰和碳酸氢铵反应生成碳酸锰沉淀、硫酸铵、二氧化碳;
(7)根据元素化合价代数和等于0计算z值;
(8)Fe2+和HNO3发生氧化还原反应,氧化产物是Fe3+、还原产物是NO。
(1)SiO2难溶于硫酸,所以“滤渣1”含有SiO2;“溶浸”中二氧化锰能氧化硫化锰生成硫酸锰、硫和水,根据得失电子守恒,反应方程式是MnO2+MnS+2H2SO4=2MnSO4+S+2H2O;
(2)MnO2具有氧化性,“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+;KSCN溶液遇Fe3+变红,检验Fe3+的试剂是KSCN溶液;
(3)Fe3+完全沉淀的pH是2.8,Al3+完全沉淀的pH是4.7,“调pH”除铁和铝,溶液的pH范围应调节为4.7~6之间,氨水与硫酸铝反应生成氢氧化铝沉淀和硫酸铵,反应的离子方程式是Al3++3NH3H2O=Al(OH)3↓+3NH4+;
(4)加入Na2S除去Zn2+和Ni2+,生成沉淀NiS和ZnS,所以“滤渣3”的主要成分是NiS和ZnS;
(5)H2O2和Fe2+反应,氧化产物是Fe3+、还原产物是H2O,反应的离子方程式是2Fe2++H2O2+2H+=2Fe3+ +2H2O;
(6)“沉锰”过程中硫酸锰与碳酸氢铵反应生成碳酸锰沉淀、硫酸铵、二氧化碳,反应的离子方程式是Mn2++2![]() =MnCO3↓+CO2↑+H2O;
=MnCO3↓+CO2↑+H2O;
(7)LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=![]() 时,根据元素化合价代数和等于0,1+2
时,根据元素化合价代数和等于0,1+2![]() +3
+3![]() +4z-2×2=0,z=
+4z-2×2=0,z=![]() ;
;
(8)Fe2+和HNO3发生氧化还原反应,氧化产物是Fe3+、还原产物是NO,根据得失电子守恒,反应的离子方程式是3Fe2+ +4H++NO3-=3Fe3++NO↑+2H2O。


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:
【题目】某化学实验室产生的废液中的阳离子只可能含有Na+、NH4+、Ba2+、Cu2+、Al3+、Fe2+、Fe3+中的某几种,实验室设计了下述方案对废液进行处理,以回收金属,保护环境。
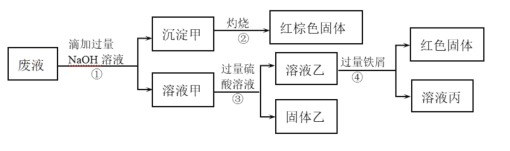
已知:步骤①中,滴加NaOH溶液过程中产生的沉淀会部分溶解。下列说法中正确的是
A.根据步骤①的现象,说明废液中一定含有Al3+
B.由步骤②中红棕色固体可知,废液中一定存在Fe3+
C.沉淀甲中可能含有Al(OH)3
D.该废液中一定含有NH4+、Ba2+、Cu2+、Fe2+和Fe3+至少存在一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在20 mL 0.1 mol·L-1一元弱酸HA溶液中滴加0. 1 mol· L-1 NaOH溶液,溶液中1g[c(A-)/c(HA)]与pH关系如图所示。下列说法正确的是

A. A点对应溶液中:c(Na+)>c(A-)>c(H+)>c(OH-)
B. 25℃时,HA酸的电离常数为1. 0× 10-5.3
C. B点对应的NaOH溶液体积为10 mL
D. 对C点溶液加热(不考虑挥发),则c(A-)/[c(HA)c(OH-)]一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
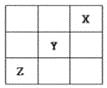
A.Z一定是活泼的金属元素
B.Y的最高价氧化物的水化物是一种强酸
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘化氢常用于制备碘的化合物和用作有机反应的还原剂。碘化氢不稳定,易分解,碘化氢极易溶于水,其水溶液称为氢碘酸,氢碘酸是强酸,有较强的还原性。
(1)氢碘酸若在空气中长期放置,溶液会变成黄色,其原因是___(用化学方程式来表示)。
(2)实验室中常用干燥的红磷和碘相互接触,加少量水微热,即可生成碘化氢和亚磷酸(H3PO3),该反应的化学方程式为___。
(3)氢气和碘蒸气能直接反应生成碘化氢,H2(g)+I2(g)![]() 2HI(g) ΔH<0。T℃时,向1L恒容密闭容器中充入0.2molH2和0.2molI2(g),5min时反应达到平衡,H2、I2(g)和HI的物质的量浓度(c)随时间(t)变化的曲线如图l所示:
2HI(g) ΔH<0。T℃时,向1L恒容密闭容器中充入0.2molH2和0.2molI2(g),5min时反应达到平衡,H2、I2(g)和HI的物质的量浓度(c)随时间(t)变化的曲线如图l所示:
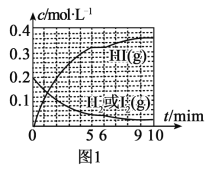
①0~5min内,以HI表示的该反应速率v(HI)=___。
②T℃时,该反应的平衡常数K=___。
③6min时,改变的外界条件为___。
④10min时,保持其他条件不变,再向容器中充入0.1molH2、0.1molI2(g)、0.2molHI(g),12min时达到新平衡。在图2中画出10~12min,H2和HI的浓度变化曲线___(曲线上标明H2和HI);0~5min和0~2min时间段,H2的转化率分别用α1、α2表示,则αl___α2(填“>”、“<”或“=”)。
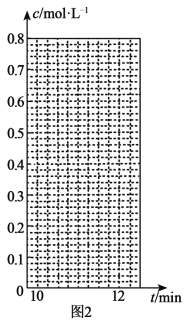
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有1L0.6mol· L-1的盐酸和 NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体的体积比为V(甲) : V(乙)= 3: 4,则加入铝粉的质量为
A.7.2 gB.5.4 gC.3.6 gD.2.7 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)写出H2CO3的电离方程式:__________________________________________。
(2)现有①CH3COOH、②HCl两种溶液,选择填空:
A.①>② B.①<② C.①﹦②
①当它们物质的量浓度相等时,中和等体积、等物质的量浓度的烧碱溶液需两种酸溶液的体积关系为____________。
②当它们氢离子浓度相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为____________。
II.煤化工产业中常用合成气(主要成分是氢气和一氧化碳气体)合成氨和甲醇。请回答:
(1)工业合成氨的化学方程式为N2+3H2![]() 2NH3 ,在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。则该条件下的平衡常数为________。
2NH3 ,在某压强恒定的密闭容器中加入2 mol N2和4 mol H2,达到平衡时,N2的转化率为50%,体积变为10 L。则该条件下的平衡常数为________。
(2)合成甲醇的主要反应是2H2(g)+CO(g)![]() CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如:
CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如:
物质 | H2 | CO | CH3OH |
浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率v(H2)=________。
②比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
③反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡______(填“逆向”、“正向”或“不”)移动,平衡常数K_________(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锂离子电池的正极材料(主要含LiCoO2、Al、C等)为原料制备CoC2O4.2H2O的一种实验流程如图:
![]()
![]()
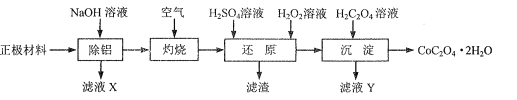
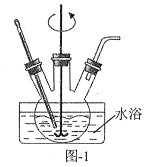
(1)“除铝”可在如图1所示的装置中进行。保持温度、反应物和溶剂的量不变,实验中提高铝的去除率的措施有___。
(2)“灼烧”的主要目的是___。
(3)“还原”步骤温度在70℃左右,LiCoO2发生反应的化学方程式为___。若该步骤用盐酸代替H2SO4和H2O2,也可达到“还原”的目的,但其缺点是___。
(4)“沉淀”步骤中,证明Co2+已沉淀完全的实验操作及现象是___。
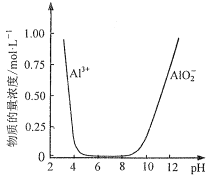
(5)设计由“滤液X”制备纯净的Al2O3的实验方案。(已知含铝物种浓度与pH的关系如图所示。实验中必须使用的试剂:H2SO4溶液、BaCl2溶液、蒸馏水)___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com