
【题目】欲配制0.2mol/L 的NaOH溶液980mL,有以下仪器:
①烧杯 ②100mL量筒 ③托盘天平(带砝码) ④玻璃棒 ⑤胶头滴管
(1)配制时,必须使用的仪器有___________(填代号),还缺少的玻璃仪器是 ________。该实验中两次用到玻璃棒,其作用分别是_______________,_________________。
(2)使用容量瓶前必须进行的一步操作是_____________________。
(3)配制溶液时,一般可以分为以下几个步骤:正确的操作顺序是:_______________(用字母表示,每个字母只能用一次);
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.用托盘天平准确称取所需的NaOH固体的质量,放入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C.将已冷却的溶液沿玻璃棒注入1000mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
在①操作中需称量NaOH_______g
(4)请你分析下列哪些操作会引起所配浓度偏大(填写字母)___________________。
A.将NaOH放在滤纸上称量
B.称取NaOH的砝码已生锈
C.容量瓶未干燥即用来配制溶液
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
E.往容量瓶转移时,有少量液体溅出
F.在容量瓶中定容时视线如下图所示

G.烧杯未进行洗涤
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(5)若定容时不小心使液面超过了刻度线,应采取的措施是_______________
【答案】①③④⑤1000 mL容量瓶搅拌加速溶解引流检漏BCAFED8.0 gBDF重新配制
【解析】
(1)欲配制0.2mol/L的NaOH溶液980mL,需要1000mL容量瓶。配制溶液的操作步骤为:首先计算出需要的药品的质量,然后用托盘天平称量,后放入烧杯中溶解,同时用玻璃棒搅拌,待溶液冷却至室温后,用玻璃杯引流移液至1000mL容量瓶中,然后洗涤烧杯和玻璃棒2~3次,将洗涤液也注入容量瓶,然后向容量瓶中注水,至液面离刻度线1~2cm时,改用胶头滴管逐滴加入,至凹液面与刻度线相切,然后摇匀、装瓶,所以用到的仪器有:托盘天平、烧杯、玻璃棒、1000mL容量瓶、胶头滴管,故必须使用的仪器是①③④⑤,还缺少的玻璃仪器是1000 mL容量瓶。实验中两次用到玻璃棒,溶解氢氧化钠溶液时需要使用玻璃棒搅拌加速溶解、转移溶液时用玻璃棒引流。
(2)容量瓶使用前必须要捡漏;
(3)操作过程是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶等步骤,故正确的操作顺序为BCAFED;根据n=cV可知需要NaOH的物质的量为1L×0.2mol/L=0.2mol,质量为m=nM=0.2mol×40g/mol=8.0g;
(4)A.将NaOH放在滤纸上称量,由于氢氧化钠易吸水,导致氢氧化钠的质量减少,浓度偏小;
B.称取NaOH的砝码已生锈,氢氧化钠的质量增加,浓度偏大;
C.容量瓶未干燥即用来配制溶液不影响;
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容,冷却后溶液体积减小,浓度偏大;
E.往容量瓶转移时,有少量液体溅出,溶质减少,浓度偏小;
F.根据示意图可知俯视刻度线,溶液体积减小,浓度偏大。
G.烧杯未进行洗涤,溶质减少,浓度偏小;
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,溶液体积增加,浓度偏小。
答案为BDF。
(6)若定容时不小心使液面超过了刻度线,则无法补救,只能重新配制。


科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g)![]() pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
pC(g)在密闭容器中进行,右图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是

A.T1<T2 p1>p2 m+n>p 放热反应
B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应
D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 等质量的乙烯和乙醇完全燃烧,消耗O2的物质的量相同
B. 乙醇与浓硫酸混合,加热至170℃制乙烯的反应属于消去反应
C. 用酸性重铬酸钾溶液检验酒驾,发生的反应属于乙醇的氧化反应
D. 乙醛使溴水或酸性KMnO4溶液褪色均属于氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:锂离子电池的总反应为:LixC+Li1-xCoO2![]() C+LiCoO2锂硫电池的总反应为:2Li+S
C+LiCoO2锂硫电池的总反应为:2Li+S![]() Li2S。有关上述两种电池说法正确的是
Li2S。有关上述两种电池说法正确的是
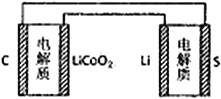
A. 锂离子电池放电时,Li+向负极迁移 B. 锂硫电池充电时,锂电极发生还原反应
C. 理论上两种电池的比能量相同 D. 右图表示用锂离子电池给锂硫电池充电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在航天飞机返回地球大气层时,为防止其与空气剧烈摩擦而被烧毁,需在航天飞机外表面安装保护层.该保护层的材料可能为( )
A.铝合金
B.合金钢
C.新型陶瓷
D.塑料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠保存不当容易变质,某课外活动小组为了粗略测定过氧化钠的质量分数,他们称取10.0g样品,并设计用如图装置来测定过氧化钠的质量分数。

上图中的E和F构成量气装置,用来测定O2的体积。
(1)写出以下装置发生反应的化学方程式:
装置A:___________________________。
装置B:___________________________。
装置C:____________________________。
(2)NaOH溶液的作用是_________________________。
(3)为准确读出氧气的体积需以下操作,正确的顺序为_________。
A.调整量筒高度,使广口瓶E与量筒F内液面相平
B.将气体冷却至室温
C.平视,使凹液面最低点与视线水平相切再读数
读出量筒内水的体积后,折算成标准状况氧气的体积为1.12L,则样品中过氧化钠的质量分数为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同主族常见的三种元素 X、Y、Z,它们最高价氧化物对应水化物的酸性强弱顺序为:HXO4<HYO4<HZO4 , 下列判断不正确的是( )
A.Y 单质可以在海水中提取
B.单质氧化性:Y>Z
C.气态氢化物稳定性:HX<HZ
D.离子半径:X﹣>Y﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: CH3COOH 的酸性强于H2CO3。
(1)请写出H2CO3的电离方程式_____________________________。
(2)请写出CH3COONa 的水解离子方程式_____________________________。
(3)浓度均为0.1mol/L的CH3COONa 溶液和Na2CO3溶液,pH 前者_______后者(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中可逆反应 mA(g)+nB(g)![]() pC(g)+qQ(g)m、n、p、q为任意整数时,达到平衡的标志是
pC(g)+qQ(g)m、n、p、q为任意整数时,达到平衡的标志是
①体系的压强不再改变 ②体系的温度不再改变 ③各组分的浓度不再改变 ④各组分的质量分数不再改变 ⑤反应速率v(A)∶v(B)∶v(C)∶v(Q)=m∶n∶p∶q ⑥单位时间内m mol A断键反应,同时p mol C也断键反应
A. ③④⑤⑥ B. ①③④⑤ C. ②③④⑥ D. ①③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com