
【题目】决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
A通常显 价,B元素的核外电子排布式为 。
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如下图所示),已知3种离子晶体的晶格能数据如下表:

离子晶体 | NaCl | KCl | CaO |
晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是 。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有 个。
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是 。
(4)某配合物的分子结构如下图所示,其分子内不含有 (填序号)。

A.离子键
B.极性键
C.金属键
D.配位键
E.氢键
F.非极性键
【答案】
(1)+3;1s22s22p63s2
(2)TiN>MgO>CaO>KCl;12
(3)CrO2;
(4)AC
【解析】
试题分析:(1)从表中原子的第一至第四电离能可以看出,A的第一、第二、第三电离能都较小,可失去3个电子,最高化合价为+3价,应为Al元素,可失去2个电子,即最外层应有2个电子,应为Mg元素,核外电子排布式为1s22s22p63s2,故答案为:+3;1s22s22p63s2;
(2)离子晶体中晶格能越大,形成的离子晶体越稳定,熔点越高硬度越大,晶格能与离子的半径、电荷有关,电荷越多、离子半径越小,晶格能越大,TiN中阴阳离子所带电荷为3,大于其它离子所带电荷,MgO、CaO中所带电荷相同,但镁离子半径小于钙离子半径,氯化钾中阴阳离子所带电荷为1,且钾离子半径>钙离子半径,氯离子半径大于氧离子半径,所以KCl、MgO、CaO、TiN4种离子晶体熔点从高到低的顺序是TiN>MgO>CaO>KCl; MgO的晶体结构与NaCl的晶体结构相似,所以一个Mg2+周围和它最邻近且等距离的Mg2+个数为12,故答案为:TiN>MgO>CaO>KCl;12;
(3)V2O5中钒离子的核外电子排布式为:1s22s22p63s23p6;CrO2中铬离子的核外电子排布式为1s22s22p63s23p63d2,所以CrO2中的未成对电子数大于V2O5中未成对电子数,故选CrO2,故答案为:CrO2;
(4)该配合物中存在的化学键有:非金属元素之间的共价键,镍元素与氮元素之间的配位键,氧原子和氢原子之间的氢键,故选AC。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接4个不同的原子或原子团,则这种碳原子称为“手性碳原子”。凡有一个手性碳原子的物质一定具有光学活性。物质:  ,具有光学活性,它发生下列反应后生成的有机物没有光学活性的是( )
,具有光学活性,它发生下列反应后生成的有机物没有光学活性的是( )
A.与NaOH溶液共热
B.与甲酸发生酯化反应
C.与银氨溶液发生银镜反应
D.在Ni催化下与H2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 原电池是利用氧化还原反应将化学能转换为电能的装置
B. 由于生铁中含碳,所以比纯铁耐腐蚀
C. 在原电池中,电子从正极流向负极
D. 在原电池中,负极上发生还原反应,正极上发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提纯下列物质(括号内物质为杂质),所选用的除杂试剂和分离方法正确的是
被提纯的物质 | 除杂试剂 | 分离方法 | |
A | 乙酸乙酯(乙醇) | 乙酸 | 加热回流 |
B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
C | 乙醇(乙酸) | 新制氧化钙 | 蒸馏 |
D | 苯(溴) | 碘化钾溶液 | 分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有广泛用途。一种合成阿魏酸的反应可表示为:
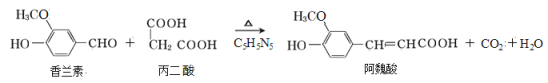
下列说法正确的是
A.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B.香兰素、阿魏酸均可与Na2CO3、 NaOH溶液反应
C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D.与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

(1)负极反应式为________________________;正极反应式为__________________________。
(2)该电池工作时,H2和O2连续由外部供给,电池可连续不断地提供电能。因此,大量安全储氢是关键技术之一。
金属锂是一种重要的储氢材料,其吸氢和放氢原理如下:
Ⅰ.2Li+H22LiH
Ⅱ.LiH+H2O===LiOH+H2↑
①反应Ⅱ中的氧化剂是________________;
②已知LiH固体密度为0.80g·cm-3,用锂吸收112 L(标准状况下)H2,生成的LiH体积与被吸收的H2体积比为__________(可用分数表示或用a×10-b表示,a保留两位小数);
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com