
【题目】某原电池装置如图所示。下列有关叙述中,正确的是
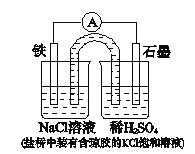
A.Fe作正极,发生氧化反应
B.负极反应: 2H+ + 2e-=H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.工作一段时间后,NaCl溶液中c(Cl-)增大
科目:高中化学 来源: 题型:
【题目】将大气中的氮气活化合成氨是维持地球上生命所必需的转化过程,最近我国成功研制出高效电催化固氮催化剂Mo2N,它的研制成功能有效提高氮肥生产效率。
回答下列问题:
(1)钼(Mo)位于第五周期,与铬同副族,则Mo的价电子排布式为______________。
(2)基态氮原子核外电子空间运动状态有____种,氮元素所在周期中第一电离能最大的前三种元素依次是____(按由大到小的顺序写)。
(3)氮元素能形成一系列的化合物,如NH3、HN3(结构式为![]() )、H2NCH2COOH等。NH3的分子构型为________,HN3结构式中间两个氮原子的杂化轨道类型为________,1个HN3分子中含______个π键;H2NCH2COOH(熔点为182 ℃)、CH3CH2COOH(熔点为22 ℃)的相对分子质量几乎相同,但熔点相差很大,从物质结构的角度分析,导致该现象的主要原因是______。
)、H2NCH2COOH等。NH3的分子构型为________,HN3结构式中间两个氮原子的杂化轨道类型为________,1个HN3分子中含______个π键;H2NCH2COOH(熔点为182 ℃)、CH3CH2COOH(熔点为22 ℃)的相对分子质量几乎相同,但熔点相差很大,从物质结构的角度分析,导致该现象的主要原因是______。
(4)氮与铂元素形成的某种化合物晶胞如图所示,则该化合物的化学式为______,若该晶胞的边长为d pm,则晶体的密度为____ g/cm3。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制纯碱的化学史上,侯德榜使用而索尔维法没有使用的反应原理的化学方程式是( )
A.CO2+NaCl+NH3+H2O→NaHCO3↓+NH4Cl
B.2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.CaO+2NH4Cl→CaCl2+2NH3↑+H2O
D.NaHCO3+NH3+NaCl→Na2CO3+NH4Cl↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于
A.1.7B.2.0C.12.0D.12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物G的合成路线如下:

已知:C为烃
(1)A中含氧官能团名称为:____________。
(2)E的化学名称为:__________________。
(3)F→G的反应类型___________________。
(4)F的结构简式_____________________________。
(5)写反应①的化学方程式________________________________。
(6)写出D生成E的化学方程式________________________________。
(7)满足下列条件B的同分异构体有________种,其中核磁共振氢谱图中峰的面积之比为1∶2∶2∶3的结构为__________________(任意写一种)。①含苯环结构;②只有一种官能团。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。回答下列问题:

(1)液滴边缘是_______(填“正”或“负”)极区,发生的电极反应为____________________________。
(2)液滴中的Cl-由_______区向_______区迁移(填“b”或“a”)。
(3)在b区出现铁锈环的原因是液滴下的Fe因发生氧化反应而被腐蚀,生成的Fe2+_____________________进一步氧化、脱水形成铁锈。
(4)若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:还原性HSO3->I-,氧化性IO3-> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目_______。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后溶液中的还原产物为_______(填化学式);
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0.1000 mol·L![]() NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L![]()
![]() 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是

A.点①所示溶液中:![]()
B.点②所示溶液中:![]()
C.点③所示溶液中:![]()
D.滴定过程中可能出现:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,调节反应物用量与浓度不会改变反应产物的是( )
A.![]() 通入石灰水B.NaOH溶液滴入
通入石灰水B.NaOH溶液滴入![]() 溶液
溶液
C.硫酸中加入锌粉D.![]() 溶液中滴入NaOH溶液
溶液中滴入NaOH溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com