
【题目】将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。回答下列问题:

(1)液滴边缘是_______(填“正”或“负”)极区,发生的电极反应为____________________________。
(2)液滴中的Cl-由_______区向_______区迁移(填“b”或“a”)。
(3)在b区出现铁锈环的原因是液滴下的Fe因发生氧化反应而被腐蚀,生成的Fe2+_____________________进一步氧化、脱水形成铁锈。
(4)若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为___________________________。
【答案】正 O2+2H2O+4e-=4OH- b a 由a区向b区迁移,与b区的OH-形成Fe(OH)2 Fe-2e-=Fe2+
【解析】
NaCl溶液滴到一块光亮清洁的铁板表面上,一段时间后在液滴覆盖的圆周中心区(a)被腐蚀变暗,实际上是发生了吸氧腐蚀,这时,负极电极反应为:Fe-2e-=Fe2+(发生氧化反应)正极电极反应为:O2+2H2O+4e-=4OH-(发生还原反应)在液滴外沿,由于Fe2++2OH-=Fe(OH)2,4Fe(OH)2+O2+2H2O=4Fe(OH)3 形成了棕色铁锈环(b),据此分析。
(1)液滴边缘是正极区,O2在液滴外沿反应,正极电极反应为:O2+2H2O+4e-=4OH-(发生还原反应);
(2)在电解池中,阴离子氯离子移向阳极,即液滴中的Cl-由b区向a区迁移;
(3)在b区出现铁锈环的原因是液滴下的Fe因发生氧化反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2进一步氧化、脱水形成铁锈;
(4)若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,由于Fe的金属活动性比铜强,Fe仍为负极,负极发生的电极反应为:Fe-2e-=Fe2+。


科目:高中化学 来源: 题型:
【题目】HBr是一种重要的工业原料,可以用来生产医用药品,合成染料或香料,用作石油化工的催化剂等。如图是工业制备HBr的一种生产流程:

(1)气体a是燃煤工业的烟道气和工业生产硫酸的尾气的成分,结合框图信息可判断气体a的分子式为___。混合物①中加的水为___(填“冰水”或“热水”),原因是___。
(2)试剂b为含氯的盐,b为___(用化学式表示),混合②的目的是___。第二次蒸馏后的“含c的溶液”中c为___。
(3)生产流程中操作A的名称___,实验室中蒸馏操作是在___中进行的。(填玻璃仪器名称)
(4)工业生产中制得的氢溴酸带有淡淡的黄色。于是甲、乙两同学设计了实验加以探究:①甲同学假设工业氢溴酸呈淡黄色是因为含有Fe3+,则用于证明该假设所用的试剂为___(填化学式),若假设成立可观察到的现象为___。
②乙同学假设工业氢溴酸呈淡黄色是因为其中含有杂质___,用于证明该假设成立的方法为___(简单写出实验步骤)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂生产新型清洁燃料甲醚(CH3-O-CH3)的流水线反应原理为:在 10L 的反应容器内进行的反应①的化学平衡常数表达式为K=[CO][H2]/[H2O]。反应②的热化学方程式为:3H2(g)+3CO(g)CH3OCH3(g)+CO2(g)+Q。反应③为:CO2+NH3+H2O→NH4HCO3,完成下列填空:
(1)反应①的方程式为______。经3min反应容器内的水蒸气从20.0mol变为 2.0mol,则此 3min 内 CO 的平均反应速率V(CO)=______。
(2)能判断反应①已达化学平衡状态的是(选填编号)______。
A.在消耗 n 摩尔氢气的同时产生 n 摩尔的水
B.容器内气体的平均相对分子质量保持不变
C.容器内所有的物质的总物质的量保持不变
D.化学反应速率:V(逆)(H2O)=V(正)(CO)
(3)已知升高温度,反应②的化学平衡常数会减小,则反应②的热化学方程式中的Q(选填“>”或“<”)______0。该反应的逆反应速率V(逆)随时间 t 变化的关系如图一所示,则在 t2时改变的反应条件是______。
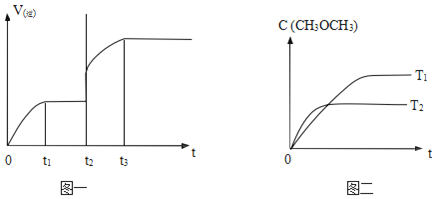
(4)在不同温度下,反应容器内甲醚(CH3OCH3)的浓度c(CH3OCH3)随时间t 变化的状况如图二所示。则反应温度 T1(选填“>”、“=”或“<”)______T2。
(5)若反应③得到的是一种纯净常见化肥的溶液。经测定溶液中也存在 NH3H2O 分子和CO32-离子,试用化学用语表示产生这两种微粒的原因:______,______。相同温度下,都为 0.1mol/L的 NaHCO3溶液甲和 NH4HCO3溶液乙相比较,溶液中c(CO32-)甲(选填“>”、“=”或“<”)甲______乙。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,无水四氯化锡是一种无色易挥发、易流动的液体,遇水极易发生水解。某学习小组设计了下图所示的装置制备无水四氯化锡。其反应原理是 Sn(s)+2Cl2(g)=SnCl4(l) △H=-511kJ/mol
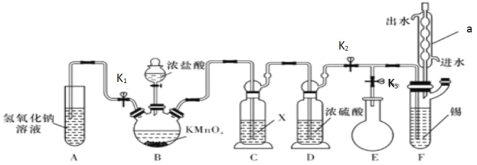
请回答下列问题:
(1)仪器 a 的名称是_____。
(2)装置 C 中所用试剂 X 是_____,装置 D 的作用是_____。
(3)装置 B 中发生反应的离子方程式是_____。
(4)利用该反应制取 Cl2 相对于用二氧化锰和浓盐酸反应的优点是:_____。
(5)若要制取5mol含氯气的物质的量分数为20%的SnCl4,则至少需通入的氯气(标准状况下)的体积为______
(6)上述实验设计中,还有一些不合理之处,请写出一点:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示。下列有关叙述中,正确的是
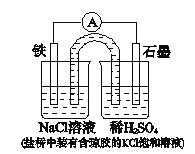
A.Fe作正极,发生氧化反应
B.负极反应: 2H+ + 2e-=H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.工作一段时间后,NaCl溶液中c(Cl-)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A. Cu与Cu2O的物质的量之比为2∶1 B. 硝酸的物质的量浓度为2.6mol/L
C. 产生的NO在标准状况下的体积为4.48L D. Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+ ![]() O2(g)=H2O(g);ΔH1= akJ·mol-1
O2(g)=H2O(g);ΔH1= akJ·mol-1
②2H2(g)+O2(g) = 2H2O(g);ΔH2= b kJ·mol-1 ③ H2(g)+ ![]() O2(g)=H2O(l);ΔH3= c kJ·mol-1
O2(g)=H2O(l);ΔH3= c kJ·mol-1
④2H2(g)+O2(g) = 2H2O(l);ΔH4= d kJ·mol-1,下列关系式中正确的是( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由菱镁矿(主要成分为MgCO3、CaCO3、FeCO3、SiO2)制备高纯Mg(OH)2的一种工艺如下:
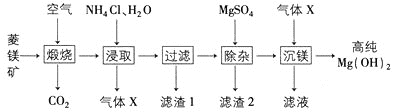
下列说法不正确的是
A.“煅烧”时FeCO3发生反应为4FeCO3+O2![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
B.“浸取”产生的气体X为NH3
C.“滤渣1”“滤渣2”分别为SiO2、CaSO4
D.“沉镁”所得的固体是否洗涤干净可用BaCl2溶液检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲乙丙丁戊是中学常见的无机物,他们的转化关系如图所示![]() 某些条件和部分产物已略去
某些条件和部分产物已略去![]() 下列说法错误的是
下列说法错误的是![]()
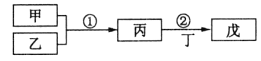
A.若戊为一种强碱且焰色反应为黄色,则反应![]() 可能都属于氧化还原反应
可能都属于氧化还原反应
B.常温下,若丙为无色气体,戊为红棕色气体,则甲、乙是铜和稀硝酸
C.若甲为硫磺燃烧产物,丁为水,则戊可用于干燥甲
D.若甲为浓盐酸,乙为![]() ,则戊可能使品红褪色
,则戊可能使品红褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com