
【题目】将锌棒和铜棒插入西红柿中,电流表指针发生偏转,如图所示,下列说法正确的是( )

A. 负极反应为Zn-2e-==Zn2+
B. 该装置将化学能转化为电能
C. 电流由锌通过导线流向铜棒
D. 一段时间后,锌棒质量会增加
科目:高中化学 来源: 题型:
【题目】人类逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”。下列错误的是( )
A. 煤、石油和天然气都属于碳素燃料B. 发展太阳能经济有助于减缓温室效应
C. 太阳能电池将太阳能直接转化为电能D. 菠菜蛋白质“发电”不属于“太阳能文明”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某市售照明材料LED晶片是一种发光二极管。材质组成为:GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、GaInN(氮化镓铟)等。请回答下列问题:
(1)砷基态原子的核外电子排布式为______________________。
(2)上述非金属元素氢化物的沸点从高到低的顺序为___________。
(3)下列说法正确的是___________
a.电负性:As<Ga b.SiC与GaAs互为等电子体 c.第一电离能:As>Se>Ga
(4)如图所示为GaAs的晶胞结构,晶体熔点为1237℃。
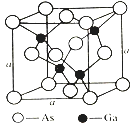
①晶胞中砷与镓原子间的化学键类型有___________。
②一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是___________。
③一个晶胞的组成为___________。
④已知晶胞棱长a=5.64×10-10m,则该晶胞密度为ρ=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组辨析以下说法:①粗盐和酸雨都是混合物;②非金属氧化物一定都是酸性氧化物;③冰和干冰既是纯净物又是化合物;④Na2O、Na2O2都是钠的氧化物,都是碱性氧化物;⑤磷酸和醋酸都是多元酸;⑥纯碱和烧碱都是碱。其中正确的是( )
A.②③⑥B.①②④C.①③D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[选修5:有机化学基础]扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F的路线如下:

(1)A可发生银镜反应,且具有酸性,A的结构简式为____________。B的分子式为C6H6O,则A与B所发生反应的类型为___________。
(2)C生成D的化学方程式为_____________________________。E是由2分子C生成的含有3个六元环的化合物,E的结构简式为______________。
(3)1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为_______mol。符合下列条件的F的同分异构体(不考虑立体异构)共有______种。
①苯环上只有2个取代基且处于对位,其中一个是羟基;
②在稀H2SO4中或NaOH溶液中加热均能发生水解反应;
③能发生银镜反应。
(4)已知:R—CH2—COOH![]()
![]() ,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
,A有多种合成方法,在下面的空格处写出由乙酸合成A的路线流程图(其他原料任选)。合成路线流程图示例如下:
H2C===CH2![]() CH3CH2OH
CH3CH2OH![]() CH3COOC2H5
CH3COOC2H5
_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲~辛戊均为人体必需的短周期非金属元素,在周期表中的相对位置如下表,下列判断正确的是 ( )

A. 非金属性:丙>庚
B. 原子半径:甲>乙
C. 原子最外层电子数:辛>己
D. 最高价氧化物对应水化物酸性:戊>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。
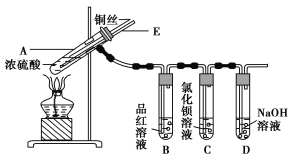
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为____________________________________________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_______________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ________ | ________ |
写出其SO2表现还原性的离子反应方程式:______________________________________。
(4) 装置D的作用__________________________________________________________ 。
(5)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1mL1.0mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
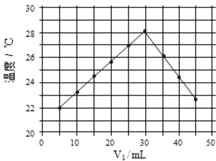
A. 做该实验时环境温度为22℃ B. 该实验表明热能可转化为化学能
C. NaOH溶液的浓度约为1.5mol·L-1 D. 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1L 0.4mol/L HN03溶液中加入Fe粉和Cu粉的混合物9g,充分反应,放出NO气体且金属有剩余。则反应后溶液中c(NO3-)为(忽略溶液体积的变化)
A. 0. 2mol/L B. 0.225 mol/L C. 0.3mol/L D. 0.325 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com