
【题目】如图有关图示分析正确的是( )
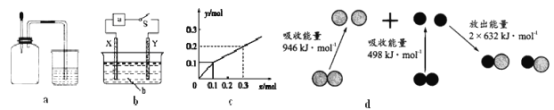
A. 如图a所示,集气瓶内充満Cl2和CH4的混合气体或NO2和O2的混合气体,置于光亮处,将滴管内的水挤入集气瓶后,焼杯中的水会迸入集气瓶,并可能充满集气瓶
B. 如图b所示,X为铁棒,Y为铜棒,M为直流电源,当S闭合后,当b为NaOH溶液,X极附近产生白色沉淀时,电子从X极流入M
C. Pt内电极, 电解含0.10 mol M+和0.1 molN3+ (M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如图c,离子氧化能力M+>N3+>H+
D. 图d为N2(g)和O2(g)生成NO(g)过程中的能量変化,则N-N的键能为946kJ·mol-1,其热化学方程式为N2(g)+O2(g)=2NO(g) △H=-180 kJ·mol-1
【答案】B
【解析】A.生成的一氯甲烷不溶于水;B.X为铁棒,X极附近产生白色沉淀时,可以知道Fe为阳极失去电子,电子从负极流向正极;C.通过0.2mol 电子时生成0.1molY,则应该是氢离子放电,而N3+不放电,氧化性最弱;D.由图可以知道,反应热=946+498-2×632=180 kJ·mol-1;以此来解答。
因为甲烷与氯气的反应中可能产生一氯甲烷气体,而一氯甲烷不溶于水,则水不可能充满集气瓶,A错误;X极附近产生白色沉淀,这说明X电极是铁电极,与电源的正极相连,作阳极失去电子转化为亚铁离子,因此电子从X极流入a,B正确;根据图象可以知道通过0.10mol电子时产生0.1molY,这说明应该是M+放电.再通过0.2 mol电子时生成0.1molY,则应该是氢离子放电,所以离子氧化能力M+>N3+>H+,C错误;图d为N2(g)和O2(g)生成NO(g)过程中的能量変化,氮气含有三键,键能大于氧气中键能,则N≡N的键能为946kJ·mol-1,反应热=946+498-2×632=180 kJ·mol-1,所以热化学方程式为N2(g)+O2(g)=2NO(g)△H=+180kJ·mol-1,D错误;正确选项B。


科目:高中化学 来源: 题型:
【题目】羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
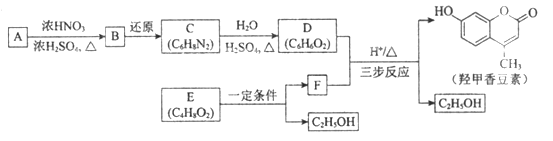
己知:
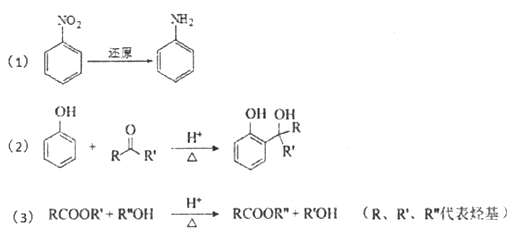
请回答下列问题:
(1)A属于芳香烃,其结构简式是____________;B中所含的官能团是____________。
(2)C→D的反应类型是____________。
(3)E属于酯类。仅以乙醇为有机原料,选用必要的无机试剂合成E,写出有关化学方程式____________。
(4)己知:2E![]() F+C2H5OH。F所含官能团有
F+C2H5OH。F所含官能团有![]() 和____________。
和____________。
(5)以D和F为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式:________
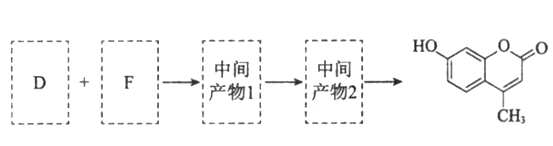
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中充入A(g)和B(g),发生反应A(g)+B(g) ![]() 2C(g)+D(s),所得实验数据如下表:
2C(g)+D(s),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(A) | n(B) | n(C) | ||
① | 600 | 0.30 | 0.20 | 0.30 |
② | 700 | 0.20 | 0.30 | 0.24 |
③ | 800 | 0.10 | 0.10 | a |
下列说法不正确的是
A. 实验①中,若5min时测得n(B)=0.050mol,则0至5min时间内平均反应速率v(A)=0.015mol/(L·min)
B. 实验②中达到平衡后,增大压强,A的转化率不变,平衡常数不变
C. 700℃时该反应的平衡常数K=4.0
D. 实验③中,达到平衡时,a>0.10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)某短周期元素组成的分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结
构,原子间以单键相连。下列有关说法中错误的是(________)
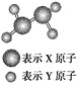
A.X原子可能为ⅤA族元素
B.Y原子一定为ⅠA族元素
C.该分子中,既含极性键,又含非极性键
D.从圆球的大小分析,该分子可能为N2F4
(2)若上述模型中Y原子最外层达到2电子稳定结构且其相对分子质量与O2相同,则该物质的分子式为______________,它与P2H4常温下均为气体,但比P2H4易液化,常用作火箭燃料,其主要原因是______________________________________________________________________。
Ⅱ.已知X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键,试推断:
(1)X、Z两种元素的元素符号:X___________________________________________、
Z______________________。
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________,它的共价键属于________(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为________;含有极性共价键和非极性共价键的化合物的电子式为________________________________。
(3)由X、Y、Z所形成的常见离子化合物是__________(写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为___________________________________________________________________________________________;
X与W形成的化合物与水反应时,水是_____________________________________
(填“氧化剂”或“还原剂”)。
(4)用电子式表示W与Z形成W2Z的过程: __________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学选修3—有机化学基础)
8羟基喹啉被广泛用作金属离子的络合剂和萃取剂,也是重要的医药中间体。下图是8羟基喹啉的合成路线。
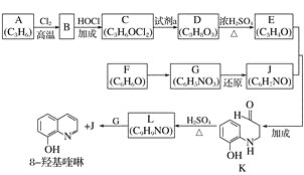
已知:ⅰ.![]()
ⅱ.同一个碳原子上连有2个羟基的分子不稳定。
(1)按官能团分类,A的类别是________________。
(2)A→B的化学方程式是________________。
(3)C可能的结构简式是________________。
(4)C→D所需的试剂a是________________。
(5)D→E的化学方程式是________________。
(6)F→G的反应类型是________________。
(7)将下列K→L的流程图补充完整:
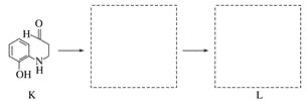 ___________________________
___________________________
(8)合成8羟基喹啉时,L发生了________(填“氧化”或“还原”)反应。反应时还生成了水,则L与G物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘富集在海藻中,我国海带产量居世界第一,除供食用外,大量用于制碘。提取碘的途径如下所示:
干海带![]() 海带灰
海带灰![]() 水溶液
水溶液![]()
![]()
![]() ―→碘单质
―→碘单质
下列有关叙述正确的是( )
A. 碘元素在海水中也有游离态存在 B. 在提取的过程中用的氧化剂可以是H2O2
C. 操作A是结晶或重结晶 D. B是提纯操作,常用蒸馏或分馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化镁用于制药工业,还是重要的绿色阻燃剂。
I、治疗胃酸过多药物Stmoache的有效成分为Mg(OH)2。
(1)该药物治疗胃酸(主要成分为盐酸)过多症时反应的离子方程式:___________。
Ⅱ、已知:Mg (s)+2H2O(g)=Mg(OH)2(s)+H2(g) △H1=-441kJ·mol-1
H2O(g)=H2(g)+![]() O2(g) △H2=+242kJ·mol-1
O2(g) △H2=+242kJ·mol-1
Mg(s)+![]() O2(g)=MgO(s) △H3=-602kJ·mol-1
O2(g)=MgO(s) △H3=-602kJ·mol-1
(2)氢氧化镁分解的热化学方程式是___________。
(3)氢氧化镁可以作为阻燃剂的原因_________。(写一条即可)
Ⅲ、某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。
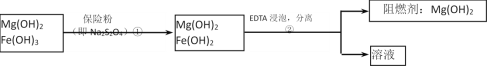
(4)步骤②中分离操作的名称是__________。
(5)步骤①中的反应如下:6Fe(OH)3 +S2O42-+2OH- =6Fe(OH)2 +2SO42-+4H2O。每消耗0.1mol保险粉(Na2S2O4)时,转移电子的数目是__________mol。
(6)已知EDTA只能与溶液中的Fe2+反应生成易溶于水的物质,不与Mg(OH)2反应。虽然Fe(OH)2难溶于水,但步骤②中随着EDTA的加入,最终能够将Fe(OH)2除去并获得纯度高的Mg(OH)2。请从沉淀溶解平衡的角度加以解释。
_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化铁是合成草酸铁的重要原料。
利用工业FeCl3制取纯净的草酸铁晶体[Fe2(C2O4)3·5H2O]的实验流程如下图所示:

(1)抑制FeCl3水解,溶液X为___________。
(2)流程中FeCl3能被异丙醚萃取,其原因是__________________________;检验萃取、分液后所得水层中是否含有Fe3+的方法是_______________________________________。
(3)得Fe2(C2O4)3·5H2O需用冰水洗涤,其目的是________________________。
(4)为测定所得草酸铁晶体的纯度,实验室称取a g样品,加硫酸酸化,用KMnO4标准溶液滴定生成的H2C2O4,KMnO4标准溶液应置于下图所示仪器_____(填“甲”或“乙”)中。
![]()
下列情况会造成实验测得Fe2(C2O4)3·5H2O含量偏低的是_____________。
a.盛放KMnO4的滴定管水洗后未用标准液润洗
b.滴定管滴定前尖嘴部分有气泡,滴定后消失
c.滴定前仰视读数,滴定后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】动物油和植物油的不同之处是( )
A. 前者给人体提供的热量多,后者给人体提供的热量少
B. 前者是高分子化合物,后者不是
C. 前者的烃基是较饱和的,后者的烃基是较不饱和的
D. 前者能水解,后者不能水解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com