
����Ŀ���塢����Ҫ�����ں�ˮ�У��С�����Ԫ�ء������ơ���ˮ�еĵ⸻���ں����У��ҹ����������������һ������ʳ���⣬���������Ƶ⡣��ȡ���;��������ʾ��
�ɺ���![]() ������
������![]() ˮ��Һ
ˮ��Һ![]()
![]()
![]() �D���ⵥ��
�D���ⵥ��
�����й�������ȷ����(����)
A. ��Ԫ���ں�ˮ��Ҳ������̬���� B. ����ȡ�Ĺ������õ�������������H2O2
C. ����A�ǽᾧ���ؽᾧ D. B���ᴿ������������������
���𰸡�B
��������
A.��Ԫ���ں�ˮ��ֻ�л���̬��
B.˫��ˮ����ɫ�����������Խ�����������Ϊ�ⵥ����
C.�ӵ��Լ��ε�ˮ��Һ�л�õⵥ�ʿ�������ȡ�ķ�����
D.ʵ�ֵⵥ�ʺ���ȡ���ķ�����Ը��ݵ���������������������
A.��Ԫ���ں�ˮ��ֻ�л���̬��û������̬����A������
B.˫��ˮ����ɫ�����������Խ�����������Ϊ�ⵥ��������ȡ�Ĺ������õ�������������H2O2����B��ȷ��
C. ������ͼ��Ϣ֪����ˮ������̬�ĵⱻ�����ɵⵥ�ʣ�����ȡ�ķ����õ������ȡ������Һ��������A����ȡ����C������
D. ����������B����ʱ����ʹ��������������D������
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������������������ȼ�գ����û������100mL 3.00mol/L��NaOH��Һ���ܶ�Ϊ1.12g/mL��ǡ����ȫ���գ������Һ�к���NaClO�����ʵ���Ϊ0.0500mol��
��1��ԭNaOH��Һ����������Ϊ
��2��������Һ��Cl�������ʵ���Ϊ mol
��3�����������Ͳμӷ�Ӧ�����������ʵ���֮��n(Cl2)��n(H2)�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں����µ��ܱ������У��п��淴Ӧ2NO��g��+O2��g��![]() 2NO2��g��������<0������˵���Ѵﵽƽ��״̬����
2NO2��g��������<0������˵���Ѵﵽƽ��״̬����
A. ����Ӧ����NO2�����ʺ��淴Ӧ����O2���������
B. ���������ɫ��dz���ֲ���
C. ��Ӧ����ѹǿ����ʱ��仯���仯
D. �������ƽ�����������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и�������(����ָ��������)�ܴ���������ǣ� ��
A. ������Һ��Na����Fe3����Cl����NO3��
B. NH4����Na����NO3����SiO32��
C. ��ѿ����Һ�У�SO42����MnO4����K����H�����Դ�������
D. 0.1mol /LNH4HCO3��Һ�У�K����Na����NO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�й�ͼʾ������ȷ���ǣ� ��
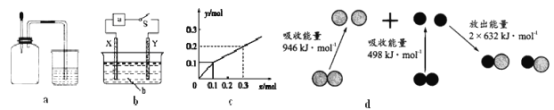
A. ��ͼa��ʾ,����ƿ�ڳ䜺Cl2��CH4�Ļ�������NO2��O2�Ļ������,���ڹ�����,���ι��ڵ�ˮ���뼯��ƿ�����е�ˮ����뼯��ƿ�������ܳ�������ƿ
B. ��ͼb��ʾ,XΪ����,YΪͭ��,MΪֱ����Դ,��S�պϺ�,��bΪNaOH��Һ,X������������ɫ����ʱ,���Ӵ�X������M
C. Pt�ڵ缫, ��⺬0.10 mol M+��0.1 molN3+ (M+��N3+��Ϊ����������)����Һ,���������������ʻ�����������ʵ���(y)�뵼����ͨ�����ӵ����ʵ���(x)�Ĺ�ϵ��ͼc,������������M+>N3+>H+
D. ͼdΪN2(g)��O2(g)����NO(g)�����е������仯,��N-N�ļ���Ϊ946kJ��mol-1,���Ȼ�ѧ����ʽΪN2(g)+O2(g)=2NO(g) ��H=-180 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y�����γɻ�����XY2�������й���������ȷ����( )
A. ��XY2�ǹ��ۻ������X��Y��ԭ�������������1
B. ��XY2�����ӻ������X��Y��ԭ�������������8
C. ��X��Y��ԭ���������5�������ӻ�����XY2��X�����Ӱ뾶��Y���Ӱ뾶С
D. ��X��Y��ԭ���������6���ۻ�����XY2������ǿ����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. Ԫ�����ڱ��У�����һ�͵��������⣬��n���������ǽ���Ԫ��(����ϡ������Ԫ��)��������Ϊ(8��n)
B. SiCl4��PCl3�����и�ԭ���������ﵽ8�����ȶ��ṹ
C. M�������Ϊ����������Ԫ����������������Ԫ��ԭ�ӵ�M���������һ�����
D. ����A�����A�������Ԫ���γɵ�ԭ�Ӹ�����Ϊ1��1����������Ϊ38�Ļ�����Ǻ��й��ۼ��������ͻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��Ȼ�ѧ����ʽ��д���Ӧ��������ȷ����
A. ϡ������0.1 mol/L NaOH ��Һ��Ӧ��H+(aq)+OH��(aq)= H2O(l) ��H = +57.3 kJ��mol1
B. ��֪ 2C(s)+O2(g)=2CO(g)��H= -221 kJ��mol-1�� ���֪ C ����ֵΪ 110.5 kJ��mol1
C. 0�桢30MPa �£��� 0.5mol N2 �� 1.5molH2 �����ܱյ������г�ַ�Ӧ���� NH3(g)������ 19.3kJ�� ���Ȼ�ѧ����ʽΪ��N2(g) + 3H2(g) ![]() 2NH3(g) ��H= -38.6kJ��mol1
2NH3(g) ��H= -38.6kJ��mol1
D. �ܱ������У�0.3mol ����� 0.2mol ���ۻ�ϼ������������� 0.2mol ʱ���ų� 19.12 kJ ������ �� Fe(s)+S(s)=FeS(s)��H= - 95.6 kJ��mol1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ƽ�ȩ��NaHSO2HCHO2H2O���׳Ƶ��飬��ӡȾ��ҽҩ�Լ�ԭ���ܹ�ҵ���й� ��Ӧ�á��� Na2SO3��SO2��HCHO��п��Ϊԭ���Ʊ����������Ƽ�ȩ��ʵ�鲽�����£� ��֪�����������Ƽ�ȩ������ˮ�������Ҵ�������ǿ��ԭ�ԣ����� 120�����Ϸ����ֽ⡣
���� 1����������ƿ�м���һ���� Na2SO3 ��ˮ�������ܽ⣬����ͨ�� SO2������Һ pH ԼΪ 4���Ƶ� NaHSO3��Һ��
���� 2����װ�� A �е����ܻ�����Ƥ��������ƿ�м����Թ�����п�ۺ�һ������ȩ��Һ���� 80��90���£� ��ӦԼ 3h����ȴ�����£����ˣ�
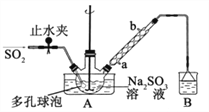
���� 3������Һ�������Ũ������ȴ�ᾧ��
��1��װ�� B���ձ���Ӧ�������Һ��_________������������ȴˮ��_______����a������b�����ڽ�ˮ��
��2��A �ж�����ݵ�������________��
��3���������л�������Ҫ���ʳ� H2O ���________���ѧʽ����
��4��д������ 2 �з�����Ӧ�Ļ�ѧ����ʽ________��
��5������ 3 �����������������Ũ����ԭ����________��
��6��Ϊ�˲ⶨ��Ʒ�Ĵ��ȣ�ȷ��ȡ 2.0g ��Ʒ����ȫ����ˮ��� 100mL ��Һ��ȡ 20.00mL ������Һ�� �����������ȫ��Ӧ����֪ I2 ����������ȩ�����ʲ���Ӧ�������� BaCl2 ��Һ��������ȫ�����ˡ�ϴ�ӡ� ���������صõ���ɫ���� 0.466g�������ƵõIJ�Ʒ�Ĵ���Ϊ________ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com