
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小
D.甲的相对分子质量比乙的相对分子质量小
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】甲基丙烯酸甲酯(MMA)是聚甲基丙烯酸甲酯(有机玻璃)的单体,也用于制造其他树脂、塑料、涂料、粘合剂和润滑剂等.MMA的合成路线如图所示(反应条件和试剂略).
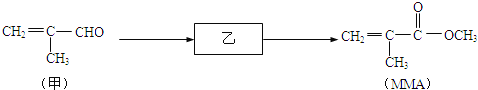
请回答:
(1)甲分子中所含官能团的名称是 .
(2)MMA的分子式是 .
(3)乙的结构简式是 .
(4)MMA在一定条件下生成聚甲基丙烯酸甲酯的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在27.5 g水中溶解12.5 g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21 g/cm3,求:
(1)该溶液中阴阳离子的总物质的量(结果保留三位有效数字,下同);
(2)取出20.0 mL该溶液,配成溶度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作叙述正确的是( )
A. 实验用剩的药品应放回原试剂瓶中
B. 切割白磷时应该在水下进行
C. 测某酸性溶液的pH时,先用水将pH试纸湿润
D. 在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 0.4mol/L AgNO3 溶液,0.3mol/L MgCl2 溶液和 0.2mol/L 的 AlCl3 溶液按 3:2:1 的体积相混合静置后, 上层清夜中 Cl-的浓度为(混合后溶液体积变化不计)
A. 0.2mol/L B. 0.1mol/L C. 0.6mol/L D. 0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100g物质的量浓度为18mol/L,密度为ρg/mL的浓硫酸中,加入一定量的水稀释为9mol/L的硫 酸溶液,则加入水的体积是
A.大于100mL B.小于100mL C.等于100mL D.等于100/ρ mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2SO3应用广泛。利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的成本低,优势明显,其流程如下。
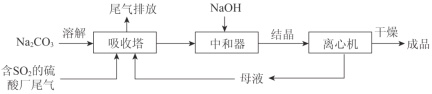
(1)举例说明向大气中排放SO2导致的环境问题:_________。
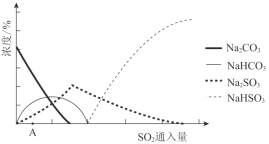
(2)下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是_________。
(3)中和器中发生的主要反应的化学方程式是_________。
资料显示: Ⅰ.Na2SO3在33℃时溶解度最大,将其饱和溶液加热至33℃以上时,由于溶解度降低会析出无水Na2SO3,冷却至33℃以下时析出Na2SO3·7H2O; Ⅱ.无水Na2SO3在空气中不易被氧化,Na2SO3·7H2O在空气中易被氧化。 |
(4)为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
①请结合Na2SO3的溶解平衡解释NaOH过量的原因_________。
②结晶时应选择的最佳操作是_________(选填字母)。
A.95~100℃加热蒸发,直至蒸干
B.维持95~100℃蒸发浓缩至有大量晶体析出
C.95~100℃加热浓缩,冷却至室温结晶
(5)为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是_________、_________。
(6)KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
①滴定终点前反应的离子方程式是:![]() IO3-+
IO3-+![]() SO32- =
SO32- =![]() _______ +
_______ +![]() _______(将方程式补充完整)。
_______(将方程式补充完整)。
②成品中Na2SO3(M = 126 g/mol)的质量分数是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com