
【题目】三硫代碳酸钠(Na2CS3)在农业上用作杀菌剂和杀线虫剂,在工业上用于处理废水中的重金属离子,某化学兴趣小组对Na2CS3的一些性质进行了探究性实验。
实验Ⅰ.探究Na2CS3的性质:
步骤 | 操作及现象 |
① | 取少量Na2CS3固体溶于蒸馏水中,配制成溶液并分成两等份 |
② | 向其中一份溶液中滴加几滴酚酞试剂,溶液变成红色 |
③ | 向另一份溶液中滴加用硫酸酸化的KMnO4溶液,紫色褪去 |
(1)H2CS3是___(填“强”或“弱”)酸。
(2)已知步骤③中反应的氧化产物是SO42-,则该反应的离子方程式为:____。
(3)某同学取步骤③反应后所得溶液于试管中,滴加足量盐酸和氯化钡溶液,他认为通过测定产生的白色沉淀的质量即可求出实验中所用的Na2CS3的质量。你是否同意他的观点,并说明理由:___。
实验Ⅱ.测定Na2CS3溶液的浓度:
按如图所示装置进行实验:将50.0mLNa2CS3溶液置于三颈烧瓶中,打开仪器M的活塞,滴入足量2.0mol·L-1的稀H2SO4,关闭活塞。
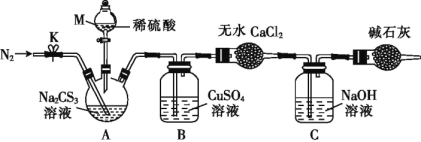
已知:CS32- +2H+=CS2+H2S↑,CS2和H2S均有毒。(CS2不溶于水,沸点为46℃,与CO2的某些性质相似,与NaOH作用生成Na2COS2和H2O)
(4)仪器M的名称是___。反应开始前需要先通入一段时间N2,其作用为____。
(5)B中发生反应的离子方程式为:____。
(6)为了计算三硫代碳酸钠溶液的浓度,可通过测定B中生成沉淀的质量来计算。称量B中沉淀质量之前需要进行的实验操作是___。若B中生成沉淀的质量为8.4g,则Na2CS3溶液的物质的量浓度是____。
【答案】弱 5CS32-+24MnO4-+52H+=15SO42-+5CO2↑+24Mn2++26H2O 不同意,因为步骤③中加入的酸性KMnO4溶液是用H2SO4酸化的,含有SO42-,所以生成的硫酸钡沉淀质量偏大 分液漏斗 排尽装置中的空气,防止生成的H2S被氧化 Cu2++H2S=CuS↓+2H+ 过滤、洗涤、干燥 1.75mol·L-1
【解析】
(1)Na2CS3的水溶液中加入酚酞变红色,说明Na2CS3是强碱弱酸盐;
(2)根据氧化还原反应的规律分析作答;
(3)酸性高锰酸钾溶液用稀硫酸酸化;
(4)根据仪器的图形判断仪器的名称;A中发生Na2CS3+H2SO4=Na2SO4+CS2+H2S↑,生成的硫化氢可与B中的硫酸铜反应生成CuS沉淀;
(5)反应结束后打开活塞k,再缓慢通入热N2一段时间是把生成的硫化氢和二硫化碳全部赶入后面装置完全吸收;
(6)当A中反应完全后,打开K缓慢通入热N2一段时间,然后对B中混合物进行过滤、洗涤、干燥,称重,得8.4黑色固体,根据关系式Na2CS3~H2S~CuS分析计算求得。
(1)Na2CS3的水溶液中加入酚酞变红色,说明Na2CS3是强碱弱酸盐,则H2CS3为弱酸,
故答案为:弱;
(2)步骤③的氧化产物是SO42,还原产物是锰离子,同时还生成二氧化碳、水,离子方程式为5CS32-+24MnO4-+52H+=15SO42-+5CO2↑+24Mn2++26H2O;
(3)酸性高锰酸钾溶液用稀硫酸酸化,所以不能通过计算白色沉淀计算Na2CS3的量,因为步骤③中加入的酸性KMnO4溶液是用H2SO4酸化的,含有SO42-,所以生成的硫酸钡沉淀质量偏大,
故答案为:不同意,因为步骤③中加入的酸性KMnO4溶液是用H2SO4酸化的,含有SO42-,所以生成的硫酸钡沉淀质量偏大;
(4)仪器M的名称为分液漏斗;因H2S为还原性气体,易被空气氧化,故反应开始前需要先通入一段时间N2,排尽装置中的空气,防止生成的H2S被氧化,故答案为:分液漏斗;排尽装置中的空气,防止生成的H2S被氧化;
(5)A中发生Na2CS3+H2SO4=Na2SO4+CS2+H2S↑,生成的硫化氢可与B中的硫酸铜反应生成CuS沉淀,反应的离子方程式为Cu2++H2S=CuS↓+2H+;
(6)当A中反应完全后,打开K缓慢通入热N2一段时间,然后对B中混合物进行过滤、洗涤、干燥,称重,得8.4黑色固体,n(CuS)=![]() ,根据关系式Na2CS3H2SCuS得n(Na2CS3)=n(CuS)=0.0875mol,c(Na2CS3)=
,根据关系式Na2CS3H2SCuS得n(Na2CS3)=n(CuS)=0.0875mol,c(Na2CS3)=![]() = 1.75mol·L-1,
= 1.75mol·L-1,
故答案为:过滤、洗涤、干燥;1.75mol·L-1。


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )
A.相同条件下,质量相等的CO和CO2它们所含的氧原子数目之比为11:7
B.同体积、同密度的C2H4和CO,两种气体的分子数一定相等
C.配制450mL0.1molL-1的NaOH溶液,用托盘天平称取NaOH固体1.8g
D.1L0.45molL-1NaCl溶液中Cl-的物质的量浓度比0.1L0.1 molL-1AlCl3溶液大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某种原子的质量是a g,若NA只表示阿伏伽德罗常数的数值,该原子的相对原子质量为______,b g该原子的物质的量为______mol。
(2)a g A气体与b g B气体分子数相等,同温同压下,气体A与气体B的密度之比为___________。
(3)向10 mL 0.1mol/LNaHCO3溶液中缓缓滴入0.1mol/LCa(OH)2溶液,首先发生反应的两种离子为____________(填离子符号,下同),随后溶液中有白色沉淀生成,生成沉淀的两种离子为____________。当加入少量Ca(OH)2溶液时,发生的离子反应方程式为_______________________。
(4) 将3.22 g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需加入水的质量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )
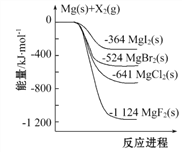
A. 由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方 程式为:MgBr2(s)+Cl2(g)![]() MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
MgCl2(s)+Br2(g) ΔH=+117 kJ·mol-1
B. 热稳定性: MgI2 > MgBr2 > MgCl2 > MgF2
C. 工业上可由电解MgCl2溶液冶炼金属Mg,该过程需吸收热量
D. 金属镁和卤素单质(X2)的反应能自发进行是因为ΔH均小于零
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化锌常用作有机合成的催化剂。实验室采用HCl气体除水、ZnCl2升华相结合的方法提纯市售氯化锌样品(部分潮解并含高纯高温不分解杂质)。实验装置如图所示:
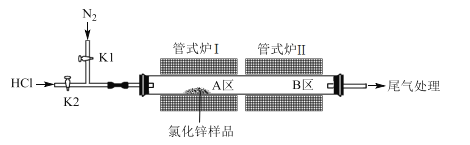
回答下列问题:
(1)无水氯化锌在空气中易潮解生成Zn(OH)Cl的化学方程式为_____。
(2)除水阶段:打开K1,K2。将管式炉I、II升温至150 ℃,反应一段时间后将管式炉I、II的温度升至350 ℃,保证将水除尽。除水阶段发生反应的化学方程式为 ____。
(3)升华阶段:撤去管式炉II,将管式炉I迅速升温至750℃,升温的目的是_____。一段时间后关闭管式炉I并关闭 ____(填K1或K2),待冷却后关闭 ____(填K1或K2)。最后将_____(填A或B)区的氯化锌转移、保存。
(4)除水阶段HCl与 N2流速要快,有利于提高除水效率。升华阶段HCl与N2流速要慢,其原因是_____。
(5)测定市售ZnCl2样品中的锌的质量分数。步骤如下:
① 溶液配制:称取m g样品,加水和盐酸至样品溶解,转移至250 mL的 ____中,加蒸馏水至刻度线,摇匀。
② 滴定:取25.00mL待测液于锥形瓶中,用c mol·L-1K4[Fe(CN)6]标准溶液滴定至终点,消耗V mL。滴定反应为:2K4[Fe(CN)6]+3ZnCl2=K2Zn3[Fe(CN)6]2↓+6KCl该样品中锌的质量分数为 ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四室式电渗析法制备盐酸和NaOH的装置如图所示。a、b、c 为阴、阳离子交换膜。已知:阴离子交换膜只允许阴离子透过,阳离子交换膜只允许阳离子透过。下列叙述正确的是( )
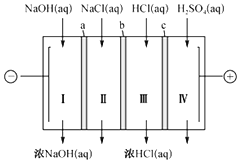
A. b、c 分别依次为阳离子交换膜、阴离子交换膜
B. 通电后Ⅲ室中的Cl-透过c 迁移至阳极区
C. Ⅰ、Ⅱ、Ⅲ、Ⅳ四室中的溶液的pH均升高
D. 电池总反应为4NaCl+6H2O![]() 4NaOH+4HCl+2H2↑+O2↑
4NaOH+4HCl+2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是

A. 选择合适的试剂,用图甲可分别制取少量CO2、CO和SO2
B. 洗涤沉淀时(见图乙),向漏斗中加入适量水至浸没沉淀并滤干,重复2-3次
C. 用图丙所示装置除去HCl中的少量CO2
D. 用图丁装置从KI和I2的固体混合物中回收I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I是一种抗脑缺血药物,合成路线如下:
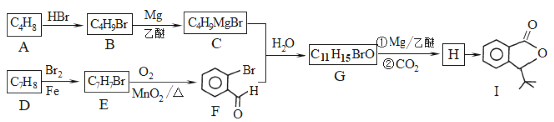
已知:
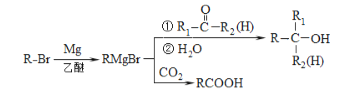
回答下列问题:
(1)按照系统命名法,A的名称是_____;写出A发生加聚反应的化学方程式:__________。
(2)反应H→I的化学方程式为________;反应E→F的反应类型是______。
(3)写出符合下列条件的G的所有同分异构体的结构简式:________
①遇FeCl3溶液发生显色反应 ②核磁共振氢谱有4组峰
(4)α,α-二甲基苄醇(![]() )是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:
)是合成医药、农药的中间体,以苯和2-氯丙烷为起始原料制备α,α-二甲基苄醇的合成路线如下:
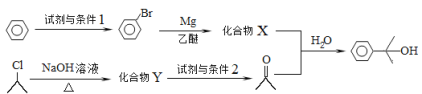
该合成路线中X的结构简式为____,Y的结构简式为________;试剂与条件2为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学研究发现,具有高度对称的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为化学界关注的热点。立体烷烃中有一系列对称结构的烃,如:![]() (正四面体烷C4H4)、
(正四面体烷C4H4)、![]() (棱晶烷C6H6)、
(棱晶烷C6H6)、![]() 立方烷C8H8)等,下列有关说法正确的是
立方烷C8H8)等,下列有关说法正确的是
A. 立体烷烃的C原子都形成4个单键,因此它们都属于烷烃
B. 上述一系列物质互为同系物,它们的通式为C2nH2n(n≥2)
C. 棱晶烷与立方烷中碳原子均为饱和碳原子,其二氯代物的种数不同
D. 苯、盆烯(![]() )与棱晶烷属于同分异构体
)与棱晶烷属于同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com