
【题目】已知A、B为单质,C为化合物,能实现上述转化关系的是( )
![]()
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A. ①② B. ①③ C. ②④ D. ③④
【答案】C
【解析】
试题从![]() 转化关系可知,电解电解质溶液时,是电解电解质本身,因此C可以为不活泼金属的无氧酸盐或无氧酸。①若A为钠,则B为氧气,则C为过氧化钠,C的水溶液为氢氧化钠,电解氢氧化钠得到氢气和氧气,不符合转化关系,故①错误;②若C的溶液遇Na2CO3,放出CO2气体,则C可以为HCl、HBr、HI等,电解这些酸的水溶液实际上是电解本身,在阴极得到氢气,故A可能是H2,B可能为卤素单质,故②符号上述转化关系,故②正确;③若C的溶液中滴加KSCN溶液显红色,则C中含铁离子,电解铁盐不会得到铁单质,故③错误;④由C的溶液中滴加NaOH溶液有蓝色沉淀生成,则C为铜盐,C可以为卤化铜,如氯化铜、溴化铜等,电解他们的水溶液都会得到铜和卤素单质,故B可以为铜,故④正确;故选C。
转化关系可知,电解电解质溶液时,是电解电解质本身,因此C可以为不活泼金属的无氧酸盐或无氧酸。①若A为钠,则B为氧气,则C为过氧化钠,C的水溶液为氢氧化钠,电解氢氧化钠得到氢气和氧气,不符合转化关系,故①错误;②若C的溶液遇Na2CO3,放出CO2气体,则C可以为HCl、HBr、HI等,电解这些酸的水溶液实际上是电解本身,在阴极得到氢气,故A可能是H2,B可能为卤素单质,故②符号上述转化关系,故②正确;③若C的溶液中滴加KSCN溶液显红色,则C中含铁离子,电解铁盐不会得到铁单质,故③错误;④由C的溶液中滴加NaOH溶液有蓝色沉淀生成,则C为铜盐,C可以为卤化铜,如氯化铜、溴化铜等,电解他们的水溶液都会得到铜和卤素单质,故B可以为铜,故④正确;故选C。


科目:高中化学 来源: 题型:
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题。
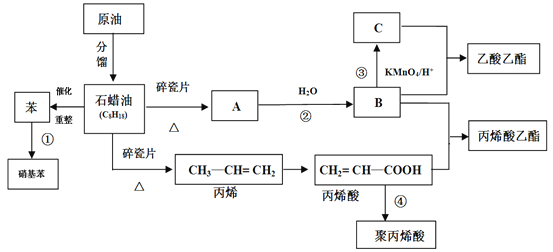
(1)A的结构简式为________。
(2)丙烯酸中含氧官能团的名称为_______。
(3)①③反应的反应类型分别_______、_______。
(4)写出下列反应方程式
①反应②的方程式_____________________;
②反应④的方程式_____________________;
③丙烯酸+B→丙烯酸乙酯________________。
(5)丙烯酸(CH2=CH—COOH)的性质可能有_______
①加成反应 ②取代反应 ③加聚反应 ④中和反应 ⑤氧化反应
A.只有①③ B.只有①③④
C.只有①③④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)![]() H2(g)+I2(g)△H > 0,H2物质的量随时间的变化如图所示。
H2(g)+I2(g)△H > 0,H2物质的量随时间的变化如图所示。
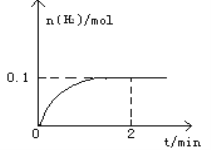
(1)2 min时HI的转化率a(HI)=____________________。该温度下,H2(g)+I2(g)![]() 2HI(g)的平衡常数K=________________。
2HI(g)的平衡常数K=________________。
(2)下列哪种情况能说明该反应已经达到平衡状态(___________)
A.气体的密度不再变化了
B.气体的颜色不再变化了
C.气体的总压强不再变化了
D.相同时间内消耗氢气的质量和生成碘的质量相等
E.单位时间内消耗氢气和消耗碘化氢的物质的量相等
F.氢气的质量分数不变了
(3)在恒容绝热(不与外界交换能量)条件下进行2A(g)+B(g) ![]() 2C(g)+D(s)反应,该反应的平衡常数的表达式K=____________________,按下表数据投料:
2C(g)+D(s)反应,该反应的平衡常数的表达式K=____________________,按下表数据投料:
物质 | A | B | C | D |
起始投料/mol | 2 | 1 | 2 | 0 |
反应达到平衡状态,测得体系压强升高。该反应△H____0(填“>”、“<” 或者“=”),简述该反应的平衡常数与温度的变化关系:__________________________________________________。
(4)该反应如果把D的物质的量增大一倍,逆反应速率________(填“增大”、“减小” 或者“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
A. 2.0 mol·L-1 B. 1.5 mol·L-1 C. 0.18 mol·L-1 D. 0.24 mol·L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法不正确的是( )
A.乙醇和乙酸都是常用调味品的成分
B.乙醇、乙烷和乙酸都可与钠反应生成氢气
C.“酒越陈越香”与酯化反应有关
D.乙醇与甲醚(CH3OCH3)互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含2mol NaOH、1mol Ba(OH)2、2mol NaAlO2的混合液中慢慢通入CO2至过量,下列有关说法正确的是

A. 整个过程中共发生四个离子反应。
B. 根据现象可判断酸性强弱为:H2CO3>HAlO2>HCO3-
C. 通入3molCO2和通入5molCO2都只产生3mol沉淀
D. 整个过程中生成沉淀的物质的量与通入CO2的体积的图象如图所示:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家积极探索新技术对CO2进行综合利用。
Ⅰ.CO2可用FeO吸收同时获得H2。
i. 6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) △Hl=-76.0 kJ·mol-1
ⅱ. C(s)+2H2O(g)=CO2(g)+2H2(g) △H2= +113.4 kJ·mol-1
(1)则3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=_________。
Ⅱ.CO2可用来生产燃料甲醇。
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。在体积为1L的恒容密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(2)从反应开始到平衡,氢气的平均反应速率v(H2)=_________ mol·(L·min) -1。
(3)氢气的转化率=________________________。
(4)该反应的平衡常数为______________________(保留小数点后2位)。
(5)下列措施中能使平衡体系中n(CH3OH)/n(CO2)增大的是_________________。
A.升高温度 B.充入He(g),使体系压强增大
C.再充入1 mol H2 D.将H2O(g)从体系中分离出去
(6)当反应达到平衡时,CH3OH的体积分数为m1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,CH3OH的体积分数为m2,则m1________m2的关系(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在无色透明溶液中能大量共存的是
A.NH4+、Mg2+、SO42-、Cl-B.Na+、H+、SO32-、Cl-
C.Na+、Cu2+、SO42-、OH-D.Na+、Ca2+、Cl-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com