
����Ŀ���ȼ��ⱥ��ʳ��ˮ��ȡNaOH�Ĺ�������ʾ��ͼ���£�
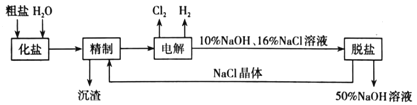
������ͼ�����������գ�
��1���Ӻ�ˮ�л�ȡ���εķ�����___��
��2���������������У�����ȥ����ˮ�е�Ca2+��Mg2+��SO42-���ɽ��еIJ����У�
A. ����
B. �ӹ���BaCl2��Һ
C. ������ϡ����
D. �ӹ���NaOH��Һ
E. �ӹ���Na2CO3��Һ
����ȷ������˳����___(����ĸ)��
�ڲ���B��Ŀ����___
�۲���C��Ŀ����___
�ܲ���D�з�����Ӧ�����ӷ���ʽ��___
�ݴ˲����е�ϡ�����ܷ���ϡ�������?____(����������������)��������___��
��3������������������Һ����Ȼ����NaCl�ķ�����___���۲쵽��������___��
��4���������������У�ͨ������Ũ������ȴ�ᾧ��___�ķ�����ȥNaCl���÷�����ԭ������ͬ�¶���NaCl��NaOH���ܽ�Ȳ�ͬ���ڸò����¶��£��ܽ�Ƚϴ����___��
��5�����������п�ѭ��ʹ�õ�������______��(�ѧʽ)��
���𰸡������ᾧ BDEAC(��BEDAC) ��ȥ��Һ��SO42- ��ȥ��Һ�е�̼���ƺ��������� Mg2++2OH-= Mg(OH)2�� �� ������NO3-���� ȡ�����������Һ�������е���ϡ�����ữ���ٵμ���������Һ �μ���������Һ�������ɫ���� ���� NaOH NaCl��NaOH
��������
(1)���ݴ���Һ�л�����ʵķ����������
(2)��ȥ����ˮ�е�Ca2+��Mg2+��SO42-��һ�����NaOH��Һ�dz�ȥþ���ӣ���BaCl2��Һ�dz�ȥ��������ӣ���Na2CO3��Һ�dz�ȥ�����Ӻ����ı����ӣ���ˣ�Na2CO3��Һһ����BaCl2��Һ֮����룬Ϊ�˲�ʹ�����ij����ܽ⣬һ��Ҫ�ڹ��˺��ټ�����ݴ˷������
(3)����������������Һ����Ȼ����NaCl��ֻ��Ҫ���麬�������Ӽ��ɣ�
(4)��ͬ�¶���NaCl��NaOH���ܽ�Ȳ�ͬ���Ȼ��Ƶ��ܽ�������¶ȱ仯�������������ܽ�Ƚϴ������¶ȵı仯�ϴݴ˷������
(5)��������ͼ���������п�ѭ��ʹ�õ����ʡ�
(1)�Ӻ�ˮ�л�ȡ���Σ�����ͨ�������ᾧ�ķ����õ����ʴ�Ϊ�������ᾧ��
(2)���������������У���ȥ����ˮ�е�Ca2+��Mg2+��SO42-������NaOH��Һ�dz�ȥþ���ӣ���BaCl2��Һ�dz�ȥ��������ӣ���Na2CO3��Һ�dz�ȥ�����Ӻ����ı����ӣ���ˣ�Na2CO3��Һһ����BaCl2��Һ֮����룬Ϊ�˲�ʹ�����ij����ܽ⣬һ��Ҫ�ڹ��˺��ټ����ᣬ��ȷ������˳����BDEAC��BEDAC���ʴ�Ϊ��BDEAC(��BEDAC)��
�ڲ���B�ӹ���BaCl2��Һ��Ϊ�˳�ȥ��������ӣ��ʴ�Ϊ����ȥ��Һ��SO42-��
�۲���C������ϡ���ᣬΪ�˳�ȥ��Һ�е�̼���ƺ��������ƣ��ʴ�Ϊ����ȥ��Һ�е�̼���ƺ��������ƣ�
�ܲ���D�ӹ���NaOH��Һ��Ϊ�˳�ȥMg2+����Ӧ�����ӷ���ʽΪMg2++2OH-= Mg(OH)2�����ʴ�Ϊ��Mg2++2OH-= Mg(OH)2����
�������ϡ�������ϡ���ᣬ������NO3-���ʣ��ʴ�Ϊ��������NO3-���ʣ�
(3)����������������Һ����Ȼ����NaCl��ֻ��Ҫ���麬�������Ӽ��ɣ�����Ϊ��ȡ�����������Һ�������е���ϡ�����ữ���ٵμ���������Һ�������ְ�ɫ������֤������NaCl���ʴ�Ϊ��ȡ�����������Һ�������е���ϡ�����ữ���ٵμ���������Һ���μ���������Һ�������ɫ������
(4)�������������У�ͨ������Ũ������ȴ�ᾧ�����˵ķ�����ȥNaCl��ԭ������ͬ�¶���NaCl��NaOH���ܽ�Ȳ�ͬ���Ȼ��Ƶ��ܽ�������¶ȱ仯�������������ܽ�Ƚϴ������¶ȵı仯�ϴ����Ƶ��������ƾ��壬�ʴ�Ϊ�����ˣ�NaOH��
(5)��������ͼ�����������п�ѭ��ʹ�õ�������NaCl��NaOH���ʴ�Ϊ��NaCl��NaOH��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹһþ���Ͻ��ĩ�ڹ���ϡH2SO4���ܽ⣬��������Һ�м���NaOH��Һ�����ɳ���������w�ͼ���NaOH��Һ�����V�Ĺ�ϵ��ͼ��ʾ����úϽ���þ����������֮��Ϊ�� ��
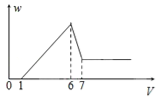
A. 2��3 B. 1��1 C. 4��3 D. 8��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����KNO3������Ʒ�к���������KCl��BaCl2���ʣ�Ϊ���ᴿKNO3������õ�BaCl2����������ʵ�������

��1���������K2CO3��������Ӧ�����ӷ���ʽΪ_________________________________��
��2�������ͼ�����ʵ��ܽ�����߿�֪�����۵�������_________________��

��3��������Ϊ������֮ǰ��������������b��Ҳ�ܵõ������Ĺ���1������Ϊ�ù۵��Ƿ���ȷ������������______________________________________��
��4�����Ƶõ� KNO3�������� 200 mL0.2mol/L KNO3 ��Һ��
�ٱ�ʵ���õ�����������ƽ��ҩ�ס����������ձ�����ͷ�ιܡ���Ͳ������_______________��
�����������ʹ�����Ƶ�KNO3 ��Һ��Ũ��ƫ�ߵ���______________������ĸ����
A��û��ϴ���ձ��Ͳ����� B������ƿ�����������������ˮ
C������ʱ���ӿ̶��� D������ʱ���ӿ̶���
E�����ݺ�����ƿ������ҡ�ȣ����ú�Һ����ڿ̶��ߣ��ټ�ˮ���̶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3COOH����ѧ��ѧ�г��õ�һԪ���ᣬ��ش��������⣺
��1����Ƽ�ʵ��֤��CH3COOHΪ����__��
��2����0.1mol/L CH3COOH��Һ�м�����ˮϡ����100mL����ϡ�����У��������ı仯�ǣ�����������С���������䡱����ȷ��������
n(H+)=___��![]() =___��
=___��![]() =__��c(OH-)=___��
=__��c(OH-)=___��
��3��OH-Ũ����ͬ�ĵ������������Һ�������CH3COOH���ֱ���п�۷�Ӧ����������һ����Һ�д���п�ۣ��ҷų�������������ͬ��������˵����ȷ����__����д��ţ�
�ٷ�Ӧ��Ҫ��ʱ�䣺CH3COOH��HCl
�ڿ�ʼ��Ӧ�����ʣ�HCl��CH3COOH
�۲μӷ�Ӧ��п�۵����ʵ�����CH3COOH=HCl
�ܷ�Ӧ���̵�ƽ�����ʣ�CH3COOH��HCl
����������п��ʣ��
��CH3COOH��Һ����п��ʣ��
��4����ʳ��ˮ�еμ�һ��Ũ�ȵ����ᣬ�Գ��������Ԥ�������ȷ����__��
A.��ɫ���� B.Һ��ֲ� C.���������� D.����ɫ����
��5������������Һ���ٴ�ˮ����pH=10��NaOH��Һ����pH=3�Ĵ�����Һ����pH=10��CH3COONa��Һ���ԱȽ�������Һ��ˮ�ĵ���̶ȵĴ�С��ϵ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ĺϳ�·������ͼ��ʾ
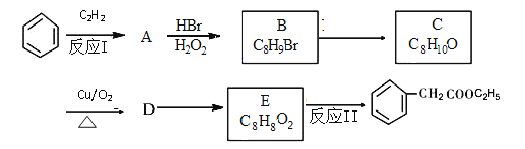
��1����Ӧ����Ӧ����Ϊ___________________�� D�к���������Ϊ_____________д���ƣ���
��2����Ӧ���ķ�Ӧ����Ϊ��_________________��
��3��C��D�Ļ�ѧ��Ӧ����ʽΪ________________________________________��
��4��д��һ����������������E��ͬ���칹��Ľṹ��ʽΪ__________________________��
���ܷ���������Ӧ �ں������ұ�����һ��������� �۲������Ʒ�Ӧ
��5��д��B�ϳ�![]() �ĺϳ�·�ߡ��ϳ�·�߳��õı�ʾ��ʽΪ��_______________
�ĺϳ�·�ߡ��ϳ�·�߳��õı�ʾ��ʽΪ��_______________
![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ���������������ϴ�������Ҫ�ɷ�ΪAl2O3������������Pd(��)����������������Pd���������£�
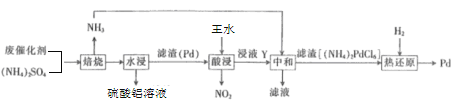
�ش��������⣺
��1������������Һ����Ũ������ȴ�õ�ʮ��ˮ�����������壬�ù���Ļ�ѧʽΪ___��
��2������ʱAl2O3��(NH4)2SO4��Ӧ�Ļ�ѧ����ʽΪ___��
��3����ˮ��Ũ�����Ũ���ᰴ�����Ϊ___�Ļ�����ˮ���ȶ�������ʱ��������������(NOCl)���������÷�Ӧ�Ļ�ѧ����ʽΪ___��
��4����ҺY�к�PdԪ�ص�������H2PdCl6(������)���������ʱ��Ӧ�Ļ�ѧ����ʽΪ___��
��5�������Ȼ�ԭ���еõ��Ĺ���ֻ��Pd��ÿ����1molPdʱ���ɵ���������ʵ���Ϊ___��
��6��Pd�������Ĵ���������䴢��ԭ��Ϊ2Pd��s��+xH2��g���T2PdHx��s��������x�����ֵΪ0.8����֪��Pd���ܶ�Ϊ12gcm��3����21.2cm3Pd�ܴ����״����H2��������Ϊ___L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮϵ�����ӵ�ذ�ȫ���ܺá��۸�������Ի����Ѻã����ž���г�ǰ����ij�����ӵ�ع���ԭ����ͼ������ܷ�ӦΪ��2NaFePO4F + Na3Ti2(PO4)3![]() 2Na2FePO4F+ NaTi2(PO4)3
2Na2FePO4F+ NaTi2(PO4)3
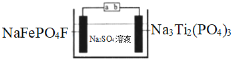
����˵���������
A.���ʱ��a�ӵ�Դ����
B.�ŵ�ʱ����Һ�е�Na+��NaFePO4F�缫�ϵõ��ӱ���ԭ
C.���ʱ�������ϵĵ缫��ӦΪNaTi2(PO4)3+2Na++2e��=Na3Ti2(PO4)3
D.�����ϣ��õ���ڳ���ŵ��������Һ�е�c(Na+)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������һ�ְ�ɫ���壬������ˮ���������Ҵ�����ѧ����������������ơ�ijѧϰС������ڼ��Ի���������CaCl2��H2O2��Ӧ��ȡCaO2��8H2O��װ����ͼ��ʾ��
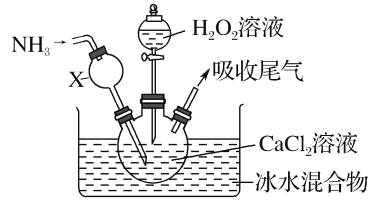
�ش��������⣺
��1��С��ͬѧ��������֪����ʵ������������Ϊ20%��H2O2��Һ��Ϊ���ˡ�����H2O2��Һ����������Ϊ30%����С��ͬѧ������H2O2��Һ����Լ20%��H2O2��Һ�Ĺ����У�ʹ�õIJ�������������������ͷ�ι��⣬����___��
��2������X����Ҫ���ó������⣬�����е�������___��
��3���ڱ�ˮԡ�н��е�ԭ����___��
��4��ʵ��ʱ����������ƿ������CaO2��8H2O���壬�ܷ�Ӧ�����ӷ���ʽΪ___��
��5����Ӧ���������ˡ�ϴ�ӡ����º�ɻ��CaO2��8H2O�������Լ��У�ϴ��CaO2��8H2O�����ѡ����____��
A����ˮ�Ҵ� B��Ũ���� C��Na2SO3��Һ D��CaCl2��Һ
��6����CaCl2ԭ���к���Fe3+���ʣ�Fe3+���ֽ�H2O2����ʹH2O2�����������Խ��͡���Ӧ�Ļ���Ϊ��
��Fe3+ +H2O2=Fe2++H++HOO��
��H2O2+X=Y +Z+W������ƽ��
��Fe2++��OH=Fe3++OH-
��H+ +OH-=H2O
�������������Ƶ�������еĻ�ѧ����ʽΪ___��
��7���������ƿ����ڳ�;�������磬�������˹������ƾ���____�����ʡ�
A.��ˮ������Ӧ���� B.���������������CO2����
C.����ˮ��������ǿ D.����ǿ�����ԣ���ɱ������
��8��������CaO2��8H2O������ȵ�150~160�棬��ȫ��ˮ��õ�����������Ʒ��
��С��ⶨ����������Ʒ��CaO2�Ĵ��ȵķ����ǣ�ȷ��ȡ0.4000g����������Ʒ��400�����ϼ�������ȫ�ֽ��CaO��O2(�����ʲ���������)���õ�33.60mL(�ѻ���Ϊ��״��)���塣
�����ù���������Ʒ��CaO2�Ĵ���Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ˮ��Һ�У�ֻ���ܺ������������е������֣�K����Mg2����Fe3����NH![]() ��Cl����CO
��Cl����CO![]() ��SO
��SO![]() ����ÿ��ȡ10.00 mL����ʵ�飺
����ÿ��ȡ10.00 mL����ʵ�飺
�ٵ�һ�ݼ���AgNO3��Һ�г���������
�ڵڶ��ݼ�������NaOH����ȣ��ռ�������0.672 L��(��״����)��
�۵����ݼ�����BaCl2��Һ��ø������6.63 g����������������ϴ�ӣ������ʣ4.66 g��
��ش�
(1) c(CO![]() )��____mol��L��1��
)��____mol��L��1��
(2) K���Ƿ���ڣ�_______�������ڣ�Ũ�ȷ�Χ��_____(�������ڣ��ػش�)��
(3) ��������ʵ��:
�ٲ����ж���Щ�����Ƿ����________________;
����������Щ���ӣ���ν��м��飿_____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com