
【题目】已知原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素;Y和Z基态原子的未成对电子数均等于周期序数;D的氧化物是典型的两性氧化物;E是所在周期中电负性最大的元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体。请回答下列问题(用元素符号或化学式表示):
(1)X元素位于周期表的________区。
(2)基态D原子的价电子轨道表示式是______,其第一电离能反常地低于同周期前一种元素,原因是_______。
(3)YZ2分子的电子式是__________,该分子的空间构型是_____________。
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲中Y原子的杂化类型是_______,它能溶于水的原因是______________。
(5)金属F与XE的热浓溶液反应产物之一是X3[FE4],该反应的化学方程式是______________。
(6)F与Z形成的一种晶胞结构如图,其中F原子均匀地分散在立方体内部,原子a、b、d的坐标参数依次为(0,0,0)、(![]() ,
, ![]() ,
, ![]() )、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。
)、(3m,3m,3m),则m=________。已知该晶体的密度为ρg/cm3, NA是阿伏伽德罗常数值,则原子b和d之间的核间距是__________nm(列出计算式即可)。

【答案】 s ![]() Mg原子的3s2全充满,反而比Al原子3p1稳定
Mg原子的3s2全充满,反而比Al原子3p1稳定 ![]() 直线型 sp2 HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶 2Cu+8 HCl(浓)
直线型 sp2 HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶 2Cu+8 HCl(浓) ![]() H2↑+2H3[CuCl4]
H2↑+2H3[CuCl4] ![]()
![]() ×
×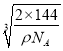 ×107
×107
【解析】原子序数依次增大的X、Y、Z、D、E、F六种前四周期元素。X是宇宙中最丰富的元素,X为H元素;Y和Z基态原子的未成对电子数均等于周期序数,则Y为C元素,Z为O或P元素;D的氧化物是典型的两性氧化物,D为Al元素,则Z为O元素;E是所在周期中电负性最大的元素,E为卤族元素;F的单质是一种紫红色金属,在潮湿空气中该金属表面会慢慢生成一种绿色固体,F为Cu元素,则E为Cl元素。
(1)X为H元素,价电子排布式为1s1,位于周期表的s区,故答案为:s;
(2) D为Al元素,基态D原子的价电子轨道表示式为![]() ,镁元素的3p为全空,为稳定状态,第一电离能比铝高,故答案为:
,镁元素的3p为全空,为稳定状态,第一电离能比铝高,故答案为:![]() ;Mg原子的3s2全充满,反而比Al原子3p1稳定;
;Mg原子的3s2全充满,反而比Al原子3p1稳定;
(3)YZ2为CO2,电子式为![]() ,C原子采用sp杂化,分子的空间构型直线型,故答案为:
,C原子采用sp杂化,分子的空间构型直线型,故答案为:![]() ;直线型;
;直线型;
(4)甲是由X、Y、Z三种原子构成的含有16个电子的分子,甲为HCHO,其中C原子的价层电子对数=3+![]() ×(4-2×1-1×2)=3,采用sp2杂化,HCHO和H2O分子间形成氢键,且都是极性分子,根据相似相溶原理,HCHO能溶于水,故答案为:sp2;HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶;
×(4-2×1-1×2)=3,采用sp2杂化,HCHO和H2O分子间形成氢键,且都是极性分子,根据相似相溶原理,HCHO能溶于水,故答案为:sp2;HCHO和H2O分子间形成氢键,且都是极性分子,相似相溶;
(5)金属铜与氯化氢的热浓溶液反应产物之一是H3[CuC14],反应的化学方程式为2Cu+8 HCl(浓) ![]() H2↑+2H3[CuCl4] ,故答案为:2Cu+8 HCl(浓)
H2↑+2H3[CuCl4] ,故答案为:2Cu+8 HCl(浓) ![]() H2↑+2H3[CuC14];
H2↑+2H3[CuC14];
(6)根据原子a、b、d的坐标参数依次为(0,0,0)、(![]() ,
, ![]() ,
, ![]() )、(3m,3m,3m),可知a为坐标原点,则d的坐标为(
)、(3m,3m,3m),可知a为坐标原点,则d的坐标为(![]() ,
, ![]() ,
, ![]() ),因此m=
),因此m=![]() 。
。
晶胞中,白球的数目为8×![]() +1=2,黑球全部在晶胞内部,数目为4,化学式为Cu2O;把晶胞分成8个小的立方体如图
+1=2,黑球全部在晶胞内部,数目为4,化学式为Cu2O;把晶胞分成8个小的立方体如图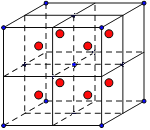 ,则Cu位于小立方体的中心,即小红球,则Cu+与O2-之间的最近距离为小立方体的体对角线的一半。Cu2O晶体的密度为ρ gcm3,1mol晶胞的质量为2×144g,则晶胞的边长为
,则Cu位于小立方体的中心,即小红球,则Cu+与O2-之间的最近距离为小立方体的体对角线的一半。Cu2O晶体的密度为ρ gcm3,1mol晶胞的质量为2×144g,则晶胞的边长为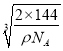 cm=
cm=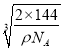 ×107 nm,因此Cu+与O2-之间的最近距离为
×107 nm,因此Cu+与O2-之间的最近距离为![]() ×
×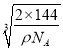 ×107 nm,故答案为:
×107 nm,故答案为: ![]() ×
×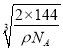 ×107。
×107。


科目:高中化学 来源: 题型:
【题目】下列实验中,始终无明显现象的是
A. NH3通入AlCl3溶液中
B. SO2通入HNO3酸化的Ba(NO3)2溶液中
C. NO2通入FeSO4溶液中
D. CO2通入CaCl2溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用元素周期律解释的是( )
A.酸性:HClO4>H2SO4
B.Na、Mg与水反应,Na更剧烈
C.气态氢化物的稳定性:HF>HCl
D.向Na2SO3溶液中加盐酸,有气泡产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是________。
2NH3(g)△H<0。下列各项能说明该反应已经达到平衡状态的是________。
A、容器内气体密度保持不变
B、容器内温度不再变化
C、断裂1mol N≡N键的同时,生成6mol N﹣H键
D、反应消耗N2、H2与产生NH3的速率之比1:3:2
(2)已知:①Zn(s)+1/2O2(g) = ZnO(s) △H =-348.3 kJ/mol
②2Ag(s)+1/2O2(g) = Ag2O(s) △H =-31.0 kJ/mol
则Zn(s)+Ag2O(s) = ZnO(s)+2Ag(s)的△H=________ kJ/mol。
(3)已知两个热化学方程式:
C(s)+O2(g)==CO2(g) △H = -393.5kJ/mol
2H2(g)+O2(g)==2H2O(g)△H = -483.6kJ/mol
现有0.2mol炭粉和H2组成悬浮气,使其在O2中完全燃烧,共放出63.53kJ的热量,则炭粉与H2的物质的量之比是________。
(4)在水溶液中,YO3n-和S2-发生反应的离子方程式如下:YO3n- + 3S2- + 6H+ = Y-+ 3S↓+ 3H2O
①YO3n-中Y的化合价是_____________;
②Y元素原子的最外层电子数是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.2 mol·L-1的NaOH溶液滴定10.00mL0.2 mol·L-1一元酸HA溶液,溶液的温度和pH随加入NaOH溶液体积(V)的变化曲线如图所示。下列有关说法不正确的是
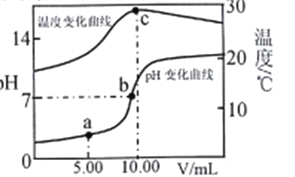
A. HA是弱酸
B. c点水的离子积最大
C. c点后温度降低主要原因是NaA水解吸热
D. 在a、b点之间(不包括b点)一定有c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:
4HCl(g) + O2(g)![]() 2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
2Cl2(g) + 2H2O(g) ΔH=-115.6 kJ/mol
恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是
A. 氯化氢的转化率不再改变 B. 气体的质量不再改变
C. 断开4 mol H-Cl键的同时生成4 mol H-O键 D. n(HCl)∶n(O2)∶n(Cl2)∶n(H2O)=4∶1∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是( )
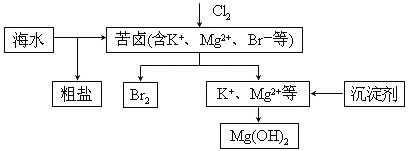
A. 向苦卤中通入Cl2是为了提取溴
B. 工业生产中常选用NaOH作为沉淀剂
C. 粗盐可采用除杂和重结晶等过程提纯
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用![]() 将其还原吸收
将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组为了模拟工业流程从浓缩的海水中提取液溴,查阅资料知:Br2的沸点为59℃,微溶于水,有毒性。设计了如下操作步骤及主要实验装置(夹持装置略去):
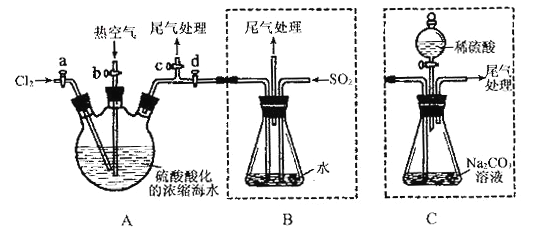
①连接A与B,关闭活塞b、d,打开活塞a、c,向A中缓慢通入至反应结束;②关闭a、c,打开b、d,向A中鼓入足量热空气;③进行步骤②的同时,向B中通入足量SO2 ;④关闭b,打开a,再通过A向B中缓慢通入足量Cl2 ;
⑤将B中所得液体进行蒸馏,收集液溴。
请回答:(1)实验室中采用固液加热制备氯气的化学方程式为______________________;
(2)步骤②中鼓入热空气的作用为_________________________;
(3)步骤③B中发生的主要反应的离子方程式为_____________________。
(4)此实验中尾气可用______________(填选项字母)吸收处理。
a.水 b.浓硫酸 c.NaOH溶液 d.饱和NaCl溶液
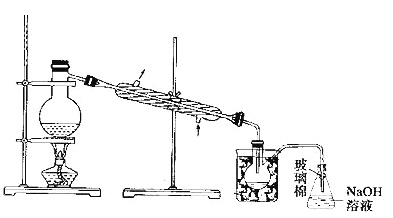
(5)步骤⑤中,用下图所示装置进行蒸馏,收集液溴,将装置图中缺少的必要仪器补画出来。
(6)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中滴加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,C中反应生成了NaBrO3等,请写出滴加稀硫酸时发生反应的离子方程式_________________。
(7)与B装置相比,采用C装置的优点为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯醇(CH2=CH—CH2OH)可发生的化学反应有( )
①加成 ②氧化 ③燃烧 ④加聚 ⑤取代
A. ①②③B. ①②③④
C. ①②③④⑤D. ①③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com