
【题目】图所示与对应叙述相符的是
A.  表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS) <Ksp(CuS)
表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS) <Ksp(CuS)
B.  pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸
pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸
C.  表示用0.1000 mol·L-lNaOH溶液滴定25.00 mL盐酸的滴定曲线,则 c(HCl)=0.0800 mol ·L-1
表示用0.1000 mol·L-lNaOH溶液滴定25.00 mL盐酸的滴定曲线,则 c(HCl)=0.0800 mol ·L-1
D.  反应N2(g)+3H2(g)
反应N2(g)+3H2(g) ![]() 2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2)
【答案】C
【解析】
A.当相同c(S2-)时,由图像可知,平衡时c(Cu2+)<c(Fe2+),则c(Fe2+)c(S2-)>c(Cu2+)c(S2-),根据Ksp(FeS)=c(Fe2+)c(S2),Ksp(CuS)=c(Cu2+)c(S2),则Ksp(FeS)>Ksp(CuS),故A错误;
B.溶液中pH值与c(H+)间的关系为pH=-lgc(H+),溶液中c(H+)大,对应的pH值就小,当稀释弱酸时,随着水的加入,稀释可以促进弱酸的电离,但是总体来讲,溶液体积的增量超过溶液中H+的物质的量的增量,表现为溶液中c(H+)=![]() 减小,pH值增大;由于稀释促进弱酸的电离,因而在稀释相同倍数的弱酸时,对于酸性较弱的酸,能够促进其电离,增加了溶液中H+的量,也就表现为c(H+)会较酸性较强的弱酸大些,pH就较酸性较强的弱酸小些,因此总的来讲,酸性较强的弱酸稀释后对应的溶液pH值越大,从图像看出,甲酸的酸性是较乙酸强,即酸性甲酸>乙酸,故B错误;
减小,pH值增大;由于稀释促进弱酸的电离,因而在稀释相同倍数的弱酸时,对于酸性较弱的酸,能够促进其电离,增加了溶液中H+的量,也就表现为c(H+)会较酸性较强的弱酸大些,pH就较酸性较强的弱酸小些,因此总的来讲,酸性较强的弱酸稀释后对应的溶液pH值越大,从图像看出,甲酸的酸性是较乙酸强,即酸性甲酸>乙酸,故B错误;
C.用0.1000mol/L的NaOH溶液滴定25.00mL的盐酸溶液,由图像可知,当消耗NaOH体积为20.00mL时,溶液为中性,此时酸和碱恰好完全反应,溶液中c(H+)=c(OH-),即n(H+)=n(OH-),则有c(HCl)V(HCl)=c(NaOH)V(NaOH),因此c(HCl)=![]() =
=![]() =0.0800mol/L,故C正确;
=0.0800mol/L,故C正确;
D.由图像可知,A与B状态时NH3的百分含量相等,对于有两种反应物参加的可逆反应,增加其中一种反应物的物料可使另一种反应物的转化率增加;A状态时,![]() 值较小,可认为是增加了H2的量使得H2自身的转化率变小,B状态时,
值较小,可认为是增加了H2的量使得H2自身的转化率变小,B状态时,![]() 值较大,可认为是增加了N2的量,从而提高了H2的转化率,转化率αA(H2)不一定等于αB(H2),故D错误;
值较大,可认为是增加了N2的量,从而提高了H2的转化率,转化率αA(H2)不一定等于αB(H2),故D错误;
答案选C。


科目:高中化学 来源: 题型:
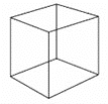
【题目】立方烷结构为立方体,分子式为C8H8,其熔点比相同碳原子的辛烷高,立方烷的结构简式如图所示。下列有关立方烷的说法正确的是( )
A.其一氯代物只有1种,二氯代物有2种
B.常温常压下为气体
C.与乙苯(结构简式为![]() )是同分异构体
)是同分异构体
D.与苯的含碳质量分数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1mol下列物质完全燃烧生成稳定的产物时放出的热量如下:

则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的ΔH为( )
A.-44.2kJ·mol-1B.44.2kJ·mol-1
C.-330kJ·mol-1D.330kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25°C时,![]() ,
,![]() 。下列说法正确的是
。下列说法正确的是
A.25°C时,饱和![]() 溶液与饱和
溶液与饱和![]() 溶液相比,前者的
溶液相比,前者的![]() 大
大
B.25°C时,在![]() 的悬浊液加入少量的
的悬浊液加入少量的![]() 固体,
固体,![]() 增大
增大
C.25°C时,![]() 固体在20ml0.01 mol·
固体在20ml0.01 mol·![]() 氨水中的
氨水中的![]() 比在20mL0.01mol·
比在20mL0.01mol·![]()
![]() 溶液中的
溶液中的![]() 小
小
D.25°C时,在![]() 的悬浊液加入
的悬浊液加入![]() 溶液后,
溶液后,![]() 不可能转化成为
不可能转化成为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向Na2CO3溶液中滴入盐酸,混合溶液的pH与离子浓度变化的关系如图所示。已知:lgX=lg![]() 或lg
或lg![]() ,下列叙述正确的是( )
,下列叙述正确的是( )

A.曲线m表示pH与![]() 的变化关系
的变化关系
B.当溶液呈中性时,c(Na+)=c(HCO3-)+2c(CO32-)
C.Ka1(H2CO3)=1.0×10-6.4
D.25℃时,CO32-+H2O![]() HCO3-+OH-的平衡常数为1.0×10-5.7
HCO3-+OH-的平衡常数为1.0×10-5.7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液 b.澄清石灰水 c.饱和小苏打溶液 d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000 mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U型管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________(填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应可用于合成CH3OH:
![]()
(1)Mn2+基态核外电子排布式为____________。
(2)与NO3-互为等电子体的分子为_______(写化学式)。
(3)CO32-的空间构型是________(用文字描述)。
(4)1molCH3OH中含有σ键的数目为______mol。CH3OH与H2O可以任意比互溶,除因为它们都是极性分子外,还因为________。
(5)锰元素的一种硫化物晶体的晶胞结构如图所示,该硫化物的化学式为________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是
A.N2O的电子式可表示![]()
B.N2O与SiO2为等电子体、具有相似的结构(包括电子式)
C.N2O与CO2均不含非极性键
D.N2O为三角形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物X、Y、A、B、C、D、E、F、G之间的转化关系如下所示。

已知以下信息:
①![]()
②![]() (R、R’代表烃基)
(R、R’代表烃基)
③X在催化剂作用下可与H2反应生成化合物Y。
④化合物F的核磁共振氢谱图中只有一个吸收峰。
回答下列问题:
(1)X的含氧官能团的名称是______,X与HCN反应生成A的反应类型是________。
(2)酯类化合物B的分子式是C15H14O3,其结构简式是________________。
(3)X发生银镜反应的化学方程式是______________________________________
(4)G在NaOH溶液中发生水解反应的化学方程式是_________________________
(5) 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位。满足上述条件的同分异构体共有________种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式____________________________________________。
的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位。满足上述条件的同分异构体共有________种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式____________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com