
【题目】某同学利用如图所示的实验装置进行铁跟水蒸气反应的实验,并研究铁及其化合物的部分性质。请回答下列问题:
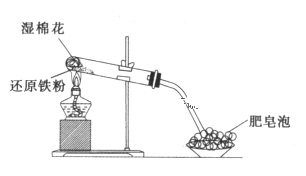
(1)硬质试管中发生反应的化学方程式为_______________________________。
(2)该同学为确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明硬质试管的固体物质中一定有_________,可能有__________________;若溶液未变红色,则说明硬质试管中固体物质的成分是_____________________________________。
(3)该同学按(2)中所述实验方案进行了实验,结果溶液未变红色,原因是________________________________(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其与NaOH溶液反应。若按图所示操作,可观察到试管中先生成白色沉淀,后沉淀迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变为红褐色的过程中所发生反应的化学方程式:__________________________________。
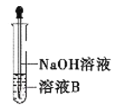
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明![]() 具有_________性。由此可知,实验室中含
具有_________性。由此可知,实验室中含![]() 的盐溶液需现用现配制的原因是__________,并且配制含
的盐溶液需现用现配制的原因是__________,并且配制含![]() 的盐溶液时应加入少量___________________。
的盐溶液时应加入少量___________________。
【答案】3Fe+4H2O(g) ![]() Fe3O4+4H2 Fe3O4 Fe Fe3O4和Fe Fe+2Fe3+=3Fe2+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 还原 易被空气中的氧气氧化而变质 铁粉
Fe3O4+4H2 Fe3O4 Fe Fe3O4和Fe Fe+2Fe3+=3Fe2+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 还原 易被空气中的氧气氧化而变质 铁粉
【解析】
(1)依据铁与水蒸气高温下反应生成四氧化三铁和氢气解答;
(2)KSCN溶液溶液变红色,说明有三价铁离子;溶液未变红色,说明无三价铁离子;
(3)铁单质能将三价铁离子还原成二价铁离子;
(4)白色沉淀为氢氧化亚铁,氢氧化亚铁具有还原性,易被空气中氧气氧化生成氢氧化铁;
(5)未变红的溶液变成红色,Fe2+ 被氧化为Fe3+,说明具有还原性。
(1)铁与水蒸气高温下反应生成四氧化三铁和氢气,装置中湿棉花的作用提供水蒸气,发生反应的化学方程式为:3Fe+4H2O(g) ![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)KSCN溶液变红色,说明有三价铁离子,说明硬质试管中固体一定有Fe3O4,可能有Fe;KSCN溶液未变红色,说明无三价铁离子,一定有Fe3O4和Fe;
(3)铁单质能将三价铁离子还原成二价铁离子,离子方程式,Fe+2Fe3+=3Fe2+;
(4)白色沉淀为氢氧化亚铁,氢氧化亚铁具有还原性,易被空气中氧气氧化生成氢氧化铁,反应的方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)未变红的溶液变成红色,Fe2+ 被氧化为Fe3+,说明具有还原性。实验室中含Fe2+的盐溶液需现用现配制的原因是易被空气中的氧气氧化而变质,并且配制含Fe2+的盐溶液时应加入少量铁粉,可以把氧化后的Fe2+再还原成Fe2+。


科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2Cl2)是一种常用于橡胶硫化、有机物氯化的试剂,甲同学查阅资料:①将干燥的氯气在110~140 ℃ 间与硫反应,即可得S2Cl2粗品;②有关物质的部分性质如表所示:
物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
S | 112.8 | 444.6 | 略 |
S2Cl2 | -77 | 137 | ①一种橙黄色的液体,遇水易水解,有淡黄色固体出现,同时产生能使品红溶液褪色的气体。 ②300 ℃以上完全分解。③S2Cl2+Cl2=2SCl2 |
设计如图所示实验装置在实验室合成S2Cl2:
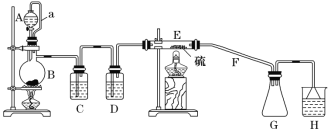
回答以下问题:
(1)仪器A的名称是_______________。
(2)B中所发生反应的离子方程式为___________________________________。
(3)C装置的作用是___________________________________ 。
(4)S2Cl2粗品中可能混有的杂质是_______________ (写其中一种,填化学式)。
(5)乙同学发现,该装置中除了E处的温度不能过高外,还有一处重大缺陷需改进,否则会导致S2Cl2的产率大大降低,原因是______________________________ (用化学方程式表示);请简要提出改进方案:________________________________________________。
(6)H中的溶液可以选择下列试剂中的__________ (填字母)。
A 碳酸钠溶液 B 氯化铁溶液 C 高锰酸钾溶液 D 亚硫酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.
A元素原子的核外p电子数比s电子数少3 |
B元素形成的物质种类繁多.其形成的一种固体单质工业上常用作切割工具 |
C元素基态原子p轨道有3个未成对电子 |
D原子核外所有p轨道全满或半满 |
E在该周期中未成对电子数最多 |
F能形成红色(或砖红色)和黑色的两种氧化物 |
某同学根据上述信息,推断
(1)画出A基态原子的核外电子排布图____________________。
(2)B基态原子的核外电子排布图![]() , 该同学所画的电子排布图违背了____________________________________。
, 该同学所画的电子排布图违背了____________________________________。
(3)D基态原子中能量最高的电子,其电子云在空间有____________个方向,原子轨道呈____________形。
(4)写出C原子的电子排布式 ____________;写出E原子的电子简化排布式____________。
(5)请写出F元素价电子排布式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为__________;得到滤渣1的主要成分为__________。
(2)第②步中加H2O2的作用是__________,使用H2O2的优点是__________;调溶液pH的目的是使__________生成沉淀。
(3)第③步所得CuSO4·5H2O制备无水CuSO4的方法是__________。
(4)由滤渣2制取Al2(SO4)3·18H2O,探究小组设计了三种方案:
甲:滤渣2![]() 酸浸液
酸浸液![]() Al2(SO4)3·18H2O
Al2(SO4)3·18H2O
乙:滤渣2![]() 酸浸液
酸浸液![]() 滤液
滤液![]() Al2(SO4)3·18H2O
Al2(SO4)3·18H2O
丙:滤渣2![]() 滤液
滤液![]() 溶液
溶液![]() Al2(SO4)3·18H2O
Al2(SO4)3·18H2O
上述三种方案中,__________方案不可行,原因是__________;
从原子利用率角度考虑,__________方案更合理。
(5)探究小组用滴定法测定CuSO4·5H2O(Mr=250)含量。取ag试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用cmol·L-1EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。滴定反应为:Cu2++H2Y2-=CuY2-+2H+
①写出计算CuSO4·5H2O质量分数的表达式ω=__________;
②下列操作会导致含量的测定结果偏高的是______。
a 未干燥锥形瓶
b 滴定终点时滴定管尖嘴中产生气泡
c 未除净可与EDTA反应的干扰离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):
![]()
![]()
![]()
![]()
![]()
(1)若A是一种金属,C是淡黄色固体,则B的化学式为________________,A→C反应的化学方程式为________________。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为_______,B→C反应的化学方程式为____________________________。A和C是否能反应?______(填“能”或“不能”),若能,写出反应的化学方程式:____________________(若不能,此空不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联合国宣布2019年为“国际化学元素周期表年”。现有四种不同主族短周期元素X、Y、Z、W的原子序数依次递增,X与Y形成的化合物是光合作用的原料之一,Z、W处于同周期且族序数相差6。下列说法正确的是
A. 元素非金属性:![]()
B. Y和Z形成的化合物中只存在离子键
C. Z、W的简单离子半径:![]()
D. 只有W元素的单质可用于杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铜矿(CuFeS2)、FeCl3和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下:

(1) FeCl3溶液与黄铜矿发生反应的离子方程式为___________________________________________。
(2)向溶液1中加入过量铁粉的目的是_______________________________________________。
(3)过滤后得到的FeCO3固体应进行洗涤,检验洗涤已完全的方法是__________________________。

(4)实验室制备乳酸亚铁的装置如图所示。
①实验前通入N2的目的是_______________________________________。
②某兴趣小组用KMnO4滴定法测定样品中Fe2+含量进而计算产品中乳酸亚铁的质量分数,结果测得产品的质量分数总是大于100%,其原因可能是_______________________________________________。
(5)已知:
①CuCl为白色晶体,难溶于水和乙醇,在空气中易氧化;可与NaCl溶液反应,生成易溶于水的NaCuCl2。
②NaCuCl2可水解生成CuCl,温度、pH对CuCl产率的影响如图所示。


由CuCl(s)、S(s)混合物提纯CuCl的实验方案为:将一定量的混合物溶于饱和NaCl溶液中,________________________________________________________________________。(实验中须使用的试剂有:饱和NaCl溶液,0.1 mol·L-1 H2SO4、乙醇;除常用仪器外须使用的仪器有:真空干燥箱)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的化学用语表达正确的是( )
A | 质子交换膜氢氧燃料电池的负极反应 | O2+2H2O+4e﹣=4OH﹣ |
B | 用铁电极电解饱和食盐水 | 2Cl﹣+2H2O=Cl2↑+H2↑+20H﹣ |
C | 锅炉水垢中的CaSO4用饱和Na3CO3溶液浸泡 | CO32﹣+CaSO4=CaCO3+SO42﹣ |
D | KClO碱性溶液与Fe(OH)3反应制取K2FeO4 | 3ClO﹣+2Fe(OH)3=2FeO43﹣+3Cl﹣+4H++H2O |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是

A. A、B之间任意一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C. C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com