
【题目】A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去):
![]()
![]()
![]()
![]()
![]()
(1)若A是一种金属,C是淡黄色固体,则B的化学式为________________,A→C反应的化学方程式为________________。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为_______,B→C反应的化学方程式为____________________________。A和C是否能反应?______(填“能”或“不能”),若能,写出反应的化学方程式:____________________(若不能,此空不填)。
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在 2 L 恒容密闭容器中 3 种物质间进行反应,X、Y、Z 的物质的量随时间的变化曲线如图所示,反应在 t1 min 时达到平衡。

(1)请写出该反应的化学方程式:_____。
(2)若上述反应中X、Y、Z 分别为 NH3、H2、N2,在此 t1 min 时间内,用H2 表示该反应的平均速率 v(H2)为_____。
(3)拆开 1mol 共价键所需吸收的能量如下表:
共价键 | H-H | N≡N | N-H |
吸收的能量/kJ | 436 | 946 | 391 |
1mol N2 完全反应为NH3_____(填:吸收或放出)_____kJ 能量。事实上,将 1molN2 和3molH2 放在反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是_________。
(4)下列叙述能判断该反应达到平衡状态的是_____(填字母代号)。
A 容器内各气体组分的质量分数不再发生改变
B 正反应速率与逆反应速率相等
C 容器内气体的密度不再发生改变
D 混合气体的平均相对分子质量不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,10mL 0.40 mol·L-1H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 3 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是( )(溶液体积变化忽略不计)
A. 反应至6min时,H2O2分解了50%
B. 反应至6min时,c(H2O2)=0.20 mol·L-1
C. 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min)
D. 4~6min的平均反应速率:v(H2O2)>3.3×10-2mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两同学分别用如图所示装置测定空气中氧气的含量。先用弹簧夹夹住橡胶管,点燃钠,伸入瓶中并塞上瓶塞。待钠熄灭并冷却后,打开弹簧夹,观察广瓶内水面的变化情况:

(1)上述实验过程中发生反应的化学方程式为__________________________________。
(2)甲同学实验中广瓶内水面上升明显小于瓶内空气体积的![]() ,乙同学实验中广瓶内水面上升明显大于瓶内空气体积的
,乙同学实验中广瓶内水面上升明显大于瓶内空气体积的![]() ,下列对这两种现象解释合理的是________
,下列对这两种现象解释合理的是________
A.甲同学可能使用的钠的量不足,瓶内氧气没有消耗完
B.甲同学可能未塞紧瓶塞,钠熄灭冷却后外界空气进入瓶内
C.乙同学可能没有夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出
D.乙同学可能插入燃烧匙太慢,塞紧瓶塞之前瓶内部分空气受热逸出
(3)在实验室里,某同学取一小块金属钠做钠与水反应的实验。将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①__________,②__________,
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用如图所示的实验装置进行铁跟水蒸气反应的实验,并研究铁及其化合物的部分性质。请回答下列问题:
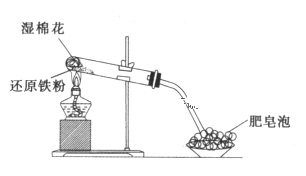
(1)硬质试管中发生反应的化学方程式为_______________________________。
(2)该同学为确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明硬质试管的固体物质中一定有_________,可能有__________________;若溶液未变红色,则说明硬质试管中固体物质的成分是_____________________________________。
(3)该同学按(2)中所述实验方案进行了实验,结果溶液未变红色,原因是________________________________(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其与NaOH溶液反应。若按图所示操作,可观察到试管中先生成白色沉淀,后沉淀迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变为红褐色的过程中所发生反应的化学方程式:__________________________________。
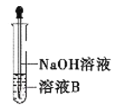
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明![]() 具有_________性。由此可知,实验室中含
具有_________性。由此可知,实验室中含![]() 的盐溶液需现用现配制的原因是__________,并且配制含
的盐溶液需现用现配制的原因是__________,并且配制含![]() 的盐溶液时应加入少量___________________。
的盐溶液时应加入少量___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如表所示:
X | Y | Z | W | R | P | Q | |
原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1、+7 | -3、+5 | +3 | ||
其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
请完成下列问题:
(1)W在周期表中的位置是___,X与P形成的化合物的电子式___。
(2)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为___。
(3)Z与Q两元素的最高价氧化物水化物之间发生反应的离子方程式为___。
(4)Y与R相比,非金属性较强的是___(用元素符号表示),根据下列方法能证明这一结论的是___(填字母序号)。
A.常温下Y的单质呈固态,R的单质呈气态
B.R、Y的氢化物稳定性不同
.Y与R形成的化合物中的化合价
D.R、Y的氧化物的水化物的酸性强弱
(5)用电子式表示由Z和R组成的化合物的形成过程___。
(6)如图为X2和R2燃烧反应的能量变化示意图,请根据此图写出该反应的热化学方程式为___(用物质化学式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量是高中化学中常用的物理量,请回答下列问题:
(1)某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO42-的物质的量是_____mol。
(2)在标准状况下,4.48 L HCl气体溶于水配成500 mL溶液,其物质的量浓度为_____________。
(3)在标准状况下,1.7 g氨气所占的体积约为_________L,与_____mol H2S含有相同的氢原子数。
(4)7.8 g Na2X中含Na+ 0.2 mol,则X的摩尔质量是_____________________。
(5)实验室需要0.3 molL-1硫酸溶液480 mL。
①配制过程用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管、试剂瓶外,还需要______________。
②需量取质量分数为98%、密度为1.84 gcm-3的浓硫酸的体积为______mL。
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应2NO2![]() 2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
2NO+O2在恒容密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成nmol O2的同时生成2nmol NO2;
②单位时间内生成nmol O2 的同时生成2nmol NO;
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态;
④混合气体的颜色不再改变的状态;
⑤密闭容器中压强不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
A. ①④⑤⑥B. ②③⑤⑥C. ①③④⑥D. 全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com